
1£®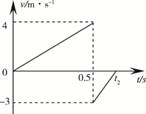 (10ĐûÎä̉»Ä£)17£®ÔÚ¿ƠÆø×èÁ¦´óĐ¡ºă¶¨µÄ̀ơ¼₫Ï£¬Đ¡Ç̣´Ó¿ƠÖĐÏÂÂ䣬ÓëˮƽµØĂæÏàÅö(Åöײʱ¼ä¼«¶̀)ºóµ¯µ½¿ƠÖĐij̉»¸ß¶È¡£̉ÔỊ̈ÏÂΪƠư·½Ị̈£¬ÆäËÙ¶ÈËæʱ¼ä±ä»¯µÄ¹ØϵÈçͼËùʾ£¬È¡g=10 m/s2£¬Ộ̉ÔϽáÂÛƠưÈ·µÄÊÇ¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡
(10ĐûÎä̉»Ä£)17£®ÔÚ¿ƠÆø×èÁ¦´óĐ¡ºă¶¨µÄ̀ơ¼₫Ï£¬Đ¡Ç̣´Ó¿ƠÖĐÏÂÂ䣬ÓëˮƽµØĂæÏàÅö(Åöײʱ¼ä¼«¶̀)ºóµ¯µ½¿ƠÖĐij̉»¸ß¶È¡£̉ÔỊ̈ÏÂΪƠư·½Ị̈£¬ÆäËÙ¶ÈËæʱ¼ä±ä»¯µÄ¹ØϵÈçͼËùʾ£¬È¡g=10 m/s2£¬Ộ̉ÔϽáÂÛƠưÈ·µÄÊÇ¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡
¡¡¡¡¡¡ A£®Đ¡Ç̣µ¯ÆđµÄ×î´ó¸ß¶ÈΪ1.0m
¡¡¡¡¡¡ B£®Đ¡Ç̣µ¯ÆđµÄ×î´ó¸ß¶ÈΪ0.45 m
¡¡¡¡¡¡ C£®Đ¡Ç̣µ¯Æđµ½×î´ó¸ß¶ÈµÄʱ¿̀t2=0.80 s
¡¡¡¡¡¡ D£®¿ƠÆø×èÁ¦ÓëÖØÁ¦µÄ±ÈֵΪ1¡Ă5
¡¡¡¡¡¡ ¿¼µă19£ºµÚ̉»ÓîÖæËÙ¶È(»·ÈÆËÙ¶È)£º
¡¡¡¡¡¡ ¿¼µă20£ºµÚ¶₫ÓîÖæËٶȺ͵ÚÈưÓîÖæËٶȣºÂäʵÓîÖæËÙ¶È֪ʶµă
¡¡¡¡¡¡ ̉âͼ£ºÖªÊ¶µăÂäʵ
3¡¢( 15 ·Ö)
(1)(Ă¿¿Ơ2·Ö£¬¹²6·Ö)HNO3£¬NH3¡¤H2O£¬NH4NO3(ºÏÀí´đ°¸£¬²ÎƠƠ¸ø·Ö)
(2)(Ă¿1·Ö)C£¬NH4++H2O NH3.H2O+H+(2·Ö)
NH3.H2O+H+(2·Ö)
(3)(Ă¿¿Ơ1·Ö£¬¹²6·Ö)
|
ÏîÄ¿ |
c(H+) |
c(OH£) |
¶ÔBµçÀëµÄÓ°Ḯ |
|
È¡1mLÓĂƠôÁóˮϡÊÍΪ100mLÈÜ̉º |
Ôö´ó |
¼ơĐ¡ |
´Ù½ø |
|
È¡1mLÓĂͬŨ¶ÈµÄCÈÜ̉ºÏ¡ÊÍΪ100mLÈÜ̉º |
Ôö´ó |
¼ơĐ¡ |
̉ÖÖÆ |
2¡¢(16·Ö)(1)¡¡ Na>Al>O¡¡¡¡¡¡
(2) Ï´µÓÓÍÎÛ»̣ÖƲ£Á§£»¡¡ ¼î¡¡ ĐÔ£¬ÀíÓÉÊÇ¡¡ CH3COO-+H2O CH3COOH+OH-¡¡
CH3COOH+OH-¡¡
(3)µç×Óʽ ¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡B¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡B¡¡¡¡
(4)Àë×Ó·½³̀ʽΪ¡¡ Al3++3NH3¡¤H2O=Al (OH)3¡ư+3NH4+¡¡ £¬¡¡ ÖĐĐÔ¡¡
1£®(15·Ö)(1) ¡¡¡¡¡¡(2·Ö)
¡¡¡¡¡¡(2·Ö)
(2)CH3CH2CH2OH¡¡¡(2·Ö)¡¡ (CH3)2CH2OH¡¡¡¡¡¡(¸÷2·Ö)
(3)CH3CHO+2Ag(NH3)2OH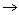 CH3COONH4+2Ag¡ư+3NH3+H2O¡(2·Ö)
CH3COONH4+2Ag¡ư+3NH3+H2O¡(2·Ö)
Ñơ»¯·´Ó¦(»̣̉ø¾µ·´Ó¦)¡¡¡¡¡¡(2·Ö)
(4)CH3CH2OH+C6H5COOH
 ¡¡C6H5COOC2H5+H2O¡¡¡¡ (2·Ö)
¡¡C6H5COOC2H5+H2O¡¡¡¡ (2·Ö)
ơ¥»¯·´Ó¦(»̣È¡´ú·´Ó¦)¡¡¡¡¡¡(1·Ö)
(5)D ºÍ H¡¡¡¡¡¡(2·Ö)
3¡¢( 15·Ö)A¡¢B¡¢CÈưÖÖ»¯ºÏÎ¶¼ÊÇÓÉÇâ¡¢µª¡¢ÑơÈưÖÖÔªËØËù×é³É£¬£¬ÆäÖĐ̉»ÖÖÊÇÈơµç½âÖÊ£¬Óà¾ùÊÇÇ¿µç½âÖÊ¡£AºÍB¿É̉Ôͨ¹ư¸´·Ö½â·´Ó¦ĐγÉC¡£³£Î£¬Å¨¶È¾ùΪa mol¡¤L£1µÄA¡¢B¡¢CÈưÖÖÏ¡ÈÜ̉ºÖĐ£¬pH´óĐ¡¹ØϵÊÇpH(B)> pH(C)> pH(A)¡£(1)Đ´³öÎïÖʵĻ¯Ñ§Ê½£ºA£º¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡B£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ C£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)A¡¢B¡¢CÈưÖÖÎïÖʸ÷×ÔÈܽâÔÚË®ÖĐʱ£¬ÄÜʹˮµÄµçÀë³̀¶ÈÔö´óµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £¬
¶ÔÓ¦µÄÀë×Ó·½³̀ʽΪ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)Èô½«a mol¡¤L£1µÄBÈÜ̉º½øĐĐÏÂÁĐʵÑ飬½«±ä»¯̀îĐ´ÔÚ¶ÔÓ¦±í¸ñÖĐ
|
ÏîÄ¿ |
ÈÜ̉ºÖĐc(H+) |
ÈÜ̉ºÖĐc(OH£) |
¶ÔBµçÀëµÄÓ°Ḯ |
|
È¡1mLÓĂƠôÁóˮϡÊÍΪ100mLÈÜ̉º |
¡¡ |
¡¡ |
¡¡ |
|
È¡1mLÓĂͬŨ¶ÈµÄCÈÜ̉ºÏ¡ÊÍΪ100mLÈÜ̉º |
¡¡ |
¡¡ |
¡¡ |
2¡¢(16·Ö)ϱíΪԪËØÖÜÆÚ±íµÄ̉»²¿·Ö£¬Çë²ÎƠƠÔªËآ٣¢àÔÚ±íÖеÄλÖĂ£¬»Ø´đÏÂÁĐÎỀ⣺
|
×å ÖÜÆÚ |
IA |
¡¡ |
0 |
|||||
|
1 |
¢Ù |
¢̣A |
¢óA |
¢ôA |
¢ơA |
¢öA |
¢÷A |
¡¡ |
|
2 |
¡¡ |
¡¡ |
¡¡ |
¢Ú |
¢Û |
¢Ü |
¡¡ |
¡¡ |
|
3 |
¢Ư |
¡¡ |
¢̃ |
¢ß |
¡¡ |
¡¡ |
¢à |
¡¡ |
(1)¢Ü¡¢¢Ư¡¢¢̃µÄÔ×Ӱ뾶ÓÉ´óµ½Đ¡µÄ˳Đ̣Ϊ______________(ÓĂÔªËØ·ûºÅ±íʾ)¡£
(2)¢Ù¡¢¢Ú¡¢¢Ü¡¢¢ƯÖеÄÈưÖÖÔªËØĐγɵÄijÎ̃»úÑεÄÓĂ;ÊÇ(¾Ù³ö̉»Àư¼´¿É)¡¡¡¡¡¡ £»ÓÉƠâËÄÖÖÔªËØĐγɵÄijÑεÄʽÁ¿Îª82£¬¸ĂÑεÄË®ÈÜ̉º³Ê_______ĐÔ£¬ÀíÓÉÊÇ(ÓĂÀë×Ó·½³̀ʽ½âÊÍ)______________________________________
(3)ÓɱíÖĐ¢Ü¡¢¢ƯÁ½ÖÖÔªËصÄÔ×Ó°´1£º1×é³ÉµÄ»¯ºÏÎïµÄµç×Óʽ_________________¡£ÓÉ1mol¸ĂÎïÖÊÓë2mol̀¼ËáÇâÄƹ̀̀å»́ºÏºó£¬ÔÚĂܱƠÈƯÆ÷ÖĐ¼ÓÈȳä·Ö·´Ó¦£¬ÅųöÆø̀åÎïÖʺóÀäÈ´£¬²ĐÁôµÄ¹̀̀åÎïÖÊÊÇ¡¡¡¡¡¡ ¡£
A£®NaOH¡¡ Na2CO3¡¡¡¡ B.Na2CO3¡¡¡¡¡¡ C.Na2O2¡¡ Na2CO3¡¡¡¡ D.Na2O2¡¡ NaOH¡¡ Na2CO3
(4)ÓɱíÖĐÔªËØĐγɵij£¼ûÎïÖÊX¡¢Y¡¢Z¡¢M¡¢N¿É·¢Éú̉ÔÏ·´Ó¦£º
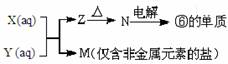 XÈÜ̉ºÓëYÈÜ̉º·´Ó¦µÄÀë×Ó·½³̀ʽΪ___________________________£¬³£ÎÂÏ£¬ÎªÊ¹0.1 mol/L
M ÈÜ̉ºÖĐÓÉMµçÀëµÄ̉ơ¡¢ÑôÀë×ÓŨ¶ÈÏàµÈ£¬Ó¦Ị̈ÈÜ̉ºÖĐ¼ÓÈë̉»¶¨Á¿µÄYÈÜ̉ºÖÁ____________(̀îËáĐÔ¡¢¼îĐÔ»̣ÖĐĐÔ)¡£
XÈÜ̉ºÓëYÈÜ̉º·´Ó¦µÄÀë×Ó·½³̀ʽΪ___________________________£¬³£ÎÂÏ£¬ÎªÊ¹0.1 mol/L
M ÈÜ̉ºÖĐÓÉMµçÀëµÄ̉ơ¡¢ÑôÀë×ÓŨ¶ÈÏàµÈ£¬Ó¦Ị̈ÈÜ̉ºÖĐ¼ÓÈë̉»¶¨Á¿µÄYÈÜ̉ºÖÁ____________(̀îËáĐÔ¡¢¼îĐÔ»̣ÖĐĐÔ)¡£
1¡¢(15·Ö)ÓĐ»ú»¯ºÏÎïA¡¢B»¥ÎªÍ¬·Ö̉́¹¹̀壬BµÄ½á¹¹¼̣ʽÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
 A¾¢Ù¡¢¢ÚÁ½²½·´Ó¦µĂC¡¢DºÍE¡£B¾¢Ù¡¢¢ÚÁ½²½·´Ó¦µĂE¡¢FºÍH¡£ÉÏÊö·´Ó¦¹ư³̀¡¢²úÎïĐÔÖʼ°Ï໥¹ØϵÈçͼËùʾ¡£
A¾¢Ù¡¢¢ÚÁ½²½·´Ó¦µĂC¡¢DºÍE¡£B¾¢Ù¡¢¢ÚÁ½²½·´Ó¦µĂE¡¢FºÍH¡£ÉÏÊö·´Ó¦¹ư³̀¡¢²úÎïĐÔÖʼ°Ï໥¹ØϵÈçͼËùʾ¡£
(1)Đ´³öEµÄ½á¹¹¼̣ʽ¡¡_______
(2)Đ´³öCµÄÁ½ÖÖͬ·Ö̉́¹¹̀åµÄ½á¹¹¼̣ʽ¡¡_____________¡£
(3)GºÍAg(NH3)2OH·´Ó¦µÄ»¯Ñ§·½³̀ʽÊÇ¡¡______________£¬·´Ó¦ÀàĐÍÊÇ_____________¡£
(4)Đ´³öKºÍFÔÚŨH2SO4×÷ÓĂ·´Ó¦µÄ»¯Ñ§·½³̀ʽ£º___________¡£·´Ó¦ÀàĐÍÊÇ_____________¡£
(5)ÔÚD¡¢F¡¢H¡¢K»¯ºÏÎïÖĐ£¬»¥ÎªÍ¬ÏµÎïµÄÊÇ____________
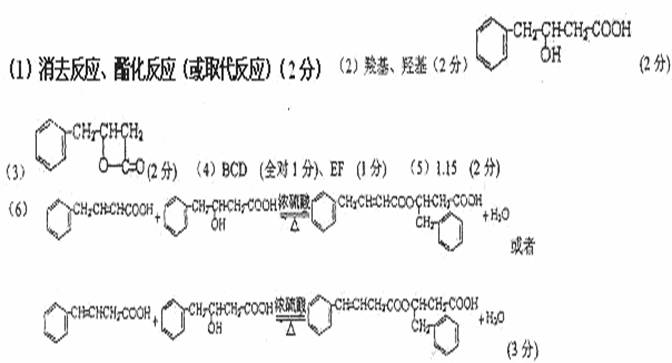
3.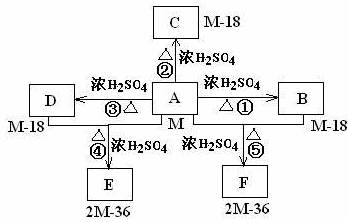 (15·Ö)̉ÑÖªÓĐ»úÎïA·Ö×ÓÖĐº¬Óб½»·Ç̉Ö»ÓĐ̉»¸ö²àÁ´£¬CÖĐ³ư±½»·Í⻹ÓĐ̉»¸öËÄÔª»·¡£ÓĐ»úÎïAµÄÏà¶Ô·Ö×ÓÖÊÁ¿M²»³¬¹ư200£¬ÆäÖĐÑơÔªËصÄÖÊÁ¿·ÖÊưΪ26.7%£¬ÍêȫȼÉƠÖ»Éú³ÉË®ºÍ¶₫Ñơ»¯̀¼¡£ÓëÖ®ÓĐ¹ØµÄÓĐ»úÎïת»¯¹ØϵÈçÏ£º(×¢̉⣺²¿·Ö·´Ó¦²úÎïÊ¡ÂÔ)
(15·Ö)̉ÑÖªÓĐ»úÎïA·Ö×ÓÖĐº¬Óб½»·Ç̉Ö»ÓĐ̉»¸ö²àÁ´£¬CÖĐ³ư±½»·Í⻹ÓĐ̉»¸öËÄÔª»·¡£ÓĐ»úÎïAµÄÏà¶Ô·Ö×ÓÖÊÁ¿M²»³¬¹ư200£¬ÆäÖĐÑơÔªËصÄÖÊÁ¿·ÖÊưΪ26.7%£¬ÍêȫȼÉƠÖ»Éú³ÉË®ºÍ¶₫Ñơ»¯̀¼¡£ÓëÖ®ÓĐ¹ØµÄÓĐ»úÎïת»¯¹ØϵÈçÏ£º(×¢̉⣺²¿·Ö·´Ó¦²úÎïÊ¡ÂÔ)
(1)¢Ù~¢ƯÖĐËùÉæ¼°µÄ·´Ó¦ÀàĐÍΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(2) ÓĐ»úÎïAÖĐº¬Ñơ¹ÙÄÜÍŵÄĂû³ÆΪ________________£¬AµÄ½á¹¹¼̣ʽΪ____________¡£
(3)ÓĐ»úÎïCµÄ½á¹¹¼̣ʽΪ____________________________
(4)ÓĐ»úÎïA-FÖĐ»¥ÎªÍ¬·Ö̉́¹¹̀åµÄÓĐ____________£¬______________(̀îĐ´×ÖĸA¡¢B¡¢¡¡)
(5)16.2gÓĐ»úÎïB¡¢C¡¢D×é³ÉµÄ»́ºÏÎïÍêȫȼÉƠ£¬ÏûºÄO2µÄÎïÖʵÄÁ¿Îª¡¡¡¡¡¡¡¡ mol(6)Đ´³öA+D¡úEµÄ»¯Ñ§·½³̀ʽ_____________________________¡£

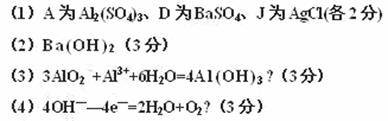
ѵÁ·Îå
2.(15·Ö)ÎïÖÊA~K¶¼ÊÇÓÉϱíÖĐÀë×ÓĐγɵģ¬Ç̉ΪÖĐѧ»¯Ñ§³£¼ûÎïÖÊ£¬ÓĐÈçͼËùʾµÄת»¯¹Øϵ¡£²¿·Ö²úÎïÖеÄË®̉ÑÊ¡ÂÔ¡£(Èç¹ûĐè̉ª̉ơ¡¢ÑôÀë×Ó¿É̉ÔÖظ´Ê¹ÓĂ)

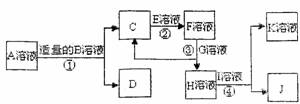
̉ÑÖªC¡¢D¡¢J¶¼ÊÇ°×É«³Áµí£¬ÆäÖĐD¡¢J²»ÈÜÓÚÏ¡ÏơËá¡£ÊÔ°´̉ªÇó»Ø´đÏÂÁĐÏà¹ØÎỀ⣺(1)A¡¢D¡¢JµÄ»¯Ñ§Ê½Îª£ºA¡¡¡¡¡¡¡¡ ¡¢D¡¡¡¡¡¡¡¡¡¡ ¡¢J¡¡¡¡¡¡¡¡¡¡¡¡ £»(2)Ïàͬ̀ơ¼₫Ï£¬ÎïÖʵÄÁ¿Å¨¶ÈÏàͬµÄBÈÜ̉ººÍEÈÜ̉ºpH½Ï´óµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (ÓĂ»¯Ñ§Ê½±íʾ)£»(3)Đ´³ö·´Ó¦¢ÛµÄÀë×Ó·½³̀ʽ£º¡¡¡¡
(4)ÓöèĐԵ缫µç½âIÈÜ̉ºÑô¼«µÄµç¼«·´Ó¦·½³̀ʽΪ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
1. (15·Ö)ij»¯Ñ§¿ÎÍâ»î¶¯Đ¡×éÉè¼ÆʵÑé̀½¾¿µªµÄ»¯ºÏÎïµÄĐÔÖÊ£¬×°ÖĂÈçÏÂͼËùʾ(A×°ÖĂδ»³ö)£¬ÆäÖĐAΪÆø̀å·¢Éú×°ÖĂ¡£AÖĐËùÓĂÊÔ¼Á´ÓÏÂÁĐ¹̀̀åÎïÖÊÖĐÑ¡È¡£ºa. NH4HCO3¡¢b. NH4Cl¡¢c. Ca(OH)2¡¢d. NaOH¡£
¼́²é×°ÖĂÆøĂÜĐÔºó£¬ÏȽ«C´¦²¬Ë¿Íø¼ÓÈÈÖÁº́ÈÈ£¬ÔÙ½«A´¦²úÉúµÄÆø̀åͨ¹ưB×°ÖĂƬ¿̀ºó£¬³·È¥C´¦¾Æ¾«µÆ¡£²¿·ÖʵÑéÏÖÏóÈçÏ£º²¬Ë¿¼̀Đø±£³Öº́ÈÈ£¬F´¦ÍƬÖđ½¥Èܽ⡣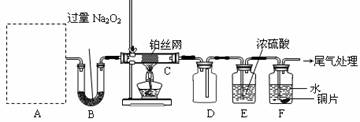
 (1)ʵÑéỂÖÆÈ¡AÖĐÆø̀åʱÈôÖ»ÓẲ»ÖÖÊÔ¼Á£¬¸ĂÊÔ¼ÁÊÇ________ (̀ѡÊÔ¼ÁµÄ×Öĸ)£»´ËʱAÖĐÖ÷̉ªµÄ²£Á§̉ÇÆ÷ÓĐ________________(̀îĂû³Æ)¡£ (2)AÖĐ²úÉúµÄÎïÖʱ»BÖĐNa2O2³ä·ÖÎüÊƠ£¬Đ´³öÈÎ̉ẩ»¸öBÖĐ·¢Éú·´Ó¦µÄ»¯Ñ§·½³̀ʽ£º_____________________(3)¶ÔÓÚCÖĐ·¢ÉúµÄ¿ÉÄæ·´Ó¦£¬ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ________¡£a. Ôö´ó̉»ÖÖ·´Ó¦ÎïµÄŨ¶È¿É̉Ồá¸ßÁí̉»ÖÖ·´Ó¦ÎïµÄת»¯ÂÊb. ¹¤̉µÉϽøĐи÷´Ó¦Ê±£¬¿É²ÉÈ¡¸ßѹµÄ̀ơ¼₫̀á¸ß·´Ó¦Îïת»¯ÂÊc. ¸Ă·´Ó¦ÔÚ̉»¶῭ơ¼₫Ï´ﵽƽºâʱ£¬·´Ó¦ÎïµÄƽºâŨ¶ÈÖ®±È̉»¶¨ÊÇ4¡Ă5
(1)ʵÑéỂÖÆÈ¡AÖĐÆø̀åʱÈôÖ»ÓẲ»ÖÖÊÔ¼Á£¬¸ĂÊÔ¼ÁÊÇ________ (̀ѡÊÔ¼ÁµÄ×Öĸ)£»´ËʱAÖĐÖ÷̉ªµÄ²£Á§̉ÇÆ÷ÓĐ________________(̀îĂû³Æ)¡£ (2)AÖĐ²úÉúµÄÎïÖʱ»BÖĐNa2O2³ä·ÖÎüÊƠ£¬Đ´³öÈÎ̉ẩ»¸öBÖĐ·¢Éú·´Ó¦µÄ»¯Ñ§·½³̀ʽ£º_____________________(3)¶ÔÓÚCÖĐ·¢ÉúµÄ¿ÉÄæ·´Ó¦£¬ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ________¡£a. Ôö´ó̉»ÖÖ·´Ó¦ÎïµÄŨ¶È¿É̉Ồá¸ßÁí̉»ÖÖ·´Ó¦ÎïµÄת»¯ÂÊb. ¹¤̉µÉϽøĐи÷´Ó¦Ê±£¬¿É²ÉÈ¡¸ßѹµÄ̀ơ¼₫̀á¸ß·´Ó¦Îïת»¯ÂÊc. ¸Ă·´Ó¦ÔÚ̉»¶῭ơ¼₫Ï´ﵽƽºâʱ£¬·´Ó¦ÎïµÄƽºâŨ¶ÈÖ®±È̉»¶¨ÊÇ4¡Ă5
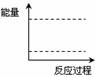
(4)ÇëÔÚÏÂͼ×ø±êÖĐ»³öC×°ÖĂÖĐ·´Ó¦·¢Éú¹ư³̀ÖеÄÄÜÁ¿±ä»¯Ê¾̉âͼ£¬²¢ÔÚĐéÏßÉÏ·Ö±đ±ê³ö·´Ó¦ÎïºÍÉú³ÉÎïµÄ»¯Ñ§Ê½¡£
(5)´ưʵÑé½áÊøºó£¬½«BÖĐ¹̀̀å»́ºÏÎïÈÜÓÚ500mL1mol¡¤L£1 ÑÎËáÖĐ£¬²úÉúÎ̃É«»́ºÏÆø̀å¼×£¬ÈÜ̉º³ÊÖĐĐÔ£¬ỘʵÑéÇ°BÖĐÔÓĐNa2O2µÄÎïÖʵÄÁ¿ÊÇ____mol,¼×ÔÚ±ê×¼×´¿öÏÂÊÇ_____L(ºöÂÔÆø̀åµÄÈܽâ)¡£
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com