
16. 刹车距离是衡量汽车安全性能的重要参数之一。图中所示的图
刹车距离是衡量汽车安全性能的重要参数之一。图中所示的图
线1、2分别为甲、乙两辆汽车在紧急刹车过程中的刹车距离s
与刹车前的车速v的关系曲线,已知紧急刹车过程中车与地面
间是滑动摩擦。据此可知,下列说法中正确的是 ( )
A.甲车的刹车距离随刹车前的车速v变化快,甲车的刹车性能好
B.乙车与地面间的动摩擦因数较大,乙车的刹车性能好
C.以相同的车速开始刹车,甲车先停下来,甲车的刹车性能好
D.甲车的刹车距离随刹车前的车速v变化快,甲车与地面间的动摩擦因数较大
15.如图,竖直环A半径为r,固定在木板B上,木板B放在水平地面上,B的左右两侧各有一档板固定在地上,B不能左右运动,在环的最低点静放有一小球C,A、B、C的质量均为m。给小球一水平向右的瞬时速度V,小球会在环内侧做圆周运动,为保证小球能通过环的最高点,且不会使环在竖直方向上跳起,瞬时速度必须满足 ( )
A.最小值
 B.最小值
B.最小值
C.最大值
D.最大值
14.用比值法定义物理量是物理学中一种重要的思想方法,下列物理量的表达式不属于用比值法定义的是 ( )
A.加速度 B.功率
B.功率
C.速度 D.加速度
D.加速度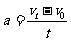
13. 维生素C(Vitamin
C,Ascorbic Acid)又叫L一抗坏血酸,是一
维生素C(Vitamin
C,Ascorbic Acid)又叫L一抗坏血酸,是一
种水溶性维生素。它是人体必需的一种维生素,人体若长期缺
乏维生素C,易患坏血病。已知维生素C具有酸性和较强的还
原性,加热或在溶液中易被氧化分解,在碱性条件下更易被氧
化,维生素C的结构简式如图所示。下列有关维生素C的说法
不正确的是 ( )
A.维生素C是一种羧酸,常温时其水溶液的pH<7
B.1 mol维生素C和足量钠反应最多可生成2 mol H2:
C.向KMnO4溶液中滴入维生素C溶液,可观察到溶液紫红色消失
D.一定条件下,维生素C既能和稀硫酸反应,又能和醋酸反应
12.设NA 代表阿伏加德罗常数的数值,下列说法中正确的是 ( )
①常温常压下,17g 甲基(-14CH3)所含的中子数为9NA
②常温常压22.4L NO气体的分子数小于NA
③ 64g的铜发生氧化还原反应,一定失去2NA个电子
④常温常压下,100mL 0.5 的乙酸溶液中,乙酸的分子数目小于0.05NA
的乙酸溶液中,乙酸的分子数目小于0.05NA
⑤标况时,22.4L二氯甲烷所含有的分子数为NA
⑥常温常压下,1 mol氦气含有的核外电子数为 4NAk-s-5+u
A.①② B.③④ C.②④ D.⑤⑥
11.下列说法正确的是 ( )
A.25℃时,pH为9的Na2CO3溶液和pH为5的NaHSO4溶液中,水的电离程度相同
B.在含有Al3+的KNO3溶液中,可通过加热的方法除去Al3+,证明盐的水解是吸热反应
C.已知HF的酸性比HCN的酸性强,则等体积等浓度NaF和NaCN两溶液中阳离子的物质的量之和相等
D.等物质的量浓度的 ① NH4Cl ② NH4HSO4 ③ Na2S ④ NaNO3 ⑤ (NH4)2SO4 ,
其pH由大到小的排列为③>④>⑤>①>②
10.下列有关实验装置及选项中的说法均正确的是 ( )
 A.实验目的:定量测定化学反应速率
A.实验目的:定量测定化学反应速率
B.实验原理:利用氧化还原反应原理,用酸性高锰酸钾溶液滴定亚硫酸钠溶液,测定亚硫酸钠溶液的浓度
C.实验过程中某步骤:将0.1mol/L50mLNaOH溶液逐滴加入到0.1mol/L55mL盐酸溶液中
D.加热烧杯,分离SiO2和NH4Cl的现象:烧杯底部有白色固体出现
9.现有M、N、P、E四种元素,有以下反应:(1)在水溶液中,M+N2+ M2++N
M2++N
(2)P+2H2O(l) P(OH)2+H2↑(3)N、E相连浸入稀H2SO4中,电极反应:N-2e
P(OH)2+H2↑(3)N、E相连浸入稀H2SO4中,电极反应:N-2e
 N2+,
N2+,
2H++2e
 H2↑,判断元素的还原性由强到弱的顺序是 ( )
H2↑,判断元素的还原性由强到弱的顺序是 ( )
A.M、N、P、E B.M、N、E、P
C.P、M、N、E D.E、P、M、N
8.X、Y、Z、W为短周期主族元素,原子序数依次增大,X的族序数是周期数的2倍,Y的气态氢化物与最高价氧化物水化物可形成盐,Z的最外层电子数与其电子总数比为3︰8,下列说法正确的是 ( )
A.X、Y、W的最高价含氧酸酸性顺序:Y>W>X
B.Z、W可形成ZW2的化合物,属于离子化合物
C.离子半径:Z>W>Y
D.气态氢化物的稳定性:Z>W
7.下列化学用语表示正确的是 ( )
A.硫酸氢钾加热熔融的电离方程式:KHSO4 = K+ + H+ + SO42-
B.氯化铵溶液显酸性的原因:NH4++ H2O = NH3•H2O + H+
C.铅蓄电池放电时阳极反应:Pb + SO42- - 2e-= PbSO4
D.氯化铁溶液中滴加少量的硫化钠溶液:2Fe3+ + S2- = 2Fe2+ + S↓
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com