
5. 表示平面,
表示平面, 为直线,下列命题中为真命题的是 ( )
为直线,下列命题中为真命题的是 ( )
A. B.
B.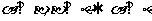
C. D.
D.
4.已知 ,则
,则 的值为 ( )
的值为 ( )
A.  B.
B.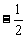 C.
C.  D.
D.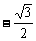
3.已知 为等差数列,且
为等差数列,且 ,则
,则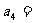 ( )
( )
A.5 B.7 C.9 D.11
2.以双曲线 的顶点为焦点,焦点为长轴的顶点的椭圆的准线方程为 ( )
的顶点为焦点,焦点为长轴的顶点的椭圆的准线方程为 ( )
A. B.
B.
C. D.
D.
1.已知集合 ,
, ,则
,则 是
是 的 ( )
的 ( )
A.充分但不必要条件 B.必要但不充分条件
C.充分且必要条件 D.既不充分也不必要条件
30、(16分)下列是芳香族化合物A、B、C、D、E的转化关系,其中A、E分子式分别是C9H8O和C9H8O2,E分子中除苯环外还含有一个六元环,且E中不含甲基。根据下列转化关系回答问题:

(1)写出A分子中所含官能团的名称____________。
(2)完成方程式,并写出反应类型:
A→B________________________,反应类型________________________。
B→C________________________,反应类型________________________。
(3)写出E的结构简式____________;写出由D反应生成高聚物的结构简式___________。
(4)D的同分异构体符合下列条件:①苯环有两个取代基;②取代基上无甲基;③能与FeCl3溶液发生显色反应;④能发生水解反应和银镜反应。
写出其中任意一种同分异构体的结构简式________________________。
29、(14分)某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
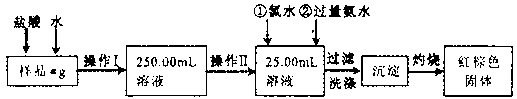
请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒、量筒外,还必须有____________ (填自选仪器名称),操作II必须用到的仪器是____________(填编号)。
A.50mL烧杯 B.50mL量筒
C.25mL碱式滴定管 D.25mL酸式滴定管
(2)洗涤是洗去附着在沉淀上的____________。(写离子符号)
(3)检验沉淀是否已经洗涤干净的操作是________________________。
(4)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是____________。
(5)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是____________。
(6)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的。他的理由是________________________。(用化学方程式表示)
28、 (15分)下列A-G均是中学常见化合物,它们之间有如图的转化关系(部分反应物或生成物略去),已知B为一种气体,E、F、G三种化合物中均含有同一种元素M,且价态互不相同。请回答下列问题。
(15分)下列A-G均是中学常见化合物,它们之间有如图的转化关系(部分反应物或生成物略去),已知B为一种气体,E、F、G三种化合物中均含有同一种元素M,且价态互不相同。请回答下列问题。
(1)M元素为____________。
(2)B是____________或____________,写出两种鉴别它们的方法____________;____________。
(3)若A与G反应也能制B,且反应中n(A)︰n(G)=1︰2,则此时该反应的离子方程式是________________________。
(4)若B与F在一定条件下反应生成一种化合物和一种单质,该反应的化学方程式为________________________。
27、(15分)X、Y、Z、W是原子序数依次增大的短周期元素,互不同族,其中只有两种为金属元素;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。Y和W的单质都能与NaOH溶液反应。请回答下列问题:
(1)X元素的名称是_______,Y、Z、W的原子半径由小到大的顺序是____________(用元素符号表示)。
(2)W元素在周期表中的位置是_________,Y元素的原子结构示意图是____________。
(3)Z和W在一定条件下能形成化合物ZW2,分子中各原子均达到了8电子稳定结构,则ZW2的电子式是____________;它在常温下呈液态,形成晶体时,属于____________晶体。
(4)X的单质与Y的单质化学性质相似,则X的单质与NaOH溶液反应的离子方程式是____________________(注:生成物中,含有X元素的化合物的化学式中含有2个氧原子)
(5)0.1mol W的单质与50 mL 1.5 mol¡L-1的FeBr2溶液反应,被氧化的Fe2+和Br-的物质的量之比是____________。
13、铜和镁的合金2.14g完全溶于一定浓度的硝酸,若反应中硝酸被还原为NO2、NO、N2O三种气体且标准状况下体积均为0.224L,在反应后的溶液中,加入足量的氢氧化钠溶液,生成的沉淀经过滤、洗涤、干燥后称量,质量为( )
A.3.12g B.4.18g
C.4.68g D.5.08g
第II卷(60分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com