
押题1. 有一矩形玻璃砖,现要测定它的折射率,给定的器材还有:白纸、铅笔、大头针1枚、直尺、直角三角板、量角器。实验时,先将直尺的一端O和另一点M标上两个明显的标记,然后将玻璃砖平放在白纸上,在白纸上沿其上下两个边缘画上两条直线,再将直尺紧贴玻璃砖的左边缘放置,使O点与直线CD相交,并在白纸上记下点M的位置,如图甲所示。然后,在某一适当位置P点
通过AB界面向左下方观察,发现点O和点M所呈的象恰
重合在同一点上,在P点插上大头针,调整它的位置,让
它刚好挡住这两者的象。
为了测得该玻璃砖的折射率,试在下边的横线上写出
重要的测量步骤,并画图说明。
。
[押题依据]插针法测定玻璃的折射率是课本中的一个基本学生实验,该部分实验的命题范围较窄,题目变化力度也不可能很大, 而就此题来说,却在原来实验模式的基础上大胆的跨了一步,即由四根针变成了一根针,并且将光的反射和折射知识巧妙的结合起来,不但具有可操作性,而且又使插针法焕然一新。此题考查了学生的推理能力、收集相关信息分析问题、处理问题的能力以及作图能力等。该题的原始模型来自于求水的折射率中的一个计算题。
 押题指数:8
押题指数:8
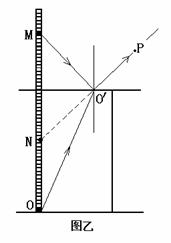
[解题指导]先通过直尺找出M点经界面AB所呈的反射像N,如图乙所示。连接N、P两点,交AB于O/点,而后画出入射光线OO/和MO/,再过O/点作一法线,得到入射角和折射角,用量角器测出两角,即可得到折射率。
得分锦囊:弄清题中所给的重合的两个像是解决该问题的突破口,这两个像一个为M点经AB界面的反射像,一个为O点的折射像。在处理这种类型的题目时,作图要规范,特别要注意标明光线的方向。
29.(14分)已知A、B、C、D四种短周期元素的原子序数依次增大,B的核电荷数是A、D核电荷数之和的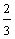 倍;A能分别与B、C、D形成电子总数相等的分子X、Y、Z。请回答下列问题:
倍;A能分别与B、C、D形成电子总数相等的分子X、Y、Z。请回答下列问题:
(1)B、D两元素的名称分别是 、 。
(2)化合物B2A2的电子式为 。
(3)Y与C的最高正价氧化物的水化物刚好完全反应时,其生成物的水溶液呈 性(填“酸”“碱”或“中”),其原因是(用离子方程式表示) 。
(4)在(3)所得生成物的水溶液中,存在着如下关系,用粒子浓度符号填写:
① c(H+)+ =c(OH-)+ ;
② c(H+)= c(OH-)+ 。
(5)用X、D2、NaOH溶液和惰性电极,可设计为一种燃料电池。则该燃料电池的
负极反应为 ;
正极反应为 。
27.(16分)

若从A出发可发生下图所示的一系列反应,其中B的分子式为C8H8O,且其苯环上的一氯取代物只有两种;G为高分子化合物。

请回答下列列问题:
(1)写出指定物质的结构简式:F ,M ,G ;
(2)指出反应①②的反应类型:① ,② 。
(3)写出B→C反应的化学方程式(有机物写结构简式):
。


⑤O==C-OH 五种物质中羟基上氢原子的活泼性顺序。在下表中填写实验现象及实验结论。
|
编号 |
实验操作 |
实验现象 |
实验结论 |
|
1 |
分别取上述五种物质的少量溶液或液体于试管中,各滴入几滴石蕊试液 |
|
|
|
2 |
分别取适量①、⑤的水溶液,各加入少量NaHCO3固体 |
|
|
|
3 |
分别取少量②、③、④,各加入适量NaOH溶液,再通入足量CO2 |
|
|
|
4 |
分别取少量②、③的液体,各加入一小粒金属钠 |
|
|
结论:上述五种物质中的羟基上氢原子活泼性顺序为 (填序号)。
26.(16分)回答有关乙烯的几个问题:
(1)下面是乙烯与酸性高锰酸钾溶液反应的离子方程式。请标出电子转移的方向和数目。
5C2H4+12MnO +36H+===10CO2+12Mn2++28H2O
+36H+===10CO2+12Mn2++28H2O
(2)配平乙烯与中性或弱碱性高锰酸钾溶液反应的离子方程式(将化学式或化学计量数填入下面相应的方框内)。

(3)乙烯和氢气组成的混合气体中碳氢两元素的质量比为12:5,则该混合气体中乙烯的体积分数为 。
(4)120℃、101kPa下,x L由乙烯和氢气组成的混合气体在y L O2中完全燃烧后,恢复到原温度和压强。若燃烧后气体体积缩小了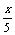 L,则x和y关系的数学表达式为 。
L,则x和y关系的数学表达式为 。
13.常温时,将V1mLc1mol·L-1的醋酸滴加到V2mLc2mol·L-1的烧碱溶液中,下列结论正确的是
A.若V1=V2,且混合溶液pH<7,则有c1<c2
B.若V1=V2,c1=c2,则混合溶液中c(Na+)=c(CH3COO-)
C.若混合溶液的pH=7,则有c1V1>c2V2
D.若混合溶液的pH=7,则混合溶液中c(Na+)>c(CH3COO-)
第II卷(60分)
12.一定条件下,向一容积可变的密闭容量中充入2molX,发生反应:
 2X(g)Y(g)+2Z(g),达到平衡后改变下述条件,气体Z的平衡平衡浓度不变的是
2X(g)Y(g)+2Z(g),达到平衡后改变下述条件,气体Z的平衡平衡浓度不变的是
A.恒温恒压下,充入1molX(g) B.恒温恒容下,充入1molY(g)
C.恒温恒压下,充入2molZ(g) D.恒温恒压下,充入1molHe(g)
11.下列叙述正确的是
A.甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色
 B.有机物CH3- -OH的消去产物有两种
B.有机物CH3- -OH的消去产物有两种
C.有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2=CH-COOCH3
D.可用溴水鉴别直馏汽油、四氯化碳和乙酸
10.已知:25℃、101kPa时,(1)12g石墨不完全燃烧生成CO,放出110.5kJ热量,CO继续燃烧又放出283.0kJ热量;(2)金刚石燃烧的热化学方程式为:
C(金刚石,s)+O2(g)==CO2(g);ΔH=-395.0kJ·mol-1。下列说法中正确的是
A.由石墨制备金刚石是放热反应
B.等质量时,金刚石所具有的能量比石墨所具有的能量低
C.CO燃烧的热化学方程式为:
2CO(g)+O2(g)===2CO2(g);ΔH=-283.0kJ·mol-1
D.石墨燃烧的热化学方程式为:
C(石墨,s)+O2(g)===CO2(g);ΔH=-393.5kJ·mol-1
8.下列离子方程式正确的是
A.向小苏打溶液中加入过理澄清石灰水:
 ===
===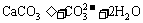
B.向苯酚钠溶液中通入少量的二氧化碳:

C.向溴化亚铁溶液通入过量氯气: ===
===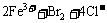
D.向氢氧化钡溶液中加入硫酸氢钠溶液至恰好完全沉淀:
 ===
===
 9.关于右图装置的叙述,正确的是
9.关于右图装置的叙述,正确的是
A.镁片为负极,镁片上产生黄绿色气体
B.铁片为阳极,铁片上产生无色气体
C.溶液中铁片与镁片之间产生白色沉淀
D.溶液的pH将逐渐增大
7.设NA为阿伏加德罗常数,下列说法正确的是
A.1mol 中含有电子数为9NA
中含有电子数为9NA
B.标准状况下,22.4LCO2和CO的混合气体中所含分子数小于NA
C.14gN2和CO的混合气体中所含原子数为NA
D.标准状况下,22.4L辛烷完全燃烧生成的二氧化碳分子数为8NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com