
2]新闻发言人说:SARS给全国人民带来了生活不便和健康威胁, 最紧要的任务是加大宣传力度和积极防治。
1]近一段时间,文坛上出现了一系列低级、庸俗的文学作品。一些具有社会道德良知的作家痛下 ,引发人们的思考。
2.依次填入下列各句横线处的词语,最恰当的一组是 ( )
1.下列词语中加粗的字,每对读音都不相同的一组是(3分) ( )
A.捡拾/拾级而上 隆重/安土重迁 稽首/滑稽可笑
B.脉搏/一脉相承 咀嚼/咬文嚼字 湖泊/鄱阳湖景
C.拜谒/殚精竭虑 纾难/别出机杼 募捐/蓦然同首
D.信笺/浅尝辄止 虎踞/前倨后恭 辱没/繁文缛节
10. 某实验小组用下列装置进行乙醇催化氧化的实验。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式 、 。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是___________反应。
(2)甲和乙两个水浴作用不相同。甲的作用是______________;乙的作用是_______________。
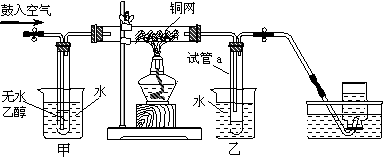
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是________________________。集气瓶中收集到的气体的主要成分是_________________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有__________________。要除去该物质,可现在混合液中加入__________(填写字母)
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过______________(填试验操作名称)即可除去。

9.某研究性学习小组在做Na2O2与水反应实验时,发现Na2O2与水反应后的溶液中滴加酚酞试液溶液呈现红色,但红色很快褪色,甲、乙、丙三同学对此现象分别做了如下推测:
甲:因为反应后试管很热,所以可能是溶液温度较高使红色褪去。
乙:因为所加水的量较少,红色褪去可能是生成的NaOH溶液浓度较大的影响。
丙:Na2O2具有强氧化性,生成物中O2、H2O2(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质。
 (1)验证甲同学的推测是否正确的方法是
,验证乙同学的推测是否正确的方法是
;当出现
现象时,即可说明丙同学的推测正确。
(1)验证甲同学的推测是否正确的方法是
,验证乙同学的推测是否正确的方法是
;当出现
现象时,即可说明丙同学的推测正确。
(2)有同学提出用定量的方法探究丙同学方案中是否含有H2O2,其实验方法为:称取2.6gNa2O2固体,使之与足量的水反应,测量产生O2的体积,与理论值比较,即可得出结论。
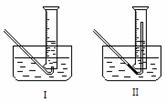
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用右图装置中的 ,理由是 。
②若在标准状况下测量气体的体积,应选用的量筒的大小规格为 (选填“100mL”、“200mL”、“500mL”)。
解析:甲的观点为温度较高就会使酚酞褪色,可以待冷却后再加酚酞试液或冷却后再看溶液是否变红;乙同学的观点是NaOH浓度过大,加水稀释即看进行验证;若欲证明丙同学观点正确,则需否定甲和乙的观点,可以冷却后观察溶液是否变红及加水稀释后溶液是否变红来验证。比较两个装置可以看出II可以防止气体冷却时出现倒吸现象,根据计算可知2.6gNa2O2全部转化为O2,其体积在标准状况下约375mL,故应选用500mL.
答案:(1)冷却后加酚酞试液或冷却后看溶液是否变红 加水稀释后看溶液是否变红 冷却后及加水稀释后均不变红
(2)①Ⅱ 防止气体冷却时发生倒现象,减小实验误差。 ②500mL
8、“旺旺雪饼”袋内有一个小纸袋,上面写着“干燥剂,主要成分是生石灰”。为此我对干燥剂的有关问题进行相关探究:
(1)问题1:为什么生石灰(CaO)可作干燥剂?(用化学方程式表示)  。
。
(2)我又对它作了一系列探究,获得较多收益,其有关实验方案如下:
|
问题与猜想 |
实验步骤 |
实验现象 |
实验结论 |
|
问题2:小纸袋中的物质能否继续作干燥剂? |
取足量小纸袋中固体放入烧杯中,加入适量水,触摸杯壁。 |
|
不能作干燥剂 |
|
问题3:我猜想变质后的物质可能是碳酸钙,该如何验证我的猜想? |
|
|
该干燥剂样品中有碳酸钙 |
(3)问题4:样品中碳酸钙的含量如何?某同学按如下流程进行实验:用盐酸溶解该干燥剂样品→干燥所得气体→用NaOH溶液吸收气体→根据NaOH溶液的增重计算该样品的含量,实验过程中所取该干燥剂样品的质量为10.0g。实验装置如图所示:

①A为溶解该干燥剂样品的装置,若已准备了长颈漏斗、双孔橡胶塞、导气管,为完成溶解至少还需要的实验仪器是 。
②A中发生反应的化学方程式为
③将插入溶液C中管子的下端改成具有多孔的球泡(如图中的D),有利于提高实验的准确度,其理由是 。
④当改进实验装置并进行正确操作后可以准确测定出干燥剂样品的含量(假设生成气体没有损失,并完全吸收)。若此时C装置在实验前后其质量增加了3.6g,则该干燥剂样品的CaCO3含量为 。
解析:作干燥剂要能吸收其中的水蒸气,故反应为CaO+H2O=Ca(OH)2;因为CaO溶于水会放出大量的热,根据结论不能再作干燥剂,所以现象为杯壁不发烫;如果是CaCO3,则可以加盐酸看是否有气泡产生即可。从所给的仪器看缺少盛放样品的容器,可选用锥形瓶等,A中的反应为Ca CO3+2HCl=CaCl2+CO2↑+H2O,多孔的球泡有利于CO2的吸收,C装置增重是吸收了CO2,即CO2为0.82mol,相当于CaCO3为8.2g,含量为82%。
CO3+2HCl=CaCl2+CO2↑+H2O,多孔的球泡有利于CO2的吸收,C装置增重是吸收了CO2,即CO2为0.82mol,相当于CaCO3为8.2g,含量为82%。
答案:(1)CaO+H2O=Ca(OH)2
(2)问题2的实验现象为:不发烫
问题3的实验步骤为:取该固体,滴加稀盐酸;实验现象为:有气泡产生
(3)①锥形瓶或广口瓶;②CaCO3+2HCl=CaCl2+CO2↑+H2O;③增大气体和溶液的接触面积,有利于二氧化碳的吸收;④82%。
7.实验室用下列装置所示的流程进行气体性质实验。图中用箭头表示气体的流向,A为一种纯净、干燥的气体,B是另一种气体,己中有红棕色气体出现。实验中所用的药品只能从下列物质中选取:Na2CO3、NaHCO3、Na2O、Na2O2、NaCl、无水CaCl2、(NH4)2CO3、碱石灰等固体和蒸馏水。
根据图中装置和现象回答:
(1)丙中发生反应的化学方程式为 。
(2)丁中应选用的干燥剂是___ __,为什么不选用所给的另一种干燥剂__ __。
(3)甲中发生反应的化学方程式_________________ ____。
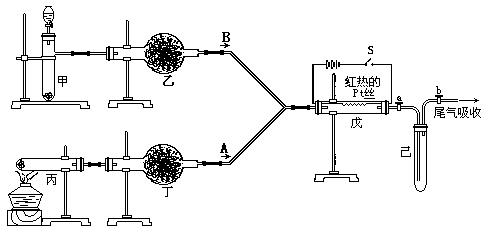
(4)戊中发生的主要反应的化学方程式 _。此反应是吸热反应还是放热反应__ __,估计可看到什么现象足以说明你的判断 。
解析:根据己中有红棕色气体产生,是在红热铂丝催化下有A、B两种气体生成的,根据所学知识可知,在戊中发生的反应为4NH3+5O2  4NO+6H2O,A、B为NH3和O2,根据所给药品知道,丙中制备的是NH3,其反应为(NH4)2CO3
4NO+6H2O,A、B为NH3和O2,根据所给药品知道,丙中制备的是NH3,其反应为(NH4)2CO3 2NH3↑+CO2↑+H2O,甲中制
2NH3↑+CO2↑+H2O,甲中制 备是是O2,其反应为2Na2O2+2H2O
= 4NaOH+O2↑。丁中的干燥剂是碱石灰,用来干燥氨气,同时除去CO2,而无水氯化钙再不能吸收CO2。
备是是O2,其反应为2Na2O2+2H2O
= 4NaOH+O2↑。丁中的干燥剂是碱石灰,用来干燥氨气,同时除去CO2,而无水氯化钙再不能吸收CO2。
答案:(1)(NH4)2CO3 2NH3↑+CO2↑+H2O
2NH3↑+CO2↑+H2O
(2)碱石灰 因为另一种干燥剂的无水CaCl2,只能吸收水,不能吸收CO2,不能使氨气完全净化。
(3)2Na2O2+2H2O = 4NaOH+O2↑
(4)4NH3+5O2  4NO+6H2O 放热 可以看到戊中铂丝比开始反应时更加红热
4NO+6H2O 放热 可以看到戊中铂丝比开始反应时更加红热
6. A、B、C、D、E五种有机物,它们的分子分别由-CH3、-OH、-COOH、-C6H5、
A、B、C、D、E五种有机物,它们的分子分别由-CH3、-OH、-COOH、-C6H5、
-CHO中的两种组成,这些化合物的性质如下所述:
(1)A能够发生银镜反应,且相对分子质量为44;
(2)B溶液加入氯化铁溶液中,溶液显紫色;
(3)C和E在有浓硫酸存在并加热的条件下,能发生酯化反应,C和E的相对分子质量之比为8:15;
(4)B和E都能跟氢氧化钠溶液反应,而A、C、D则不能;
(5)D能使酸性高锰酸钾溶液褪色,还能发生硝化反应。
由此可知,
C、D、E的结构简式是: C
D  E
。
E
。
解析:A能发生银镜反应,则A含有醛基(-CHO),又其相对分子质量为44,故A为CH3CHO,B溶液加入氯化铁溶液显紫色,故B为苯酚;C和E能发生酯化反应,为醇和酸,根据题意可知,C为CH3OH,E为CH3COOH;D能使酸性高锰酸钾溶液褪色,且能发生硝化反应,故D为甲苯。
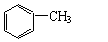 答案:CH3OH,
,CH3COOH
答案:CH3OH,
,CH3COOH
5.已知氢氧化镁是难溶于水,在氨水中的溶解度也很小。某兴趣小组在实验中将氢氧化镁固体放入NH4Cl溶液中,不断搅拌,发现氢氧化镁固体溶解了。针对这一现象,同学展开了讨论,甲同学认为:Mg(OH)2在水中存在如下溶解平衡:Mg(OH)2(S)
 Mg2+ + 2OH- , 而氯化铵水解呈酸性,其水解产生的H+与Mg(OH)2 电离出来的OH-结合生成难电离的水,从而促进了氢氧化镁的溶解平衡右移。为了检验甲同学的观点是否正确,乙同学进行了下列实验验证,用CH3COONH4(其溶液显中性)代替NH4Cl进行上述实验,发现氢氧化镁固体也溶解了,从而否定了甲同学的观点,请你说明乙同学否定甲同学观点的理由,并说明你对氢氧化镁固体能溶于氯化铵溶液的解释:
。
Mg2+ + 2OH- , 而氯化铵水解呈酸性,其水解产生的H+与Mg(OH)2 电离出来的OH-结合生成难电离的水,从而促进了氢氧化镁的溶解平衡右移。为了检验甲同学的观点是否正确,乙同学进行了下列实验验证,用CH3COONH4(其溶液显中性)代替NH4Cl进行上述实验,发现氢氧化镁固体也溶解了,从而否定了甲同学的观点,请你说明乙同学否定甲同学观点的理由,并说明你对氢氧化镁固体能溶于氯化铵溶液的解释:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com