
2.生活中发生的下列变化,属于物理变化的是
A.煤气燃烧 B.冰块融化 C.菜刀生锈 D.牛奶变酸
1.下列所示的物质中,属于纯净物的是
A.黄酒 B.矿泉水 C.24K黄金 D.钢
28.(16分)2007年度诺贝尔化学奖获得者格哈德·埃特尔建立了合成氨反应机理,T=673K时,各步反应的能量变化如图所示,图中的能量单位为kJ·mol-1。(注:图中“吸”表示在催化剂表面的吸附)请回答下列问题:
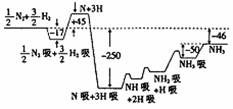 (1)合成氨反应的机理为
(1)合成氨反应的机理为
① ;


 ②N: N2吸
2N
2N吸
②N: N2吸
2N
2N吸
③ ;
 ④NH吸+H吸
NH2吸;
④NH吸+H吸
NH2吸;

 ⑤NH2吸+H吸
NH3吸 NH3。
⑤NH2吸+H吸
NH3吸 NH3。
(2)T=673K时,合成氨反应的热化学方程为 。
(3)液氨与水颇为相像,它能溶解多种无机及有机分子,其电离方程式可表示为:
 2NH3 NH+4+NH-2(某温度下其离子积常数为10-20)。液氨中的pNH4与水中的pH类似,则该温度下液氨的pNH4=
。
2NH3 NH+4+NH-2(某温度下其离子积常数为10-20)。液氨中的pNH4与水中的pH类似,则该温度下液氨的pNH4=
。
(4)盐酸肼(N2H4Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出盐酸肼第一步水解反应的离子方程式 。
25.(15分)A、B、C、D、E、F是周期表前30号元素中的六种元素,它们的原子序数依次增大,三种为金属元素、三种为非金属元素。常温下,A、E两种元素所形成的常见单质为气体,B、C、D、F四种元素所形成的常见单质为固体,实验室通常将B单质保存在煤油中,单质B与单质A因反应条件不同生成两种不同的化合物甲和乙。C和E元素的原子均只有一个未成对P电子。D和F两元素形成的某种化合物是硫酸工业的常用原料。
回答下列问题:
(1)F元素在周期表中的位置为 ,F原子基态时核外电子排布式 。
(2)甲、乙均能与水反应,但甲与水发生的反应属于氧化还原反应,写出甲的电子式 ,写出甲与水发生反应的化学方程式并标出电子转移的方向和数目: 。
(3)F的一种红褐色氢氧化物与E的单质、B的最高价氧化物对应的水化物三种物质作用可生成一种净水剂B2FA4,试写出该反应的化学反应方程式为:
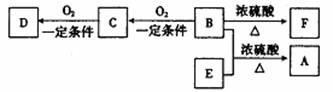 26.(13分)有些香皂、洗发香波中往往有兰花香味,这是其中添加了化学式为C10H20O2的一种香料A,下列框图列出了生成该物质的原料及一系列反应,已知:D、E都能使石蕊变红,分子式相同,经分析E中有10个H原子,且只有两种不同的H原子。C无支链,既有氧化性又有还原性,F与B碳原子数相等。
26.(13分)有些香皂、洗发香波中往往有兰花香味,这是其中添加了化学式为C10H20O2的一种香料A,下列框图列出了生成该物质的原料及一系列反应,已知:D、E都能使石蕊变红,分子式相同,经分析E中有10个H原子,且只有两种不同的H原子。C无支链,既有氧化性又有还原性,F与B碳原子数相等。
结合框图和提示回答有关问题:
(1)F可以发生的反应有 (选填序号)。
①加成反应 ②消去反应 ③加聚反应 ④氧化反应 ⑤还原反应
(2)E在甲基上的氢若被氧取代,其一氧代物有 种。将该一氧化物在NaOH溶液中加热,写出该反应的方程式: 。
(3)B、E、F分子所含的官能团的名称依次是 、 、 。设计实验检验C中的官能团 。
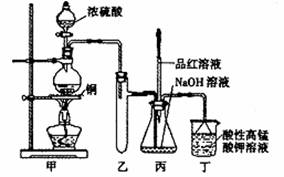 27.(14分)实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如下图所示:
27.(14分)实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如下图所示:
请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,有人认为还有一定量的H2SO4剩余,原因是
,在不增加浓H2SO4的前提下,若使剩余铜片溶解可再加入 (填写两种属于不同类别的物质)。
(2)向反应后的溶液中加入足量的CuO,使剩余的H2SO4全部转化为CuSO4,过滤后将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4·XH2O)某小组同学采用加热法测定该晶体里结晶水X的值;
①在他们的实验操作中至少称量 次。
②下面是其中一次实验的数据
|
坩埚质量 |
坩埚与晶体总质量 |
加热后坩埚与固体总质量 |
|
11.7g |
22.7g |
18.6g |
根据上表数据计算判断x的实测值比理论值(x=5) (填“偏大”或“偏小”)。
(3)装置乙的作用是: ;
(4)下列说法正确的是: (填序号)。
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.KMnO4溶液用于尾气处理
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3
f.此装置换上其它药品后,不能制取和收集少量纯净的氯气
13.下列各溶液中微粒的物质的量浓度关系错误的是 ( )
A.0.2mol/L K2CO3溶液中c(OH-)=c(HCO-3)+c(H+)+2c(H2CO3)
B.0.1mol/L NaHA溶液中其中pH=3,c(HA-)>c(H+)>c(H2A)>c(A2-)
C.向Na2SO4溶液中滴加稀HNO2得到pH=4的混合溶液c(Na+)=2c(SO2-4)
D.pH=a的HA溶液与pH=b的MOH溶液任意比混合c(H+)+c(M+)=c(OH-)+c(A-)
第Ⅱ卷(非选择题,共180分)
请用0.5毫米黑色墨水签字笔在答题卡上作答,在试卷上答题无效。
10.在中学化学实验中可用于分离或提纯的方法很多,如蒸馏、过滤、结晶、渗析、盐析等,下列各组混合物的分离或提纯选用方法最合适的是 ( )
A.除去Fe(OH)3胶体中混有的Cl---(过滤、洗涤、干燥)
B.除去O2中的N2--(通过灼热的Cu网)
C.分离NaNO3和BaSO4的混合物--(溶解、过滤)
D.从皂化反应后的混合物中分离出高级脂肪酸盐--(加入NaCl、渗析)
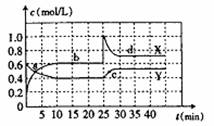 11.在恒温条件下,将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,测得各物质的浓度随时间变化关系如下图所示
11.在恒温条件下,将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,测得各物质的浓度随时间变化关系如下图所示
下列说法正确的是 ( )
A.图中的两条曲线中,Y是表示NO2浓度随时间的变化曲线
B.前10min内,用v(NO2)表示的化学反应速率为0.06mol/(L·min)
C.在25min时,反应改变的条件是增大了NO2的浓度
D.a、b、c、d四个点中,有a、b、d点的化学反应处于平衡状态
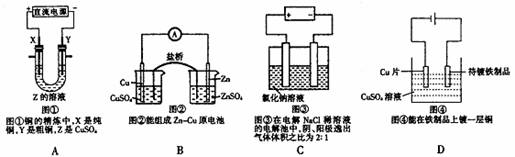 12.下列关于图像及描述说法都正确的是 ( )
12.下列关于图像及描述说法都正确的是 ( )
9.某无色透明的强酸性溶液中,能大量共存的一组离子是 ( )
A.NH+4、Na+、Cl-、SO2-3 B.Mg2+、Al3+、SO2-4、NO-3
C.Na+、K+、SO2-4、AlO-2 D.K+、NH+4、MnO-4、Cl-
7.下列物质能与水发生氧化还原反应的是 ( )
A.NH3 B.N2 C.Na D.KNO3

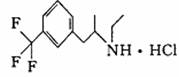 8.Br-CH2-CH2-CH(CH2)-CH2-Br可用
表示。盐酸芬氟拉明(分子结构如右图)是目前国内上市的减肥药主要化学成分,因临床使用患者出现严重不良反应。国家食品药品监督管理局发出通知,停止盐酸芬氟拉明的生产、销售和使用,并撤销该药品的批准文号。下列关于盐酸芬氟拉明的说法错误的是 ( )
8.Br-CH2-CH2-CH(CH2)-CH2-Br可用
表示。盐酸芬氟拉明(分子结构如右图)是目前国内上市的减肥药主要化学成分,因临床使用患者出现严重不良反应。国家食品药品监督管理局发出通知,停止盐酸芬氟拉明的生产、销售和使用,并撤销该药品的批准文号。下列关于盐酸芬氟拉明的说法错误的是 ( )
A.属于芳香族化合物
B.该物质可发生加成反应
C.苯环上的一氧取代有4种
D.分子中所有碳原子和氧原子可能在同一平面内
3.第I卷共20小题,每小题6分,共120分。第II卷共11题,共180分。
第I卷(选择题 共120分)
本卷共20小题,每小题6分,共120分。在每小题给出的四个选项中,只有一项是符合题目要求的。
以下数据可供解题时参考:
相对原子质量(原子量):H 1 C 12 N 14 O 16 S 32 Fe 56 Cu 64
2.答题前,请考生务必将答题卷左侧密封线内的项目填写清楚。请考生按规定用笔将所有试题的答案涂、写在答题卷上,在试题卷上作答无效。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com