
30. (12分) 果蝇是一种小型蝇类,因其具有易饲养,培养周期短,染色体数目只有8条,相对性状易区分等特点,所以是遗传学中常见的试验材料。结合所学遗传变异的知识回答下列问题:
(1) 果蝇的体细胞内有 个染色体组。其单倍体基因组有 条染色体。
(2)
 已知猩红眼和亮红眼为控制果蝇眼色的一对相对性状,由等
已知猩红眼和亮红眼为控制果蝇眼色的一对相对性状,由等 位基因A、a控制,圆形眼和棒状眼为控制
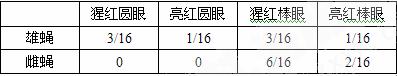
位基因A、a控制,圆形眼和棒状眼为控制 果蝇眼形的另一对相对性状,由等位基因B、b控制。现有一对猩红棒状眼的雌雄果蝇交配,得到F1表现型及比例如下表:
果蝇眼形的另一对相对性状,由等位基因B、b控制。现有一对猩红棒状眼的雌雄果蝇交配,得到F1表现型及比例如下表:
则可以得知这两对相对性状的显性性状分别是_____________________________;控制眼色和眼形的基因分别位于 染色体上;F1中亮红圆眼果蝇的基因型为 ;如果让F1中表现型为猩 红棒眼的雌雄果蝇自由交配得到F2,
红棒眼的雌雄果蝇自由交配得到F2,
那么F2中亮红圆眼果蝇的概率是_________________。
29. 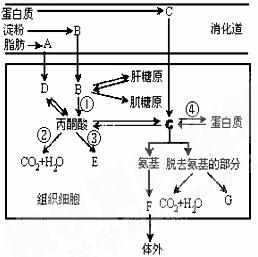 (30分) I.下图表示人体内糖类,脂肪和蛋白质部分代谢途径,图中A、B、C、D、E、F、G表示物质,①、②、③、④表示过程.
(30分) I.下图表示人体内糖类,脂肪和蛋白质部分代谢途径,图中A、B、C、D、E、F、G表示物质,①、②、③、④表示过程.
(1) 图中淀粉转变为B需要的酶有____,消化道上皮细胞吸收B物质的过程需要_________等条件,物质B从小肠肠腔中被小肠上皮细胞吸收,到进入肌肉细胞,至少需要经过_______层生物膜。
(2) 在过程①、②、③、④中,释放能量最多的是_______________,需要消耗能量的是______________。
(3) 人体处在__________________________条件时,会合成肝糖原和肌糖原。
Ⅱ.内环境的稳态是人体健康的重要保证,人体的免疫功能和 激素调节对于维持内环境稳态有着重大意义。
激素调节对于维持内环境稳态有着重大意义。
(1) 免疫是机体的一种重要的自我保护机能,以下是与人体体液免疫有关的一些细胞:
①造血干细胞 ②吞噬细胞 ③B淋巴细胞 ④效应B细胞 ⑤记忆细胞。
A.以上细胞中有分化能力的细胞有 。(填序号)
B.抗原再次进入人体,能被上述细胞中的 识别。(填序号)
C.既参与 特异性免疫又参与非特异性免疫的细胞是 。(填序号)
D.效应T细胞与体液免疫也有关系,因为其产生的 可以增强B细胞等免疫细胞的作用。
(2) 为研究促甲状腺激素(TSH)分泌的影响因素,研究者从刚宰杀的大白鼠体内分离新鲜的下丘脑和脑垂体,然后把这些结构单独或一起培养于含有或不含有甲状腺激素的培养基中,培养后测定培养基内TSH的浓度,结果如下:
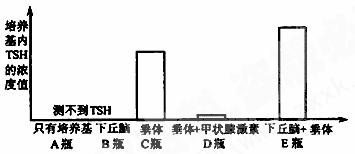
①在上述实验中设置A瓶的目的是什么? __________________________
②将以上装置中的实验结果进行相互比较,可以得出哪些结论?
A____________________________________________________________
B____________________________________________________________
C____________________________________________________________
D____________________________________________________________
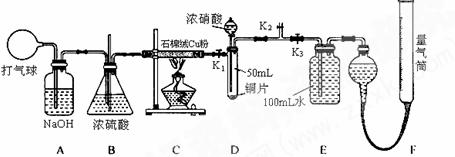
28. (14分) 某化学兴趣小组欲验证:“铜和一定量的浓硝酸反应有一氧化氮产生”。设计使用了如下装置进行实验。(假设气体体积均为标准状况,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)
试回答下列问题:
(1)
将铜粉分散在石棉绒中的原因是_________ __________________________。
__________________________。
(2)
在铜和浓硝酸反应前,挤压打气球,经A、B、C反应后,进入D中的气体主要成分是________ _(填化学式),通入该气体的目的是_________________________________;进行此步操作时应关闭_________,打开_________ (填K1、K2或K3)。
_(填化学式),通入该气体的目的是_________________________________;进行此步操作时应关闭_________,打开_________ (填K1、K2或K3)。
(3) 关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。则D中一定发生反应的离子方程式为:_______________________________________________________________________。
(4) 若E中出现倒吸,可采取的应急操作是_________________________________。
(5) I.从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000 mol·L-1的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则E容器中所得硝酸的物质的量浓度为__________________ mol·L-1。
Ⅱ.若实验测得F装置所收集到的气体体积为139.00 mL,则铜和一定量的浓硝酸反应____ _______(填“有”或“无”)NO生成,其依据是(请用数据和文字说明)__________________________________________________________________________________________________________________________________________________________________________________________________________________________。
_______(填“有”或“无”)NO生成,其依据是(请用数据和文字说明)__________________________________________________________________________________________________________________________________________________________________________________________________________________________。
27. (15分) 已知①-④均为工业生产及应用的常见反应。其中常温下B、D、J、P气体,E为分子中原子个数比为1∶l的液体。A的相对分子质量为120。(个别反应的产物已略去)
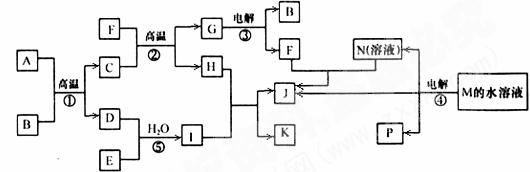
试回答下列问题:
(1) 反应F与N溶液反应的离子方程式为________________________________________;
(2)
 反应⑤中当有1mol电子转移时,氧化剂消耗
g。
反应⑤中当有1mol电子转移时,氧化剂消耗
g。
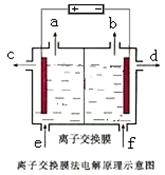
(3) 反应④的离子方程式为______________________________;
右图是该反应原理的示意图,该装置中使用的是 (填“阴”或“阳”)离子交换膜。图中从d处收集到的是 。
(4)
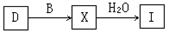 工业上由D制取I的过程可表示为:
工业上由D制取I的过程可表示为:
由D与B反应生成X的反应所用的设备是
①高炉 ②沸腾炉 ③接触室 ④分馏塔 ⑤吸收塔
已知400℃ 101Kpa时,2D(g)
+ B(g) 2X(g);△H = – 196.6KJ/mol,当2 mol D与1 mol B在该条件下反应达平衡时反应放热186.8 KJ。
2X(g);△H = – 196.6KJ/mol,当2 mol D与1 mol B在该条件下反应达平衡时反应放热186.8 KJ。
在实际生产中综合考虑各种因素,为提高D的转化率,工业选择了以下哪些条件______
①适当升高温度 ②增大压强 ③使用合适的催化剂 ④及时移走生成物 ⑤适当增大B的浓度 ⑥将反应物与生成物在热交换器中进行热交换
26. (共15分) 请根据下图作答:
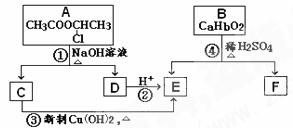
已知:一个碳原子上连有两个羟基时,易发生下列转化:
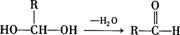
(1) 反应①所属的有机反应类型是_______________反应。
(2) 反应③的化学方程式______________________________________________________。
(3) 已知B的相对分子质量为162,其完全燃烧的产物中n(CO2)∶n (H2O) = 2∶1,则B的分子式为 。
(4) F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
(5) 化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G的结构有 种。
(6)
化合物H是B的同分异构体,H分子中含有的部分结构为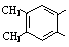 ,它的水解产物经聚合反应后可得到高聚物(CaHbO2)n.。H有多种结构,写出其中一种的结构简式
。
,它的水解产物经聚合反应后可得到高聚物(CaHbO2)n.。H有多种结构,写出其中一种的结构简式
。
25. (16分) A、B、C、D、E、F属于短周期主族元素。A的原子半径在短周期中最大,B的一种原子中,质量数与质子数之差为零, C与D、E与F均同主族,C元素的原子L层电子数是K层的2倍,E原子的核外电子总数等于C、D原子核外电子总数的差。
(1) 离子B-的结构示意图为 ;化合物CE2的分子属于 分子(填“极性”或“非极性”);用电子式表示化合物A2F的形成过程 。
(2) A、E、F形成的简单离子的半径由大到小的顺序为 (用离子符号表示);
元素C、D、E形成的常见单质中,熔沸点由高到低的顺序是(用名称表示)
(3) 由B、C可以构成的最简单的化合物W,取16.0g分子式为W·8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
(4) 使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一。有人设计制造了一种燃料电
池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3。该电池的负极反应式为 ,电池工作时,电解质里的CO32-向 极移动。
24. 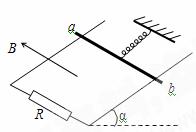 (19分) 如图所示,光滑的金属导轨间距为L,导轨平面与水平面成α角,导轨下端接有阻值为R的电阻,质量为m的金属细杆ab与绝缘轻质弹簧相连静止在导轨上,弹簧劲度系数为k,上端固定,弹簧与导轨平面平行,整个装置处在垂直于导轨平面斜向上的匀强磁场中,磁感应强度为B.现给杆一沿轨道向下的初速度v0,杆向下运动至速度为零后,再沿轨道平面向上运动达最大速度,大小为v1,然后减速为零,再沿轨道平面向下运动……一直往复运动到静止(导轨与金属杆的电阻忽略不计).试求:
(19分) 如图所示,光滑的金属导轨间距为L,导轨平面与水平面成α角,导轨下端接有阻值为R的电阻,质量为m的金属细杆ab与绝缘轻质弹簧相连静止在导轨上,弹簧劲度系数为k,上端固定,弹簧与导轨平面平行,整个装置处在垂直于导轨平面斜向上的匀强磁场中,磁感应强度为B.现给杆一沿轨道向下的初速度v0,杆向下运动至速度为零后,再沿轨道平面向上运动达最大速度,大小为v1,然后减速为零,再沿轨道平面向下运动……一直往复运动到静止(导轨与金属杆的电阻忽略不计).试求:
(1) 细杆获得初速度瞬间,通过R的电流大小;
(2) 当杆速度为v1时离最初静止时位置的距离L1;
(3) 杆由初速度v0开始运动直到最后静止,电阻R上产生的焦耳热Q.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com