
30.(15分)已知: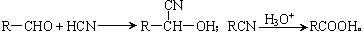
某企业合成高效、低毒农药杀灭菊酯的路线如下:

(1)写出下列物质的结构简式:
C______________;D______________;E______________;F______________。
(2)从甲苯到D的四步反应中有________步是取代反应。
(3)农药杀灭菊酯的分子式为__________________。
(4)写出E→F的化学方程式____________________________________。
29. (15分)A、B、C、W、X、Y、Z是由周期表中短周期元素组成的七种物质,其中A、B、C是三种固体单质,W、X、Y、Z是由两种元素组成的化合物。它们之间的转化关系如图所示(所有反应物和生成物均未在框图中:
(15分)A、B、C、W、X、Y、Z是由周期表中短周期元素组成的七种物质,其中A、B、C是三种固体单质,W、X、Y、Z是由两种元素组成的化合物。它们之间的转化关系如图所示(所有反应物和生成物均未在框图中:
回答下列问题:
(1)化合物Z的晶体类型属于__________晶体。
(2)写出单质C的一种用途__________________________________。
(3)航天科技测知化合物N是金星大气层的成分之一,组成化合物N的元素与W相同。已知N中两种元素的质量之比为2:1,N的相对原子质量小于80,则N的化学式为_____________。又知该分子中的每个原子都满足最外层8电子的稳定结构,试写出其电子式_________________。
(4)写出下列反应的化学方程式:
①_______________________________;②_______________________________。
28.(15分)已知硝酸铜溶液呈蓝色。但在铜与浓硝酸、稀硝酸反应的实验中,同学们发现,除了生成的气体颜色不相同外,最终溶液的颜色也不相同:前者呈绿色,而后者呈蓝色。甲、乙二位同学为此进行了实验探究。
甲:在I、II两支试管中分别加入等体积的浓HNO3和稀HNO3,再向两支试管中分别投入等质量的铜片,充分反应后铜均无剩余。结果:I中溶液呈绿色,II中溶液呈蓝色。
乙:分别取I中的绿色溶液于两支试管Ⅲ、IV中,对试管Ⅲ进行多次振荡、静置,最终溶液颜色由绿色转变为深蓝色;向试管IV中缓缓加水并不停振荡,观察到溶液由绿色变为深蓝色,最后变为淡蓝色。
请回答下列问题:
(1)分别写出Cu与浓HNO3、稀HNO3反应的化学方程式:_______、________。
(2)甲的实验_______(“能”或“不能”)说明溶液呈现不同的颜色与其物质的量浓度无关,这是因为充分反应后,I、II两试管中Cu(NO3)2溶液的物质的量浓度_______(填“相等”或“不相等”)。
(3)请你根据乙的实验,推测Cu与浓HNO3反应后溶液呈绿色的原因是________
_______________________________________________________________。
(4)请设计一个方案,验证你所得到的上述结论:___________________________
____________________________________________________________________。
27.(15分)在100℃时,将0.40mol的二氧化氮气体充入2L抽空的密闭容器中,发生反应: 2NO2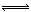 N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
|
时间/s |
0 |
20 |
40 |
60 |
80 |
|
n(NO2)/mol |
0.40 |
n1 |
0.26 |
n3 |
n4 |
|
n(N2O4)/mol |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
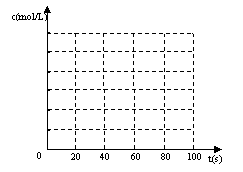 (1)在上述条件下,从反应开始直至20
s时,二氧化氮的平均反应速率为__________mol/(L·s)。
(1)在上述条件下,从反应开始直至20
s时,二氧化氮的平均反应速率为__________mol/(L·s)。
(2)若在相同情况下最初向该容器充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是_________mol/L。假设在80s时达到平衡,请在右图中画出该条件下N2O4和NO2的浓度随时间变化的曲线。
(3)上述(2)达到平衡后四氧化二氮的转化率为_________,混合气体的平均摩尔质量为_________。
(4)达到平衡后,如向该密闭容器中再充入0.32molHe气,并把容器体积扩大为4L,则平衡将 (填“向左移动”、“向右移动”或“不移动”)。
26.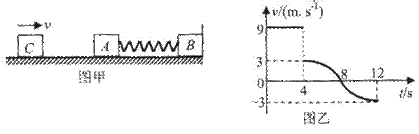 (21分)如图甲所示,物体A、B的质量分别是
(21分)如图甲所示,物体A、B的质量分别是 和
和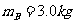 ,用轻弹簧相连放在光滑水平面上,物体B右侧与竖直墙相接触。另有一物体C从
,用轻弹簧相连放在光滑水平面上,物体B右侧与竖直墙相接触。另有一物体C从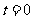 时以一定速度 向右运动,在
时以一定速度 向右运动,在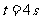 时与物体A相碰,并立即与A粘在一起不再分开。物块C的
时与物体A相碰,并立即与A粘在一起不再分开。物块C的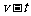 图像如图乙所示。求:
图像如图乙所示。求:
(1)物块C的质量mC;
(2)墙壁对物块B的弹力在4s到8s的时间内对B做的功W及在4s到12s的时间内对B的冲量I的大小和方向;
(3)B离开墙后弹簧具有的最大弹性势能Ep。
25.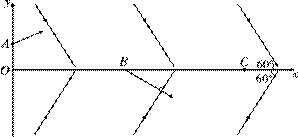 (18分)如图所示,在正交坐标系xOy的第一、四象限内分别存在两个大小相等,方向不同的匀强电场,两组平行且等间距的实线分别表示两个电场的电场线,每条电场线与x轴所夹的锐角均为60°。一质子从y轴上某点A沿着垂直于电场线的方向射入第一象限,仅在电场力的作用下第一次到达x轴上的B点时速度方向正好垂直于第四象限内的电场线,之后第二次到达x轴上的C点。求OB与BC的比值。
(18分)如图所示,在正交坐标系xOy的第一、四象限内分别存在两个大小相等,方向不同的匀强电场,两组平行且等间距的实线分别表示两个电场的电场线,每条电场线与x轴所夹的锐角均为60°。一质子从y轴上某点A沿着垂直于电场线的方向射入第一象限,仅在电场力的作用下第一次到达x轴上的B点时速度方向正好垂直于第四象限内的电场线,之后第二次到达x轴上的C点。求OB与BC的比值。
24.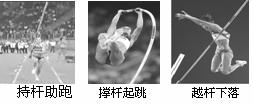 (15分)完整的撑杆跳高过程可以简化成如图所示的三个阶段:持杆助跑、撑杆起跳上升、越杆下落。在第二十九届北京奥运会比赛中,由俄罗斯女运动员伊辛巴耶娃创造的5.05m世界纪录至今无人可破。设伊辛巴耶娃从静止开始以加速度a=1.25m/s2匀加速助跑,速度达到v=9.0m/s时撑杆起跳,到达最高点时过杆的速度不计,过杆后做自由落体运动,重心下降h2=4.05m时身体接触软垫,从接触软垫到速度减为零的时间t=0.90s。已知伊辛巴耶娃的质量m=65kg,重力加速度g取10
m/s2,不计空气阻力。求:
(15分)完整的撑杆跳高过程可以简化成如图所示的三个阶段:持杆助跑、撑杆起跳上升、越杆下落。在第二十九届北京奥运会比赛中,由俄罗斯女运动员伊辛巴耶娃创造的5.05m世界纪录至今无人可破。设伊辛巴耶娃从静止开始以加速度a=1.25m/s2匀加速助跑,速度达到v=9.0m/s时撑杆起跳,到达最高点时过杆的速度不计,过杆后做自由落体运动,重心下降h2=4.05m时身体接触软垫,从接触软垫到速度减为零的时间t=0.90s。已知伊辛巴耶娃的质量m=65kg,重力加速度g取10
m/s2,不计空气阻力。求:
(1)伊辛巴耶娃起跳前的助跑距离;
(2)假设伊辛巴耶娃从接触软垫到速度减为零的过程中做匀减速直线运动,求她对软垫的压力大小。
23. (10分)电流表A1的量程为200
(10分)电流表A1的量程为200 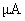 、内电阻约为500
、内电阻约为500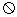 ,现要测其内阻,除若干开关、导线之外还有器材如下:电流表A2:与A1规格相同;滑动变阻器
,现要测其内阻,除若干开关、导线之外还有器材如下:电流表A2:与A1规格相同;滑动变阻器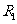 :阻值
:阻值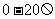 ;电阻箱
;电阻箱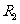 :阻值0-9999
:阻值0-9999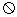 ;保护电阻
;保护电阻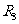 :
: ;电源:电动势E约1.5V内电阻r约
;电源:电动势E约1.5V内电阻r约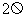 。
。
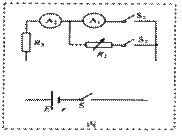
①如图丙所示,某同学设计了部分测量电路,在此基础上请你将滑动变阻器接入电路中,使实验可以完成。
②电路完整后,依你所选方案写出测量电流表A1内电阻的实验步骤。 。
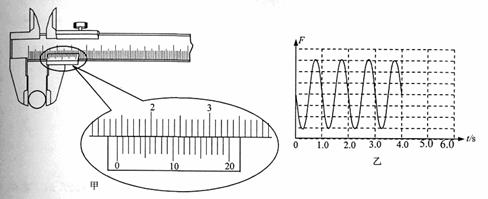
22.(8分)在做“用单摆测定重力加速度”的实验中,用主尺最小分度为1mm,游标上有20个分度的卡尺测量金属球的直径,结果如图甲所示,可以读出此金属球的直径为 mm。单摆细绳的悬点与拉力传感器相连,将摆球拉开一小角度使单摆做简谐运动后,拉力传感器记录了拉力随时间变化的情况,如图乙所示,则该单摆的周期为 s。
21.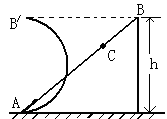 如图所示,一物体以速度v0冲向光滑斜面AB,并能沿斜面升高h,下列说法k_s_5_u正确的是( )
如图所示,一物体以速度v0冲向光滑斜面AB,并能沿斜面升高h,下列说法k_s_5_u正确的是( )
A.若把斜面从C点锯断,由机械能守恒定律知,物体冲出C点后仍能升高h
B.若把斜面弯成如图所示的半圆弧形,物体仍能沿AB/升高h
C.若把斜面从C点锯断或弯成如图所示的半圆弧状,物体都不能升高h,因为机械能不守恒
 若把斜面从C点锯断或弯成如图所示的半圆弧状,物体都不能升高h,但机械能仍守恒
若把斜面从C点锯断或弯成如图所示的半圆弧状,物体都不能升高h,但机械能仍守恒
第Ⅱ卷(非选择题 共174分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com