
29.(18分)
Ⅰ.基因型为AaBb(两对基因自由组合)的某种动物,可以产生下图中各种基因型的子细胞。请回答:
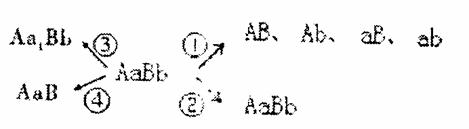
(1)在动物的 (器官)中,可能同时找到AaBb、AB、Ab、aB和ab五种基因型的细胞。
(2)与过程②相比,过程①特有的现象是(要求写4点)
(3)过程①产生的、AB、Ab、aB和ab 4种基因型的细胞,至少需要 个基因型为AaBb细的胞?原因是 。
(4)过程③和④代表的变异分别是 。
Ⅱ.基因型为AaBb(两对基因自由组合)的二倍体水稻,其体细胞中含有24条染色体。用它的花药进行离体培养,在获得由花粉发育成的单倍体植株的同时,也会得到一些由花药壁细胞发育成的二倍体植株。
(1)由花粉发育成的单倍体植株和由花药壁细胞发育成的二倍体植株在幼胚期,形态上并无明显差别,可以采用 的方法,对它们加以区分。
(2)对花药离体培养过程中得到的幼胚,用0.2%-0.4%的秋水仙素进行处理,得到了许多染色体数目增加一倍的植株。其中,两对性状均为显性的基因型是 ;只表现出一种显性性状的基因型有两种,统计这两种植株,其比例与1:1相差甚远,可能原因是:① ②
28.(16分)香豆素内酯化学式为C9H6O2,其分子结构中除含有一个苯外,还有六元环,它可以通过下列合成路线得到:
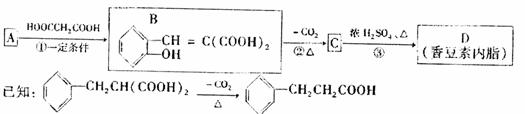
请回答下列问题:
(1)化合物B含有的官能团有(写名称):羟基、 。
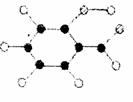 (2)A的分子结构模型如右图所示(图中球与球之间的连线代
(2)A的分子结构模型如右图所示(图中球与球之间的连线代
表化学键,如单键、双键)。则A的结构简式为 。
(3)反应③的化学方程式为 。
(4)写出C物质与足量NaOH溶液反应的化学方程式 。
(5)A的同分异构体有多种,其中含苯环的同分异构体有(可
以不填满,也可增加)
(6)现有C和D的混合物n mol,在空气中完全燃烧,生成CO2 a
L、H2O b g。若设C、D混合物中C的物质的量为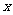 ,则
,则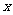 的计算式为(用题中所给字母表示) 。
的计算式为(用题中所给字母表示) 。
27.(12分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂其生产工艺如下:
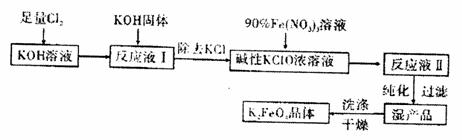
已知:①2KOH+Cl2 KCl+KClO+H2O(条件:温度较低)
②6 KOH+3
Cl2 5KCl+KClO3+3H2O(条件:温度较高)
③Fe(NO3)3 +KClO+KOH K2FeO4+KNO3+KCl+H2O
回答下列问题:
(1)该生产工艺应在 (填“温度较高”或“温度较低”)的情况下进行。(2)配平得到“反应液Ⅱ”的化学反应方程式:
□Fe(NO3)3 +□KClO+□KOH □K2FeO4+□KNO3+□KCl+□H2O
(3)在“反应液Ⅰ”中加KOH固体的主要目的是 。
A.与“反应液Ⅰ”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为KClO
(4)若从“反应液Ⅱ”中分离出m g K2FeO4,则理论上至少消耗氯气V L(换算为标准
状况)。
V= L(用含字母m的算式表示)。
(5)将适量K2FeO4晶体分别溶解于pH为4.74、7.00、11.50的水溶液中,配制FeO42-
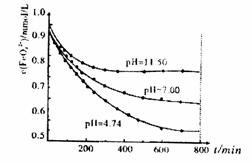 浓度均为1.0×10-3mol·L-1的试样,分别静 置800min至FeO42-浓度不再改变,结
浓度均为1.0×10-3mol·L-1的试样,分别静 置800min至FeO42-浓度不再改变,结
果见右图。已知高铁酸钾在水中的反应为:
 FeO42-+10 H2O 4 Fe(OH)3+8OH
FeO42-+10 H2O 4 Fe(OH)3+8OH
+3O2↑。发现初始pH=11.50的溶液中, 800min时高铁酸钾的最终浓度比pH=4.74的溶液中高,主要原因是: 。
26.(16分)某兴趣小组在实验室用铜和硫酸为原料多种方法制取硫酸铜。制备方法如下:
方法一:
(1)浓硫酸试剂瓶上适合贴上的标签是 (填序号)。

(2)甲同学取6.4 g铜片和10 mL 18mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色沉淀。甲同学为了验证其中白色沉淀的主要成分。设计下列实验:
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌。
实验现象: ;
实验结论:所得白色固体的化学式为 。
(3)乙还观察到加热过程中,起初液面以下出现大量白色烟雾,在试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸面消失。淡黄色固体消失的原因是(用化学反应方程式回答) 。直到最后反应完毕,发现试管中还有铜片剩余。乙根据自己所学的化学知识,认为试管中还有硫酸剩余。他这样认为的理由是 。
|
(4)丙同学认为甲设计的实验方案不好,他自己设计的思路是:2Cu+O2 2CuO,CuO+H2SO4=Cu
SO4+H2O。对比甲的方案,你认为丙同学的优点是
① ,② 。
方法三:
(5)丁同学取一铜片和稀硫酸放在试管中,再向其中滴入双氧水,发现溶液逐渐呈蓝色。写出反应的化学反应方程式 。
25.(14分)已知:X、Y、Z、W为短期元素,Q为人体血红蛋白中所必需的金属元素。X 原子最外层电子排布为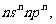 Y原子的L层s电子数比p电子数少1。在第三周期主族元素中,Z元素第一电离能最大;W元素原子半径最大。请回答:
Y原子的L层s电子数比p电子数少1。在第三周期主族元素中,Z元素第一电离能最大;W元素原子半径最大。请回答:
(1)X位于元素周期表中第 周期 族。
Q元素原子基态时的核外电子排布式为 。
(2)X、Y元素对应的氢化物中键能X-H键 Y-H键(填“<”、“>”=
(3)QZ3溶液呈酸性,用离子方程式表示其产生酸性的原因 。
(4)WY3是抗禽流感药物“达菲”合成过程中的中间活性物质,WY3也可用于汽车的保护气囊。3 mol WY3受撞击会生成4 mol Y2气体和一种离子化合物A。
①请写出上述WY3撞击反应的化学方程式 。
②根据电子云的重叠方式判断:Y2分子中存在的σ键和π键数目之比为 : 。
24. (20分)如图所示,内部光滑的木糟质量为mA=m,置于水平桌面上,精与桌面间的动摩擦因数为
(20分)如图所示,内部光滑的木糟质量为mA=m,置于水平桌面上,精与桌面间的动摩擦因数为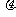 ,槽内有两个小球B、C,它们的质量分别是mB=m,mC=2m,两球间是很短的被压缩的轻弹簧(球与弹簧不连接),且B球到木槽左端、C球到木槽右端的距离均为L,这时弹簧的弹性势能为
,槽内有两个小球B、C,它们的质量分别是mB=m,mC=2m,两球间是很短的被压缩的轻弹簧(球与弹簧不连接),且B球到木槽左端、C球到木槽右端的距离均为L,这时弹簧的弹性势能为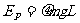 ,同时释放B、C球。并假设小球与槽碰撞后不分离,碰撞时间极短。求: .
,同时释放B、C球。并假设小球与槽碰撞后不分离,碰撞时间极短。求: .
(1)第1个小球与槽碰撞后的共同速度;
(2)第2个小球与槽碰撞后的共同速度;
(3)整个运动过程中,桌面与槽因摩擦而产生的内能。
23.如图所示,M、N为两块带等量异种电荷的平行金属板,两板间电压可取从零到某一最大值之间的各种数值。静止的带电粒子带电量为+q,质量为m(不计重力),从点P经电场加速后,从小孔 Q进入N板右侧的匀强磁场区域,磁感应强度大小为B,方向垂直于纸面向外,CD为磁场边界上的一绝缘板,它与N板的夹角为a=45°,孔Q到板的下端C的距离为L。当M、N两板间电压取最大值时,粒子恰垂直打在CD板上。求
(1)两板间电压的最大值Um;
(2)CD板上可能被粒子打中的区域的长度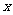
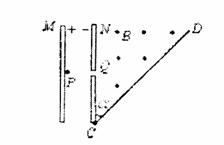 (3)粒子在磁场中运动的最长时间tm。
(3)粒子在磁场中运动的最长时间tm。
22.(14分)跳台滑雪是一种极为壮观的运动,运动员穿着滑雪板,从跳台水平飞出,在空中飞行一段距离后着陆,如图所示。设运动员连同滑雪板的总质量m=50 kg,从倾角θ=37°的坡顶A点以速度 =20m/s沿水平方向飞出,恰落到山坡底的水平商上的B处。(g=10m/s2,sin37°=0.6,cos37°=0.8)求:
=20m/s沿水平方向飞出,恰落到山坡底的水平商上的B处。(g=10m/s2,sin37°=0.6,cos37°=0.8)求:
(1)运动员在空中飞行的时间t和AB间的距高s;
(2)运功员落到水平面上的B处时顺势屈腿以缓冲,使他垂直于水平面的分速度在△t=0.20s的时间内减小为零。试求缓冲过程中滑雪板对水平面的平均压力。

21.(18分)
Ⅰ.(6分)用已调零且选择开关指向欧姆挡“×100”位置的多用电表与量程为1V的电压表按如图所示方式连接,两表指针的位置如图所示。电压表接线柱A是 (选填“正”或“负”)接线柱,此时通过电压表的电流为 mA。
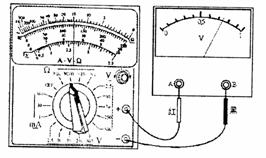
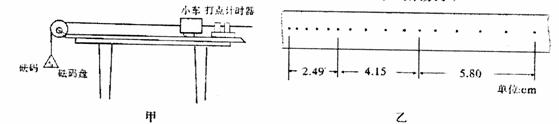
Ⅱ.(6分)“探究加速度与物体质量、物体受力的关系”的实验装置如图甲所示。
(1)在小车某次运动过程中,打出了一条纸带如图乙所示。计时器打点的时间间隔为0.02s,从比较清晰的点起,每5个点取一个计数点,并量出了相邻计数点之间的距离。该小车的加速度a= m/s2.(结果保留三位有效数字)
(2)一组同学先保持盘及盘中的砝码质量m一定,探究加速度与小车(包括车中砝码)质量M的关系,以下做法正确的是 ( )
A.平衡摩擦力时,应将盘及盘中的砝码用细绳通过定滑轮系在小车上
B.每次改变小车的质量时,不需要重新平衡摩擦力
C.实验时,先放开小车,再接通打点计时器电源
D.小车运动的加速度可根据m以及M,直接用公式a=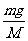 求出。
求出。
(3)在保持持小车及车中的砝码质量M一定,探究加速度与所受合外力的关系时.二位同学根据各自的实验数据分别作出的a-F图线如图甲、乙所示,对这两图的分析正确的是 ( )
 A.甲图图线不通过原点,可能是因为计算
A.甲图图线不通过原点,可能是因为计算
F时未计入砝码盘的重力;
B.甲图图线不通过原点,可能是因为没有
平衡摩擦力;
C.乙图图线的弯曲部分,是因为小车的质
量太大。
D.乙图图线的弯曲部分,是因为盘中的砝
码总质量太大。
Ⅲ.(6分)某实验小组利用如图所示电潞探究一种电阻丝的电阻率。均匀电阻丝(总阻值在 4Ω-5Ω之间)固定在刻度尺上的两端接线柱a和b上,刻度尺的中间有一个可沿电阻丝滑动的触头c,c的上端为接线柱,触头c与电阻丝通常不接触,当用手按下时,才与电阻丝接触,且可在直尺上读出触点的位置:所用器材为:电压表(0-3V,电阻约为 3kΩ)、电流表(0-0.6A,电阻约为0.5Ω)、电池组(电动势3V,内阻很小)、保护电阻R0=1Ω、螺旋测微器、开关S和导线。
实验的主要步骤如下:
①用螺旋测微器测得电阻丝的直径为d=2.000mm;
②正确连接电路,触头c移到右端,合上开关,读出电流表的示数I=0.5A:
③通过改变滑动变阻器触头c的位置,分别测量出了多组a、c间电阻丝长度L及对应的 电压U的数据,并据此在U-L坐标纸上描出了对应的点,如图所示。请你:
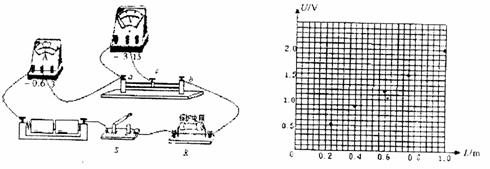
(1)在U一L坐标纸上绘出U一L图线;
(2)若测出U一L图线斜率为k,写出用d、l、k表示的该电阻丝的电阻率表达式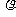 =
;
=
;
(3)代入有关数据求出该电阻丝的电阻率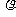 =
Ω·m。
=
Ω·m。
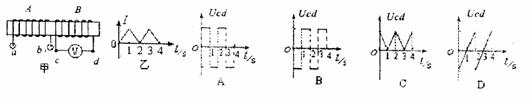
20.紧靠在一起的线图A与B如图甲所示,当给线圈A通以图乙所示的电流(规定由a端流入线圈,b端流出线圈为电流正方向)时,线圈B两的电压变化应为下图中的 ( )
第Ⅱ卷(本卷共11小题,共180分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com