
35.(1)2.8克(1分)(2)14.4%(2分)
房山区
35.(3分)某化学调查小组的同学到钢铁厂做社会调查。他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制成如下图像:
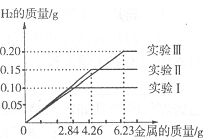
(1)实验I中铁参加反应的质量为 。
(2)稀硫酸完全参加反应的实验中,反应后溶液中溶质的质量分数是多少。
1.06
g碳酸钠中钠元素的质量:1.06
g×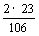 = 0.46 g
= 0.46 g
|
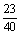 = 0.8 g
= 0.8 g
⑵所得溶液中氢氧化钠的质量分数:
|
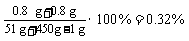
答:略
怀柔区
35.(3分)
|
Na2CO3 + Ca(OH)2 CaCO3 ↓+ 2NaOH
106 100 80
x 1 g y
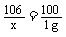
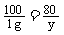
x=1.06 g y=0.8 g
35.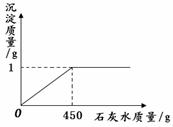 (3分)取一定质量的氢氧化钠和碳酸钠混合物完全溶于水中,得到51 g溶液,再向溶液中滴加石灰水,产生沉淀的质量与加入石灰水的质量关系如图所示。若氢氧化钠和碳酸钠混合物中钠元素的质量为0.92 g。试计算:
(3分)取一定质量的氢氧化钠和碳酸钠混合物完全溶于水中,得到51 g溶液,再向溶液中滴加石灰水,产生沉淀的质量与加入石灰水的质量关系如图所示。若氢氧化钠和碳酸钠混合物中钠元素的质量为0.92 g。试计算:
⑴混合物中氢氧化钠的质量。
⑵恰好反应时,所得溶液中溶质的质量分数。
35.(4分)解:(1)设需要NaOH的质量为x。则:
2NaOH+H2SO4=Na2SO4+2H2O
80 98
x 100kg×4.9% -------------------1分
解得:x= =4kg
-
------------------1分
=4kg
-
------------------1分
(2)设改进后需要Ca(OH)2的质量为y。
Ca(OH)2+H2SO4=CaSO4+2H2O
74 98
y 100kg×4.9%
解得:y= =3.7kg
-------------------1分
=3.7kg
-------------------1分
则可以节约经费:4kg×24.00元/kg-3.7kg×6.00元/kg=73.8元 ------------1分答:略
石景山区
35.(4分)某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。请计算:
(1)若要清洗100kg的这种石油产品,需要多少千克的NaOH?
(2)石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理100kg这种产品,可以节约多少经费?NaOH和Ca(OH)2的市场价格如下表:
|
名 称 |
Ca(OH)2 |
NaOH |
|
价格(元/kg) |
6.00 |
24.00 |
35.解:设该纯碱样品中碳酸钠的质量为x,生成的氯化钠的质量为y,
Na2CO3 +2 HCl = 2NaCl + H2O + CO2↑
106 117 44
x y 3.52g
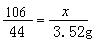
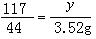
x=8.48g y=9.36g
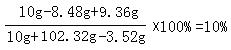
答:得到的是不饱和溶液,因为任何温度下饱和溶液溶质的质量分数都大于10%
门头沟区
35.(3分)用“侯氏制碱法”制得的纯碱常含有少量的氯化钠。将10g含有氯化钠的纯碱样品溶解于102.32g稀盐酸中,恰好完全反应,收集到3.52g的气体(假设生成的气体全部逸出)。查阅相关资料:不同温度下氯化钠的溶解度
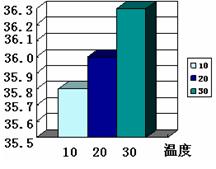 求:(1)制得纯碱中含碳酸钠的质量分数?
求:(1)制得纯碱中含碳酸钠的质量分数?
(2) 样品与盐酸反应后,得到溶液的质量分数是多少?
(3)通过计算说明烧杯中的溶液是否为饱和溶液。
35.(3分)(1)丙 (2)95% (3)9.8%
答:略。
密云
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com