
31.(10分)人的血清白蛋白通常是从人血中提取。如果应用一定的生物工程技术,将人的血清白蛋白基因转入奶牛细胞中,利用牛的乳腺细胞生产人的血清白蛋白就成为可能。大致过程如下图:
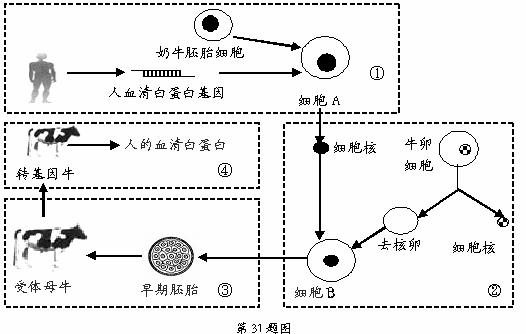
请回答下列问题:
(1)如要在体外迅速扩增人血清白蛋白基因可采用PCR技术,此技术与细胞内DNA复制比较,所不需要的酶是 。若采用PCR技术第一轮子代DNA中各含一段引物,分别是引物1和引物2,则第2轮后所得子代DNA中含引物1占所有子代DNA的比例为 。
(2)实验过程②利用的技术是 ,胚胎工程操作中最后环节是 。
(3)若将实验过程③中的早期胚胎分离成若干个胚胎细胞,让其分别发育成小牛,理论上这些小牛的基因型 (相同/不同),理由是 。
(4)若要将人的血清白蛋白与乳汁蛋白分离,可采用 法,其中相对分子质量大的蛋白 (先/后)洗脱。
(5)上述整个过程实现了 , 和胚胎工程的综合应用。
30.(24分)棉花的纤维有长纤维和短纤维,纤维的颜色有白色和紫色。控制这两对相对性状的等位基因位于非同源染色体上。控制纤维的白色与紫色基因用A、a表示,控制纤维的长与短的基因用B、b表示。现用紫色短纤维植株甲、乙分别与白色长纤维植株丙杂交,结果如下表:
|
组合 序号 |
杂交组合类型 |
子代的表现型 |
|
|
紫色短纤维 |
白色短纤维 |
||
|
一 |
甲×丙 |
210 |
208 |
|
二 |
乙×丙 |
420 |
0 |
请回答:
(1)棉花纤维的紫色和白色不同,主要是催化纤维合成的 不同。
(2)杂交过程中,必需的操作步骤是 。
(3)综合组合一和二的分析,组合 验证了孟德尔的 定律。判断的依据是 。
(4)若要得到市场上需要的免染色、含有天然紫色色素并且具有长纤维的具有经济价值高的棉花,可用上述表格中提供的材料选择最佳的类型以在最短的时间内获得能稳定遗传的个体。请用图解表示此选育过程。
(5)假设用双显性状的棉花丁和未知性状的棉花戊交配,子代的表现型除了表格中的两种外还有两种不同的类型,其比例为3︰3︰1︰1。则丁基因型为 ,戊的基因型为 。
29.(20分)下图中甲图曲线a表示某种植物在20℃、CO2浓度为0.03%的环境中随着光强度的变化光合作用合成量的变化;在B点时改变某种条件,结果发生了如曲线b的变化。丙图表示某植物在不同温度下CO2的吸收量和释放量,请分析回答。
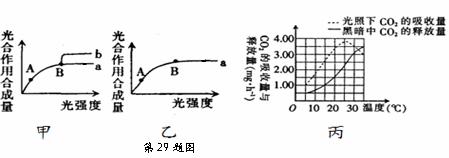
(1)若在甲图的B点时适当增大二氧化碳浓度,能否得到b曲线? 。其原因是:
。
(2)甲图中A点与B点相比较,A点时叶绿体中C3的含量 (填 “多”或“少”),[H]的含量 (填“多”或“少”)。甲图中如果在A点时温度降低10℃,请在乙图中画出A点后的曲线。
(3)丙图中在5℃时光合作用制造的有机物量是呼吸消耗有机物量的 倍。
(4)叶的形态包括颜色和形状。植物在黑暗中生长时呈现黄色和形状异常的现象,即“黄化现象”。有人做了如下实验:将花菜豆幼苗在暗处放置了7-8天,使之黄化后,每天按要求给予如下光照,结果如下:
|
光强 |
每天照光时间 |
结 果 |
|
弱光 |
0.5h |
无论光照时间的长短都逐渐恢复到正常。光照和后,能形成很多的叶绿素 |
|
2 h |
||
|
4 h |
||
|
12 h |
||
|
强光 |
1 min |
光照和时,恢复到正常形状的程度与上述光照和差不多,但是不能形成叶绿素。延长光照时间后叶绿素才逐渐合成 |
|
4 min |
||
|
10 min |
||
|
30 min |
根据上述实验结果,回答下列问题:
①请拟定该实验课题的名称: 。
②长时间在黑暗中生长的植物叶片呈黄色或黄白色的原因是 。
③由此进一步推出,从黄化恢复到正常形状与植物的光合作用是否有关? 。为什么?_______________________________。
28.(14分)
某工厂以含有大量CuS及少量铁的化合物的炼铁废渣为原料,生产CuCl2·2H2O的工艺流程如下:

材料1:焙烧过程发生的主要反应为:CuS + 2O2 + 2NaCl = Na2SO4 + CuCl2
材料2:氢氧化物沉淀的pH
|
物 质 |
Fe(OH)3 |
Cu(OH)2 |
Fe(OH)2 |
|
开始沉淀时的pH |
2.7 |
4.4 |
7.6 |
|
沉淀完全时的pH |
3.7 |
6.4 |
9.6 |
回答下列问题:
(1)若试剂A是NaClO,其作用是 ,调节溶液pH的范围为 。
(2)上述工艺流程产生的废气(含SO2的体积分数2.4%、O2的体积分数8.0%、N2及少量其他气体)中,SO2是工业合成H2SO4的原料。现将10m3废气通入一个带有活塞的体积可变的密闭容器中,同温同压下发生下述反应2SO2
+ O2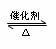 2SO3。
当反应达到平衡时,测得容器内气体体积为9.89m3,则反应中SO2的转化率为 ;此时若向容器内充入一定量惰性气体,到达新平衡时c(SO3)/c(SO2)的值将 (填“增大”、“减
2SO3。
当反应达到平衡时,测得容器内气体体积为9.89m3,则反应中SO2的转化率为 ;此时若向容器内充入一定量惰性气体,到达新平衡时c(SO3)/c(SO2)的值将 (填“增大”、“减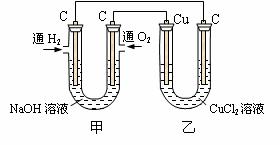 小”或“不变”)。
小”或“不变”)。
(3)将上述工艺流程生产的CuCl2·2H2O配成溶液, 按如右图所示装置进行实验。请回答:
甲池中通H2一侧的电极反应是 ,一段时间后测得乙池中C棒增重1.6g,则甲池中参加反应的O2的体积为 L(标准状况下),乙池中CuCl2溶液的pH如何变化 (填“增大”、“减小”、“不变”)。
27.(15分)
过氧化氢是一种无色黏稠的液体,它的水溶液俗称双氧水,它不稳定,既有氧化性,又有还原性,实验室里常把过氧化氢装在棕色瓶内避光并放在阴凉处。
(1)下表是某研究性学习小组研究影响过氧化氢分解速率的因素时记录的一组数据:
(用10mL H2O2溶液在不同条件下制取150mL氧气所需的时间)
|
浓 度 反应条件 |
30% H2O2 |
15% H2O2 |
10% H2O2 |
5% H2O2 |
|
无催化剂、不加热 |
几乎不反应 |
几乎不反应 |
几乎不反应 |
几乎不反应 |
|
无催化剂、加
热 |
300 s |
450 s |
520 s |
690 s |
|
有催化剂、加 热 |
10 s |
25 s |
60 s |
120 s |
请回答:该研究小组在设计方案时,考虑了浓度、 、 等反应条件对过氧化氢分解速率的影响。
(2)已知:CuSO4溶液对过氧化氢的分解具有催化作用,FeCl3溶液是否也具有催化作用?
于是某同学按右图进行实验,并用带火星的木条检验产生的气体。
 实验现象:
实验现象:
。
实验结论:FeCl3溶液可以催化H2O2 分解。
(3)探究过氧化氢的氧化性:根据所提供的实验条件设计一个实验,证明过氧化氢的氧化性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选)。请将实验步骤和实验现象填入下表:
|
实验内容 |
实验步骤 |
实验现象 |
|
验证氧化性 |
|
|
(4)已知:双氧水在碱性溶液中远比在酸性溶液中分解速率快。请分析实验室中利用Na2O2制
H2O2的条件: ;
双氧水中滴入酸化的KMnO4溶液,溶液的紫红色消失(MnO4-转化为Mn2+),此时双氧水表现出 性,反应的离子方程式为: 。
26. (14分)
(14分)
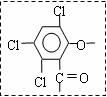
CPPO(分子式为C26H24O8Cl6)用于渲染60年国庆晚会现场气氛的魔棒中。
已知:CPPO的分子结构是一种对称结构,如右图是其结构的一部分。现设计了如下的合成路线。
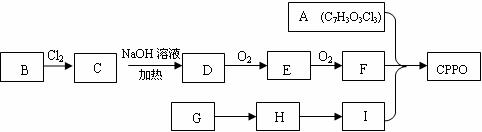
其中,G是一种有三种同分异构体的烷烃,I是一种只有一个-CH3的醇,且与G具有相同的碳原子数。请回答下列问题:
(1)B是一种常见气体,可做果实催熟剂,其分子中两个碳原子之间含有两个强度不同的共价键,其中σ键的强度比π键的强度 (填“大”或“小”)。请写出实验室制取B的化学方程式: 。
(2)A可以与醇或酸在一定条件下均能反应生成具有果香味的有机化合物。请写出A的结构简式: 。
(3)请写出G的沸点最低的同分异构体的结构简式: 。
1molCPPO能与 molH2发生加成反应。
(4)写出一定量的C在足量NaOH醇溶液中加热充分反应的化学方程式:
。
(5)写出一定量的E与足量银氨溶液发生银镜反应的化学方程式:
。
25.(15分)
A、B、D、E、G、Q分别为前四周期6种常见元素,原子序数依次递增。A与B能形成多种气态化合物,其中有一种是天然气的主要成分。E与B同周期且基态原子核外具有相同的未成对电子数。G的简单阳离子与E离子有相同的电子排布。G的p轨道上只有一个未成对电子,Q元素基态价电子排布式为3d64s2。请回答:
(1)Q位于元素周期表第_______周期第_______族, D的电负性比E的电负性_________(填“大”或“小”)。
(2)4g B单质完全燃烧放出131.2 kJ的热量,写出表示B单质燃烧热的热化学方程式:
。
(3)A、B、D、E可组成多种18 电子的分子,请写出其中两种具有18 电子的有机物的结构简式 、 。
(4)G的单质与Q的红棕色氧化物高温下能反应生成Q的单质,写出该反应的化学方程式:
。
(5)常温下,ADE3和盐A4D2E3的水溶液pH均为5。则两种水溶液中由水电离出的H+ 浓度之比是 。
24.(20分)
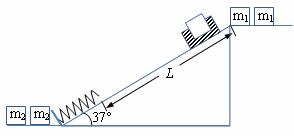
低碳经济已引起高度关注,其核心是利用绿色能源和可再生能源,减少能量应用过程中的CO2排放,为此某探究活动小组设计了如下图所示的节能运输系统。斜面轨道倾角为37°,斜面底端固定了轻弹簧,轻弹簧原来为原长,轻弹簧上端与轨道顶端的距离L=10m,运输用载货箱M与轨道间的动摩擦因数为μ=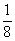 。载货箱在轨道顶端时位于顶端的装卸工将质量为m1的货物装入货箱,然后载货箱载着货物沿轨道无初速滑下,当轻弹簧被压缩至最短时,位于底部的两装卸工立刻将货物m1卸下,同时在载货箱中装入货物m2。然后载货箱和货物m2在弹簧的作用下被弹回到轨道顶端,在顶端的装卸工又取下m2装上m1,然后重复上述过程。若M=5kg,m1=44kg,(sin37°=0.6,cos37°=0.8,g=10m/s2),问
。载货箱在轨道顶端时位于顶端的装卸工将质量为m1的货物装入货箱,然后载货箱载着货物沿轨道无初速滑下,当轻弹簧被压缩至最短时,位于底部的两装卸工立刻将货物m1卸下,同时在载货箱中装入货物m2。然后载货箱和货物m2在弹簧的作用下被弹回到轨道顶端,在顶端的装卸工又取下m2装上m1,然后重复上述过程。若M=5kg,m1=44kg,(sin37°=0.6,cos37°=0.8,g=10m/s2),问
(1)当载货箱和货物m1下滑至刚接触轻弹簧时的速度大小是多少?
(2)若载货箱和货物m2在弹簧的作用下被弹回到轨
道顶端时速度恰好为零,则m2的质量为多少?
23.(16分)
如图所示,在y轴竖直向上的直角坐标系中,电场、磁场的分布情况如下:
(Ⅰ)在y<0区域内,存在沿y轴正向的匀强电场;
(Ⅱ)在y<y1区域内,同时存在垂直xoy平面向外的匀强磁场B。
 质量为m、电量为q带正电的小球A,从xoy平面内第二象限的P点以初速v0向右水平抛出。
质量为m、电量为q带正电的小球A,从xoy平面内第二象限的P点以初速v0向右水平抛出。
小球A恰好过坐标原点O,方向与x轴成60°,之后沿直线运动到达磁场区,且小球A能够第二次到达原点O,其中B、m、v0、q为已知量,重力加速度已知为g。
试求:(1)电场强度E的大小;
(2)小球A两次通过O点经历的时间间隔。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com