
19.(8分)写出下列物质电离或盐水解的离子方程式:
(1)NaHSO4溶于水_______________________________________________________
(2) H2S的电离________________________________________________________
(3)氯化铁溶液: ;
(4)碳酸钠溶液: ;
(5)AlCl3与NaHCO3混合____________________________________________________
18.下列叙述正确的是( )
A.0.1mol·L-1氨水中,c(OH-)=c(NH4+)
B.10 mL 0.02mol·L-1HCl溶液与10 mL 0.02mol·L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
C.在0.1mol·L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)+c(CH3COO-)
D.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
17.(平行班做)常温下,把pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,在所得溶液中离子浓度大小关系正确的是( )
A.c(CH3COO-)>c(Na+)>c(OH-)>c(H+) B.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.c(CH3COO-)>c(Na+)>c(H+)=c(OH-) D.c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
17.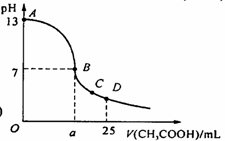 (实验班做)在25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2 mol/L CH3COOH溶液,曲线如下图所示,有关粒子浓度关系比较正确的 ( )
(实验班做)在25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2 mol/L CH3COOH溶液,曲线如下图所示,有关粒子浓度关系比较正确的 ( )
A.在A、B间任一点,溶液中一定都有
c(Na+) > c(CH3COO-) > c(OH-) > c(H+)
B.在B点,a > 12.5,且有
c(Na+) = c(CH3COO-) = c(OH-) = c(H+)
C.在C点:c(CH3COO-) = c(Na+) > c(H+) > c(OH-)
D.在D点:c(CH3COO-) + c(CH3COOH) = 2c(Na+)
16.(平行班做)在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡:
CH3COOH CH3COO-+H+ ,对于该平衡,下列叙述正确的是(
)
CH3COO-+H+ ,对于该平衡,下列叙述正确的是(
)
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)不变
D.加入少量CH3COONa固体,平衡向正反应方向移动
16. (实验班做) 在一定的温度下,向CH3COONa的稀溶液里加水稀释,下列各种量的变化中,变大的是( )
①c(H+)的物质的量浓度 ②c(OH-)的物质的量浓度
③c (CH3COO-)/c(CH3COOH) ④水的浓度⑤c(H+)·c(OH-)
A .① ④ B. ① C. ③④ D. ②⑤
15.把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液以等体积混和,则混合液中微粒浓度关系正确的为 ( )
A.c (CH3COO-)>c (Na+) B.c (OH-)>c (H+)
C.c (CH3COOH)>c (CH3COO-) D.c (CH3COOH)+c (CH3COO-)=0.02mol/L
14.(平行班做)室温时,下列混合溶液的pH一定小于7的是( )
A.pH = 3的盐酸和pH = 11的氨水等体积混合
B.pH = 3的盐酸和pH = 11的氢氧化钡溶液等体积混合
C.pH = 3的硫酸和pH = 11的氨水等体积混合
D.pH = 3的醋酸和pH = 11的氢氧化钡溶液等体积混合
14.(实验班做)室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是
A 0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液
B.0.2 mol/L的盐酸和0.1mol/L的氢氧化钡溶液
C.pH=4的醋酸溶液和pH=10的氢氧化钠溶液
D.pH=4的盐酸和pH=l0的氨水
13.下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是( )
①胆矾 ②氯化铝 ③硫酸铝 ④Na2CO3 ⑤NaHCO3 ⑥高锰酸钾
A.③④ B.①③④ C.①②③④⑤ D.全部
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com