
5.

图9-2-14
在国庆焰火联欢晚会中,天空中出现了如图9-2-14所示的雪域天路巨幅烟花画,现场观众均为我国交通运输的发展而兴高采烈.铁路运输的原理是:将能够产生匀强磁场的磁铁安装在火车首节车厢的下面,如图9-2-16甲(俯视图)所示,当它经过安放在两铁轨之间的矩形线圈时,线圈会产生一个电信号传输给控制中心.已知矩形线圈的长为L1,宽为L2,匝数为n.若安装在火车首节车厢下面的磁铁产生的匀强磁场的宽度大于L2,当火车通过安放在两铁轨之间的矩形线圈时,控制中心接收到线圈两端的电压信号u随时间t变化的关系如图9-2-15乙所示.不计线圈电阻,据此计算:
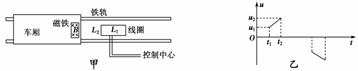
图9-2-15
(1)火车的加速度;
(2)火车在t1-t2时间内的平均速度和安装在火车首节车厢下面的磁铁产生的匀强磁场宽度.
解析:(1)根据法拉第电磁感应定律可知,线圈中产生的感应电动势E=nBL2v
不计线圈电阻,t1时刻线圈两端电压u1=nBL2v1,t2时刻线圈两端电压u2=nBL2v2
则火车的加速度a=(v2-v1)/(t2-t1),联立解得a=.
(2)由于火车做匀加速运动,火车在t1-t2时间内的平均速度v=(v2+v1)/2=,安装在火车首节车厢下面的磁铁产生的匀强磁场的宽度D=v(t2-t1)=(t2-t1).
答案:(1) (2)(t2-t1)
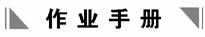
4.如图9-2-13所示,在一倾角为37°的粗糙绝缘斜面上,静止地放置着一个匝数n=10匝的圆形线圈,其总电阻R=3.14 Ω、总质量m=0.4 kg、半径r=0.4 m.如果向下轻推一下此线圈,则它刚好可沿斜面匀速下滑.现在将线圈静止放在斜面上后.在线圈的水平直径以下的区域中,加上垂直斜面方向的,磁感应强度大小按如图9-2-14所示规律变化的磁场(提示:通电半圆导线受的安培力与长为直径的直导线通同样大小的电流时受的安培力相等)问:
(1)刚加上磁场时线圈中的感应电流大小I=?
(2)从加上磁场开始到线圈刚要运动,线圈中产生的热量Q=?(最大静摩擦力等于滑动摩擦力,sin 37°=0.6,cos 37°=0.8,g取10 m/s2.)
解析:(1)由闭合电路的欧姆定律I=,由法拉第电磁感应定律E=n,
由图得,=0.5 T/s,S=πr2.联立解得I=0.4 A.
(2)设线圈开始能匀速滑动时受的滑动摩擦力为Ff,则mgsin 37°=Ff加变化磁场后线圈刚要运动时nBIL=mgsin 37°+Ff,其中L=2r,由图象知B=B0+kt=1+0.5t,由焦耳定律Q=I2Rt,联立解得Q=0.5 J.
答案:(1)0.4 A (2)0.5 J
3.(2009·全国Ⅱ,24)如图9-2-12所示,匀强磁场的磁感应强度方向垂直于纸面向里,大小随时间的变化率=k,k为负的常量.用电阻率为ρ、横截面积为S的硬导线做成一边长为l的方框.将方框固定于纸面内,其右半部分位于磁场区域中,求:
(1)导线中感应电流的大小;
(2)磁场对方框作用力的大小随时间的变化率.
解析:(1)导线框的感应电动势为E=①
ΔΦ=l2ΔB②
导线框中的电流为I=③
式中R是导线框的电阻,根据电阻率公式有R=ρ④
联立①②③④式,将=k代入得I=.⑤
(2)导线框所受磁场的作用力的大小为F=BIl⑥
它随时间的变化率为=Il⑦
由⑤⑦式得=.⑧
答案:(1) (2)
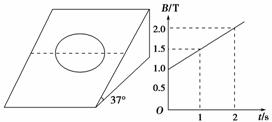
图9-2-13
2.
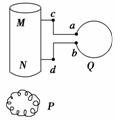
图9-2-11
(2010·陕西省西安市统考)如图9-2-11所示,Q是单匝金属线圈,MN是一个螺线管,它的绕线方法没有画出,Q的输出端a、b和MN的输入端c、d之间用导线相连,P是在MN的正下方水平放置的用细导线绕制的软弹簧线圈.若在Q所处的空间加上与环面垂直的变化磁场,发现在t1至t2时间段内弹簧线圈处于收缩状态,则所加磁场的磁感应强度的变化情况可能是( )
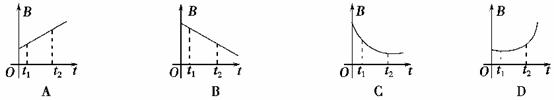
解析:在t1至t2时间段内弹簧线圈处于收缩状态,说明此段时间内穿过线圈的磁通量变大,即穿过线圈的磁场的磁感应强度变大,则螺线管中电流变大,单匝金属线圈Q产生的感应电动势变大,所加磁场的磁感应强度的变化率变大,即B-t图线的斜率变大,选项D正确.
答案:D
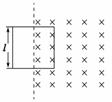
图9-2-12
1.如图9-2-10所示,MN、PQ为两条平行的水平放置的金属导轨,左端接有定值电阻R,金属棒ab斜放在两导轨之间,与导轨接触良好,磁感应强度为B的匀强磁场垂直于导轨平面,设金属棒与两导轨接触点之间的距离为L,金属棒与导轨间夹角为60°,以速度v水平向右匀速运动,不计导轨和棒的电阻,则流过金属棒中的电流为( )
A.I= B.I= C.I= D.I=
解析:(1)导体棒匀速运动,所以平均感应电动势的大小等于瞬间感应电动势的大小.
(2)题中L的有效长度为,故E=Bv.
据闭合电路欧姆定律得I=.
答案:B
(二)苯及其同系物:
1、苯的结构:分子式:C6H6,最简式CH,结构简式: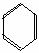 (凯库勒式)
(凯库勒式)
结构特点:苯分子为平面结构,碳碳键的键长、键角均相等,键角120°,键长介于单、双键之间,苯分子中的键是一种独特的键,由一个大π键和6个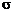 键组成。
键组成。
2、苯的性质
物理性质:苯是一种无色、有特殊香味、易挥发的液体,熔点5.5℃、沸点80.5℃,当温度较低时凝结成无色晶体。比水轻,难溶于水,是常用的有机溶剂,苯是重要的有机化工原料。
苯的化学性质:苯分子的特殊结构决定了苯分子稳定性,常温下苯不与溴水发生加成反应,也不能被酸性KMnO4溶液所氧化,在一定条件下,苯能与Cl2、溴单质、浓硝酸等发生反应。
⑴取代反应(与卤素单质、浓硝酸的取代):
⑵燃烧反应:
⑶加成反应(与H2加成)
3、苯的同系物:
苯分子中的H原子被烷基取代后的生成物,其分子通式为:CnH2n-6(n≥6),而芳香烃是指分子中有苯环的烃,它可以含有1个或多个苯环,苯的同系物属于芳香烃。芳香族化合物是指分子里含有一个或多个苯环的化合物,它包括芳香烃和它们的衍生物。
苯的同系物的物理性质:苯的同系物一般为无色液体,具有特殊气味,有毒,难溶于水,密度比相对分子质量相近的烷烃及烯烃的大,但小于1,其中甲苯、二甲苯常用作有机溶剂.
苯的同系物的化学性质
苯的同系物中含苯环和烷基,二者共同影响,使苯的同系物的性质不是苯和烷烃的性质的简单相加。苯的同系物的化学性质与苯相似。
①取代(比苯更容易,侧链对苯环的影响)
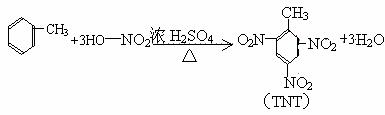
甲苯与液溴的取代:
a、苯环上的取代
b、侧链上的取代
②氧化反应:燃烧生成CO2和H2O,能被酸性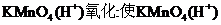 褪色
褪色
③加成反应:(与H2加成,生成环己烷等物质)
说明:
1、苯及其同系物能将溴水中的溴萃取,但不能发生加成反应,萃取了溴的苯或苯的同系物在上层,呈橙色,水在下层。
2、书写苯的同系物的同分异构体时,苯环不变,变取代基的位置,变取代基碳链的长短。如C9H12对应的苯的同系物有以下八种同分异构体。
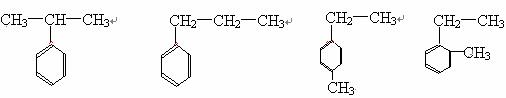
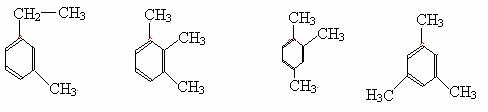
3、发生加成反应,苯及其同系物比烯烃、炔烃困难;
4、苯及其同系物发生取代反应时,条件不同,产物不一样。当在铁或Fe3+作催化剂时,苯与卤素单质发生苯环上的取代反应,生成卤代苯;而在光照的条件下,则是苯环侧链上的H被X原子所取代;
5、两个重要实验:
(1)苯和液溴的取代反应:
装置见下图:
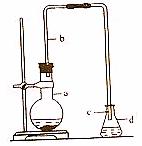
①试剂加入顺序:先加苯,再加溴,最后加铁粉。
②长导管b段的作用:导气和冷凝。
③导气管c段出口不插入液面下的原因是:防止溶液倒吸,因HBr极易溶于水。
④现象:导管出口有白雾(HBr遇水形成);锥形瓶d中加AgNO3溶液有浅黄色沉淀生成。
⑤烧瓶的橡胶塞用锡箔包住的原因:防溴蒸气腐蚀胶塞。
⑥把反应后圆底烧瓶中混合液分离开的方法:把混合液倒入盛水的烧杯,底部有褐色不溶于水的液体(这是溶有溴单质的溴苯),再向其中加入NaOH溶液洗涤(除Br2)后用分液漏斗分液即可,纯净的溴苯是无色不溶于水的液体。
⑦苯的用量不可太多,因苯、溴苯、溴相互溶解,当反应混合物倒入水中时不会在烧杯底部看到褐色液体。
(2)苯的硝化反应:
①试剂加入顺序是先加浓HNO3再加浓H2SO4,冷却后再加入苯,因为若先把浓HNO3加到浓H2SO4中易发生液体飞溅;两种酸混合时放出大量的热,易使HNO3分解,使苯挥发并会出现其他副反应。
②用水浴加热,温度计水银球应插入水浴中。水浴加热的好处:a受热均匀,b温度易控制。测水浴温度,应把水银球放入水浴中。要与实验室制乙烯时温度计的位置区别开来。
③硝基苯是无色、有毒、有苦杏仁味的油状液体,密度比水大。生成的硝基苯有黄色,原因是溶解了NO2。可通过加NaOH溶液的方法除去,然后分液。
[例1]能说明苯分子平面正六边形结构中碳碳键不是单双键相交替的事实是:
A、苯的一元取代物没有同分异构体
B、苯的间位二元取代物只有一种
C、苯的邻位二元取代物只有一种
D、苯的对位二元取代物只有一种
解析:如果苯分子是单、双键交替组成的环状结构,则苯分子的结构应为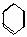 ,那么苯的邻
,那么苯的邻
|
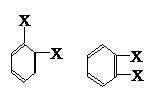
但是实际上苯的邻位二元取代物不存在同分异构体,说明苯分子中的碳碳键都是完全等同的。
答案:C
[例2]在沥青蒸汽里含有多种稠环芳香烃,其中一些可视为同系物,如A,B,C……所示。它们都含有偶数个苯环结构。
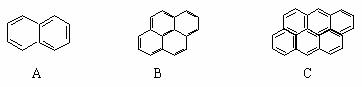
(1)该系列化合物中,相邻两化合物间递增的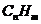
 值中的n和m 的数值分别是:n= ,m=
,其等差数列的公差为
。
值中的n和m 的数值分别是:n= ,m=
,其等差数列的公差为
。
(2)该系列化合物的通式为 。
(3)该系列化合物中第25个分子式是 。
(4)该系列化合物分子中所含C、H原子数的最大比值最接近于
(5)该系列化合物中所含碳元素的最大质量分数是 。
解析:(1)根据上述三种化合物的结构简式,可知其分子式分别为C10H8、C16H10、C22H12,从而可知这个等差数列的公差为C6H2,其中n=6,m=2。
(2)求通式要在分析前后两个分子式之差的基础上进行,令n=1时分子式为C10H8,因等差数列的公差为C6H2,则通式为C6n+4H2n+6(n=1,2,3……)
或者根据其分子式分别为C10H8、C10+6H8+2、C10+6+6H8+2+2可知,每增加两个苯环,分子中就增加6个碳原子(故碳原子是6n倍增加),增加2个氢原子(故氢原子是2n倍增加),则通式为C6n+4H2n+6。
(3)当n=25时,则分子式为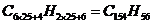 。
。
(4)该系列化合物分子中所含C、H原子数的最大比值可通过该化合物的通式求极限求得:
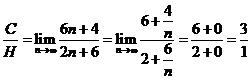
(5)该系列化合物中碳的最大质量分数为
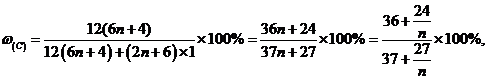
当 时,
时,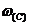 的极大值为
的极大值为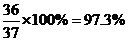
答案:(1)n=6,m=2;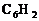
(2)C6n+4H2n+6(n=1,2,3……);
(3)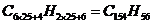
(4)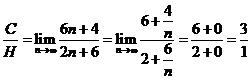
(5)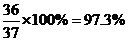
[例3]二甲苯苯环上的一溴代物有六种同分异构体,可以用还原法制得三种二甲苯,它们的熔点分别如下:
|
六种溴二甲苯的熔点/℃ |
234 |
206 |
213 |
204 |
214 |
205 |
|
对应还原二甲苯的熔点/℃ |
13 |
-54 |
-27 |
-54 |
-27 |
-54 |
由此可推断熔点为234℃的分子的结构简式为 ,熔点为-54℃的分子的结构简式为 。
解析:对于数据题首先应该分析数据,找出规律。本题中第一行给出六种物质的熔点,而还原后只有3个熔点数据,其中熔点为206℃、204℃、205℃的三种溴二甲苯还原后得到同一种二甲苯,其熔点为-54℃;熔点为213℃和214℃的两种二甲苯还原后也得到同一种熔点为-27℃的二甲苯,由此说明,有一种二甲苯的苯环上的一溴代物有三种,有一种二甲苯的一溴代物有两种,当然剩下的一种二甲苯的一溴代物只有一种。这样就把问题转化成了判断二甲苯的一溴化物的同分异构体数目。二甲苯有三种:邻二甲苯,间二甲苯,对二甲苯,它们对应的一溴二甲苯的结构简式如下:
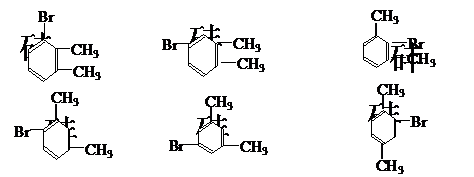
所以,有三种一溴二甲苯的是间二甲苯,只有一种一溴二甲苯的是对二甲苯。
答案:
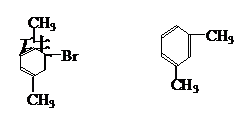
[例4]实验室用如图所示装置进行苯与溴反应的实验,请回答下列问题。
(1)若装置中缺洗气瓶,则烧杯中产生的现象无法说明苯与溴的反应是取代反应,理由是:
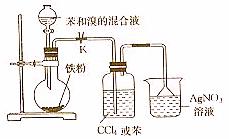
(2)反应后得到的粗溴苯中溶有少量的苯、溴、三溴苯、溴化铁和溴化氢。可通过以下操作除去:①水洗;②碱洗;③水洗;④干燥;⑤……。其中,操作②碱洗的目的是
完成操作④干燥后,接下来的操作⑤是 (填操作名称)
(3)如果省略(2)中的操作①,一开始就进行碱洗,会对后面的操作造成什么影响?(简要说明理由)
解析:若装置中缺洗气瓶,则挥发出的溴蒸气进入AgNO3溶液中生成AgBr沉淀,无法确定溴与苯反应有HBr生成。粗溴苯中含溴、FeBr3、HBr,苯等杂质,所以水洗目的是除去FeBr3、HBr,用碱洗的目的是除去溴及未除净的HBr,再水洗的目的是除去生成的NaBr、NaBrO,接下来干燥是除去其中的水分,再接下来是除去苯,所需操作为蒸馏。很显然,一开始用碱洗的后果会生成Fe(OH)3沉淀,而使分离较难。
答案:(1)溴与AgNO3溶液反应生成AgBr沉淀,无法确定溴与苯反应有HBr生成
(2)除去粗溴苯中的溴和溴化氢;蒸馏(或分馏)
(3)先用碱洗,溴化铁与碱反应生成Fe(OH)3沉淀,很难分离。
[模拟试题]
1、具有单双键交替长链(如: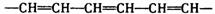 …)的高分子有可能成为导电塑料。2000年诺贝尔(Nobel)化学奖即授予开辟此领域的3位科学家。下列高分子中可能成为导电塑料的是:
…)的高分子有可能成为导电塑料。2000年诺贝尔(Nobel)化学奖即授予开辟此领域的3位科学家。下列高分子中可能成为导电塑料的是:
A、聚乙烯 B、聚丁二烯 C、聚苯乙烯 D、聚乙炔
2、若1mol气态烃能和2molHCl加成,而加成产物又可以和8mol氯气完全取代。则该烃是:
A、2-甲基丙烯 B、乙炔 C、1,3-丁二烯 D、丙炔
3、某单炔烃,氢化后的产物结构简式为: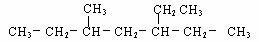 ,则该烃可能有的结构有:
,则该烃可能有的结构有:
A、1种 B、2种
C、3种 D、4种
4、下列混合物,不论它们按何种比例混合,只要质量一定,经完全燃烧后产生的CO2和H2O的物质的量均为常数的是:
A、乙炔和苯 B、甲烷和乙烷 C、乙烯和丁炔 D、苯和苯乙烯
5、用相对分子质量为43的烷基取代甲苯苯环上的1个氢原子,所得芳香烃产物的数目为:
A、3 B、4 C、5 D、6
6、在(CH3COO)2Zn存在的条件下,乙炔可以与乙酸作用生成CH2=CHOOCCH3。该反应的反应类型是:
A、加成反应 B、酯化反应 C、消去反应 D、缩合反应
7、乙烯基乙炔(CH2=CH-C≡CH)是一种重要的不饱和烃,其分子里最多在同一条直线上和最多在同一个平面上的原子数分别是:
A、4、8 B、5、8 C、3、6 D、3、4
8、CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子型碳化物。请通过对CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是:
A、ZnC2水解生成乙烷(C2H6) B、Al4C3水解生成丙炔(C3H4)
C、Mg2C3水解生成丙炔(C3H4) D、Li2C2水解生成乙烯(C2H4)
9、m molC2H2跟n mol H2在密闭容器中反应,当该可逆反应达到平衡时,生成p mol
C2H4。将反应后的混合气体完全燃烧,生成CO2和H2O,所需氧气的物质的量是:
A、(3m+n)mol B、(5/2 m+n/2-3p)mol
C、(3m+n+2p)mol D.(5/2 m+n/2)mol
10、苯环结构中不存在C-C与C=C的简单交替排列结构,可以作为证据的事实是:
①苯不能使酸性KMnO4溶液褪色 ②苯不能使溴水因化学反应而褪色 ③经实验测定只有一种结构的邻二甲苯 ④苯能在加热和催化剂条件下氢化成环己烷 ⑤苯中相邻C原子与C原子间的距离都相等
A、只有①② B、只有④⑤ C、只有①②⑤ D、只有①②③⑤
11、已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如下图:
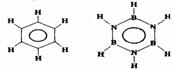
则硼氮苯的二氯取代物 B3N3H4Cl2 的同分异构体的数目为:
A、2 B、3 C、4 D、6
12、在实验室中,下列除去杂质的方法中正确的是:
A、溴苯中混有溴,加入KI溶液,振荡,用直馏汽油萃取,分液
B、硝基苯中混有浓硝酸,加入足量稀NaOH溶液洗涤,振荡,用分液漏斗分液
C、乙烯中含有SO2 ,将其通入装有KMnO4溶液的洗气瓶中进行洗气
D、乙烷中含有乙烯,通入适量的H2在一定条件下反应使乙烯转变成乙烷
13、有三种不同取代基-X、-Y、-Z,当它们同时取代苯分子中的3个氢原子,且每种取代产物中,只有两个取代基相邻时,取代产物有:
A、2种 B、4种 C、6种 D、8种
14、已知C-C可以绕键轴旋转,对于结构简式如下图所示的烃,下列说法正确的是:
A、分子中至少有10个碳原子处于同一平面上
B、分子中至少有9个碳原子处于同一平面上
C、该烃的一氯取代物最多有4种
D、该烃是苯的同系物
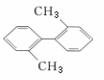
15、在苯的同系物中,加入少量酸性高锰酸钾溶液,振荡后溶液褪色。如甲苯发生上述反应时生成苯甲酸(C6H5COOH),对此解释正确的是:
A、苯的同系物分子中碳原子数比苯分子中碳原子数多
B、苯环受侧链影响而易被氧化
C、侧链受苯环影响而易被氧化
D、由于苯环和侧链的相互影响,使苯环和侧链同时被氧化
16、气体A只含X、Y两种短周期元素,X的原子序数大于Y的原子序数。B、D、E是中学化学中常见气体。固体乙为某金属氧化物,F为某金属单质。各物质有如图所示的转化关系:
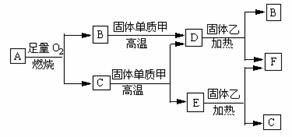
试回答下列问题:
(1)若气体A中,X与Y的质量比小于3,则气体A中肯定有(写化学式) ;
(2)若气体A的分子为线型结构,且X与Y两元素的质量比数值上等于X的相对原子质量,则X元素位于周期表 周期, 族,A的电子式为 。
(3)C与固体甲在高温下反应的化学方程式为 。
17、烷基取代苯 R可以被KMnO4的酸性溶液氧化生成
R可以被KMnO4的酸性溶液氧化生成 COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到
COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到 COOH。现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为
COOH。现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为 COOH的异构体共有7种,其中的3种是:
COOH的异构体共有7种,其中的3种是: CH2CH2CH2CH2CH3
,
CH2CH2CH2CH2CH3
,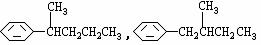
请写出其他4种的结构简式:
, ,
, 。
18、某同学设计如图所示实验装置粗略测定电石中碳化钙的质量分数。
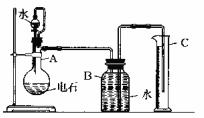
(1)烧瓶中发生反应的化学方程式是 ,装置B和C的作用是 。烧瓶要干燥,放入电石后应塞紧橡皮塞,这是因为 。
(2)所用电石质量不能太大,否则 ,若容器B的容积为250mL(标准状况)则所用电石质量为 g.
(3)漏斗与烧瓶之间的玻璃导管连接,其目的是 。
(4)实验中测得排入量筒中水的体积为VmL(换算成标准状况),电石的质量为Wg,则电石中碳化钙的质量分数 (不计导管中残留的水)。
19、某化学课外小组用下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。

(1)写出A中反应的化学方程式:
(2)观察到A中的现象是 。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
(4)C中盛放CCl4的作用是 。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入 ,现象是 。
20、下面是苯和一组稠环芳香烃的结构简式 :
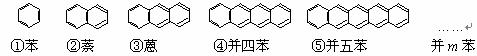
⑴写出化合物②-⑤的分子式:①C6H6 ② 、③ 、④ 、⑤ 。
⑵这类化合物的分子式通式是:C H (请以含m的表示式填在横线上,m=1,2,3,4,5……)。
⑶由于取代基的位置不同而产生的异构现象,称为官能团位置异构,一氯并五苯有 (填数字)个异构体,二氯蒽有 (填数字)个异构体。
21、两种气态链烃的混合气体1体积完全燃烧后得到3.6体积二氧化碳和3体积水蒸气(气体体积均在同温同压下测定)。已知两种烃都能使溴水褪色,且碳原子数均小于5。
(1)分析判断两种烃各是哪一类?
(2)通过计算和推理,确定这两种烃的分子式以及混合气体中的体积比。
22、某种苯的同系物0.1mol完全燃烧,生成的气体通过浓硫酸,使浓硫酸增重10.8g,再通过NaOH溶液,气体减轻39.6g。这种苯的同系物苯环上的一氯代物、二氯代物分别有3种,没有四氯代物。根据以上条件,推断此物质的分子式和结构简式。
(一)乙炔、炔烃:
乙炔是一种无色无味的气体,密度比空气小,不溶于水。乙炔分子中C原子以sp杂化方式与其他原子形成共价键,因此,乙炔的结构式为:H-C≡C-H,分子中每个原子都处于同一条直线上,键角为180°。但乙炔分子中C≡C小于三倍的C-C单键的键能之和,也小于单键和双键的键能之和,因此乙炔的性质也比较活泼,能与X2、HX等物质发生加成反应,也能被酸性KMnO4溶液等强氧化剂所氧化。
乙炔的化学性质:
①与X2、HX和H2O等物质的加成反应
②燃烧与酸性KMnO4溶液作用使其褪色
③在一定条件下,乙炔还能发生聚合反应:如三聚可得到苯,或发生加聚反应,生成高分子化合物聚乙炔等
乙炔的实验室制法: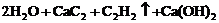
说明:
1、炔烃的结构与乙炔的结构相似,分子中都存在C≡C,C≡C含一个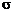 键和2个π键,与C≡C直接相连的原子处于同一条直线上,其不饱和度为2;
键和2个π键,与C≡C直接相连的原子处于同一条直线上,其不饱和度为2;
2、C=C与H2加成时,完全加成的物质的量之比为1:1,而C≡C与H2加成时,完全加成时的物质的量之比为1:2;
3、二烯烃(含两个C=C)与炔烃的通式相同,两者互为同分异构体。二烯烃与X2、H2加成时,有多种可能,可以加成一个C=C,也可以加成两个C=C;若是共轭二烯,则还可以发生1,4加成等;
4、实验室制取乙炔时,为得到平缓的乙炔气流,用块状电石代替粉末状电石,用饱和食盐水代替水,并用分液漏斗向锥形瓶(或烧瓶)内逐滴加入;生成的乙炔中由于含有H2S、PH3等气体而带有特殊难闻的气味,可通过CuSO4溶液除去。
[例1]描述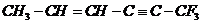 分子结构的下列叙述中,正确的是:
分子结构的下列叙述中,正确的是:
A、6个碳原子有可能都在一条直线上 B、6个碳原子不可能都在一条直线上
C、6个碳原子有可能都在同一平面上 D、6个碳原子不可能都在同一平面上
解析:C=C属于平面型结构,与C=C所直接相连的原子处于同一平面上,C≡C属于直线型结构,与之直接相连的原子处于同一条直线上。同时,由于单键可以旋转,因此CH3、CF3上各有一个H或F原子与双键处于同一平面,因此该结构中肯定共面的原子有8个,其中有6个是碳原子,可能共面的原子有10个;而共线的原子只有4个。故本题的答案为:BC
答案:BC
[例2]1mol某烃最多能与2mol氯化氢发生加成反应,生成氯代烃。1mol该氯代烃能和6mol氯气发生取代反应,生成只含碳元素和氯元素的氯代烃。求该烃的分子式及可能的结构简式。
解析:设该有机物的化学式为CxHy,则有:
CxHy+2HCl→CxHy+2Cl2;CxHy+2Cl2+6Cl2→CxCl8+6HCl,由此可得:
2x+2=8,2+y=6,解得:x=3,y=4,则该烃的化学式为:C3H4,
结构简式为:CH3-C≡CH
答案:C3H4、CH3-C≡CH
炔烃的性质,苯及其同系物的结构与性质
了解乙炔的组成与结构,掌握乙炔的性质及用途;了解炔烃的结构与性质;
了解苯的组成和结构特征,掌握苯及其同系物的化学性质。
炔、苯及其同系物的性质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com