
玻璃仪器洗净的标准是: 内壁上附着的水膜均匀, 既不聚成水滴,也不成股流下。
12.联合制碱法(侯德榜制碱法)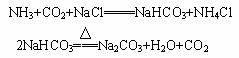
中 学 化 学 物 质 的 俗 名 一 览 表
*为了解部分
|
俗 名 |
化 学 名 称 |
主要成分化学式或结构简式 |
|
|
1、Na 纯碱(苏打) |
碳酸钠 |
Na2CO3 |
|
|
口碱 |
十水合碳酸钠 |
Na2CO3·10H2O |
|
|
食盐 |
氯化钠 |
NaCl |
|
|
*芒硝(朴硝) |
十水合硫酸钠 |
Na2SO4·10H2O |
|
|
小苏打 |
碳酸氢钠 |
NaHCO3 |
|
|
烧碱、苛性钠、火碱 |
氢氧化钠 |
NaOH |
|
|
2、K 灰锰氧 |
高锰酸钾 |
KMnO4 |
|
|
苛性钾 |
氢氧化钾 |
KOH |
|
|
草木灰 |
碳酸钾 |
K2CO3 |
|
|
3、N 碳铵 |
碳酸氢铵 |
NH4HCO3 |
|
|
硫铵 |
硫酸铵 |
(NH4)2SO4 |
|
|
硝铵 |
硝酸铵 |
NH4NO3 |
|
|
王水 |
浓硝酸、浓盐酸 |
HNO3:HCl
(体积比:1:3) |
|
|
4 、Mg
卤 水 |
氯化镁、氯化钙 |
MgCl2,CaCl2 |
|
|
5、Ca
生石灰 |
氧化钙 |
CaO |
|
|
石灰石、大理石 |
碳酸钙 |
CaCO3 |
|
|
熟石灰、消石灰、石灰水 |
氢氧化钙
|
Ca(OH)2 |
|
|
电石 |
碳化钙 |
CaC2 |
|
|
石膏(生石膏) |
二水合硫酸钙 |
CaSO4·2H2O |
|
|
熟石膏、烧石膏、煅石膏 |
一水合二硫酸钙 |
2CaSO4·H2O |
|
|
波尔多液 |
氢氧化钙、硫酸铜 |
Ca(OH) 2,CuSO4 |
|
|
石硫合剂 |
氢氧化钙、硫 |
Ca(OH) 2,S |
|
|
漂白粉 |
次氯酸钙、氯化钙 |
Ca(ClO)2
,CaCl2 |
|
|
6、Ba 重晶石 |
硫酸钡 |
BaSO4 |
|
|
7、*B 硼砂 |
十水合四硼酸钠 |
Na2B4O7·10H2O |
|
|
8、Al *高岭石(粘土) |
铝硅酸盐 |
Al2(Si2O5)(OH)4 |
|
|
*硬铝 |
铝合金 |
含 Cu 4% Mg 0.5% Mn 0.5% Si
0.7% |
|
|
*铝土矿(矾土) |
一水合氧化铝 三水合氧化铝 |
Al2O3·H2O Al2O3·3H2O |
|
|
明矾石(明矾) |
十二水合硫酸铝钾 二十四水合硫酸铝钾 |
KAl(SO4)2·12H2O 或K2SO4·Al2(SO4)3·24H2O |
|
|
刚玉(蓝宝石、红宝石) |
氧化铝 |
Al2O3 |
|
|
*冰晶石 |
六氟合铝酸钠 |
Na3AlF6 |
|
|
9、Si 石英、水晶、石英砂 |
二氧化硅 |
SiO2 |
|
|
水玻璃(泡花碱) |
硅酸钠 |
Na2SiO3或Na2O·SiO2
|
|
|
普通硅酸盐水泥 |
硅酸二钙、硅酸三钙 铝酸三钙 |
2CaO·SiO2,3CaO·SiO2, 3CaO·Al2O3 |
|
|
普通玻璃 |
|
Na2SiO3,CaSiO3,SiO2 |
|
|
正长石 |
|
KAlSi3O8 |
|
|
10、C 干冰 |
二氧化碳 |
CO2 |
|
|
黑色火药 |
硝酸钾、硫、炭粉 |
KNO3,S,C |
|
|
尿素 |
碳酰胺 |
CO(NH2)2 |
|
|
11、Cl 盐酸 |
氢氯酸 |
HCl |
|
|
12、Fe 黄铁矿 |
二硫化亚铁 |
FeS2 |
|
|
磁铁矿 |
四氧化三铁 |
Fe3O4 |
|
|
赤铁矿 |
氧化铁 |
Fe2O3 |
|
|
铁锈 |
水合氧化铁 |
Fe2O3·H2O |
|
|
14、Cu *黄铜矿 |
|
CuFeS2 |
|
|
铜绿 |
碱式碳酸铜 |
Cu2(OH)2CO3 |
|
|
胆矾(蓝矾) |
五水合硫酸铜 |
CuSO4·5H2O |
|
|
15、Zn *皓矾 |
七水合硫酸锌 |
ZnSO4·7H2O |
|
|
*锌钡白(立德粉) |
硫化锌、硫酸钡 |
ZnS,BaSO4的混合物 |
|
|
16、有机物 酒精 |
乙醇 |
C2H5OH |
|
|
电石气 |
乙炔 |
CH≡CH |
|
|
TNT(梯恩梯) |
三硝基甲苯 |
C6H2(NO2)3CH3 |
|
|
天然气、沼气、坑气 |
甲烷 |
CH4 |
|
|
木精 |
甲醇 |
CH3OH |
|
|
甘油 |
丙三醇 |
C3H5(OH)3 |
|
|
硝化甘油 |
三硝酸甘油酯 |
C3H5(ONO2)3 |
|
|
石炭酸 |
苯酚 |
C6H5OH |
|
|
蚁醛 |
甲醛 |
HCHO |
|
|
蚁酸 |
甲酸 |
HCOOH |
|
|
福尔马林 |
35~40%的甲醛水溶液 |
HCHO |
|
|
醋酸(冰醋酸) |
无水乙酸 |
CH3COOH |
|
|
硬脂酸 |
十八酸 |
CH3(CH2)16COOH 或C17H35COOH |
|
|
软脂酸 |
十六酸 |
CH3(CH2)14COOH 或C15H31COOH |
|
|
油酸 |
顺式十八烯-9--酸 |
CH3(CH2)CH=CH(CH2)7_-- COOH 或C17H33COOH |
|
|
肥皂 |
十八酸钠 |
C17H35COONa |
|
化学实验基本操作复习
18.盛石灰水的试剂瓶→稀盐酸;盛苯酚的试管→酒精或NaOH溶液;盛过FeCl3、FeCl2等的试管→用稀盐酸;做过KMnO4分解实验的试管→浓盐酸;做过碘升华实验的试管→有机溶剂;做过银镜反应实验的试管→稀硝酸;熔化过硫的试管→CS2或热的NaOH溶液;有油污的试管→用热碱液洗涤。洗涤原则是将污染物反应掉或溶解掉。
19中学化学涉及的重要的化工生产反应
(1)煅烧石灰石
(2)水煤气的生产
(3)盐酸的生产:氢气在氯气中燃烧
(4)漂白粉的生产:将氯气通入石灰乳中
(5)硫酸的生产(接触法):
(6)晶体硅的生产
(7)玻璃的生产:工业上用纯碱、石灰石和石英为原料来生产普通玻璃。

(8).合成氨生产:高温、高压、催化剂条件下
(9)、工业生产硝酸(氨氧化法)
(10) 氯碱工业:电解饱和食盐水
(11).金属的冶炼:钠的冶炼: 镁的冶炼:铝的冶炼:铁的冶炼:
17. 由于空气中CO2的作用而变质的物质:
生石灰、NaOH、Ca(OH)2溶液、Ba(OH)2溶液、NaAlO2溶液、水玻璃、碱石灰、漂白粉、苯酚钠溶液、Na2O、Na2O2;
14. 与氢气加成的:苯环结构(1:3)、碳碳双键、碳碳叁键 、醛基。酸、酯中的碳氧双键不与氢气直接加成。
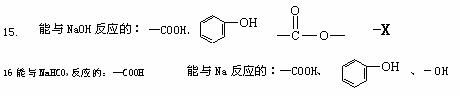
13、可用作致冷剂或冷冻剂的气体:CO2、NH3、N2。用作大棚植物气肥的气体:CO2。
12、含有非极性键的化合物不一定都是共价化合物,如Na2O2、FeS2、CaC2等是离子化合物(阴阳离子个数比是多少?它们的电子式?)。
11、 掌握一图(原子结构示意图)、五式(分子式、结构式、结构简式、电子式、最简式)、六种方程程式(化学方、电离方程式、水解方程式、离子方程式、电极方程式、热化学方程式)的正确书写。
2. 油脂、淀粉、苯酚钠、明矾、Al2S3、Mg3N2、CaC2等一定条件下的水解反应
3 同族非金属元素的氢化物熔沸点从上到下增大,含氢键的NH3、H2O、HF反常。
4 常温下呈气态的有机物:碳原子数小于等于4的烃、一氯甲烷、甲醛。
5 熔沸点比较规律:原子晶体>离子晶体>分子晶体,金属晶体差异较大。
6 原子晶体熔化只破坏共价键,离子晶体熔化只破坏离子键,分子晶体熔化只破坏分子间
作用力。
7 同类有机物一般碳原子数越大,熔沸点越高,支链越多,熔沸点越低。
同分异构体之间:正>异>新,二甲苯:邻>间>对。
8 易液化的气体:NH3、Cl2 ,NH3可用作致冷剂。
9 苯酚微溶于水(大于65℃易溶),易溶于酒精等有机溶剂。硫与白磷皆易溶于二硫化碳。
10 固体溶解度大多数随温度升高而增大,少数受温度影响不大(如NaCl),极少数随温度升高而变小[如Ca(OH)2]。 气体溶解度随温度升高而变小,随压强增大而变大。
1. 区分元素、同位素、原子、分子、离子、原子团、取代基的概念。正确书写常见元素的名称、符号、离子符号,包括IA、IVA、VA、VIA、VIIA族、稀有气体元素、1-20号元素及Zn、Fe、Cu、Hg、Ag、Pt、Au等。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com