
23.(5分)
(1) 坩埚(1分) 4(2分) (2) A、C(2分)
22.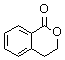 (15分)
(15分)
(1) (2分)
21.(12分)
(1) 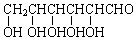 (2分) (2) C3H6O3(2分) (3)
(2分) (2) C3H6O3(2分) (3)
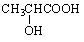 (2分)
(2分)
(4) ①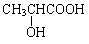
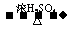 CH2
= CHCOOH + H2O(3分)
CH2
= CHCOOH + H2O(3分)
②nCH2 = CHCOOH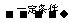
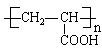 (3分)
(3分)
20.(11分)
(1) H2O(1分) H2O分子间可以形成氢键(1分) 角型或折线型(1分)
(2) CH4(1分) Si(1分 ) (3) 30(2分) (4) 石墨(1分) KC8(3分)
) (3) 30(2分) (4) 石墨(1分) KC8(3分)
25. (8分) 已知有机物A的相对分子质量不超过200。取1.48 g A完全燃烧后,将燃烧产物通过碱石灰,碱石灰的质量增加2.12g;若将燃烧产物通过浓硫酸,浓硫酸的质量增加0.36 g;取1.48 g A与足量钠反应,生成的气体在标准状况下的体积为0.336L。
(1) 1.48 g A完全燃烧生成的CO2的物质的量为________mol。
(2) A的分子式为_______________。
(3) A能使紫色石蕊试液变红,且A经催化氧化后分子中只有一种氢原子,则A的结构简式为_____________。
(4) 将a g A完全燃烧后的产物全部通入足量的Na2O2固体充分吸收,则固体质量增加
____________g 。
。
(命题人:曹 健 审题人:蒋邦龙)
 (6)
(6) 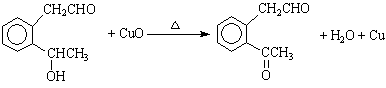 (3分)
(3分)
24.  (14分) 某兴趣小组同学在实验室用加热l-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,并检验反应的部分副产物,设计了如下装置,其中夹持仪器、加热仪器及冷却水管没有画出。
(14分) 某兴趣小组同学在实验室用加热l-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,并检验反应的部分副产物,设计了如下装置,其中夹持仪器、加热仪器及冷却水管没有画出。
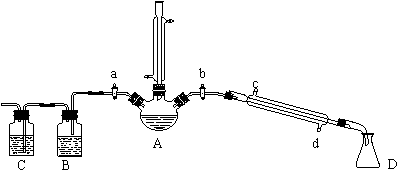 请根据实验步骤,回答下列问题:
请根据实验步骤,回答下列问题:
(1) 关闭a和b、接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷。竖直冷凝管的作用是_____________________。
(2) ①理论上,上述反应的副产物可能有:丁醚、________________(填结构简式)、溴化氢、硫酸氢钠、水等。
②熄灭酒精灯,在 竖直冷凝管上方塞上塞子、打开a,利用余热
竖直冷凝管上方塞上塞子、打开a,利用余热 继续反应直至冷却,通过B、C装置检验部分副产物。B、C中应盛放的试剂分别是__________;___________
继续反应直至冷却,通过B、C装置检验部分副产物。B、C中应盛放的试剂分别是__________;___________
③有同学通过某仪器鉴定所得产物中含有“-CH2CH2CH2CH3”, 从而确定副产物中存在丁醚。该同学的观点___________(填“正确”或“错误”)原因是____________
_______________________________________。
(3) 为了进一步分离、提纯1-溴丁烷,该兴趣小组同学查得相关有机物的有关数据如下:
请你补充下列实验步骤,直到分离出1-溴丁烷。
|
物质 |
熔点/℃ |
沸点/℃ |
|
1–丁醇 |
– 89.5 |
117.3 |
|
1–溴丁烷 |
– 112.4 |
101.6 |
|
丁醚 |
– 95.3 |
142.4 |
|
1–丁烯 |
– 185.3 |
– 6.5 |
①待烧瓶冷却后,拔去竖直的冷凝管;
②插上带橡皮塞的温度计;
③______________________;
④接通冷凝管的冷凝水,使冷水从________处流入;
⑤迅速升高温度至____________℃收集所得馏分。
(4) 若实验中所取1–丁醇、NaBr分别为7.4 g、13.0 g(浓H2SO4足量),蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6 g 1–溴丁烷,则1–溴丁烷的产率是____________。
23. (5分)《硫酸铜晶体里结晶水含量的测定》是中学化学中的一个重要实验,请回答下列该实验的相关问题。
(1) 实验中能直接加热的仪器名称为____________;进行的称量操作至少为________次。
(2) 下列操作会引起测定结果偏高的是__________________
A.加热时温度过高CuSO4发生分解 B.加热后在空气中冷却再称量
C.加热过程中有晶体溅出 D.晶体部分风化
22. (15分) 芳香族化合物甲、乙、丙、丁互为同分异构体,其分子式为C9H8O2,有关的转化关系如下图所示。已知:甲、乙、丁分子中无甲基,0.1 mol D与足量的NaHCO3反应,生成标准状况下的气体4.48 L。

提示:①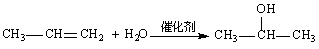
②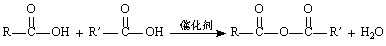
(1)
甲的结构简式为
 。
。
(2) A→乙的反应类型属于 反应,下列有机物中与C 互为同系物的是 。
a.OHC-(CH2)4-COOH b.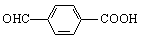
c.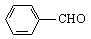 d.
d.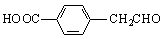
(3) 写出下列反应的方程式(有机物用结构简式表示)
B→丙 ;
丁→F反应 ① 。
(4)
X是E的同分异构体,X遇FeCl3溶液显色,能与NaHCO3反应, 1 mol X与足量的Na反应生成1 mol H2,X分子中苯环上只有两个取代基(不含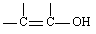 结构),则X的结构简式为
(任写一种)。
结构),则X的结构简式为
(任写一种)。
(5)
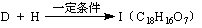
 ,满足该条件的I共有
种
,满足该条件的I共有
种
21. (12分) 某有机物A是葡萄糖在人体内的一种代谢产物,与甲醛具有相同的实验式,相对分子质量为90,A具有酸性,能分别与浓硫酸在一定条件下生成有机物B或C,B是一种六元环状化合物,C能够使溴水褪色且在一定条件下可以生成高聚物D。
请回答下列问题:
(1) 葡萄糖的结构简式为__________________。
(2) A的分子式为______________。
(3) A的结构简式为______________。
(4) 写出下列反应方程式:
①A→C______________________________________________________________;
②C→D______________________________________________________________。
20. (11分) 元素周期表反映了元素性质的周期性变化规律。请根据短周期元素在周期表中的位置、结构和相关性质,回答下列问题:
(1) 第VIA族元素形成的气态氢化物中沸点最高的是____________(用分子式表示),原因是____________________,该分子的空间构型为______________。
(2) 第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如表1所示,其中E的化学式为 ;第三周期元素单质的熔点(℃)变化如图a所示,其中h的元素符号为 。 (表1)
|
氢化物 |
A |
B |
HF |
D |
E |
|
沸点/℃ |
1317 |
100 |
19.5 |
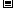 33.35 33.35 |
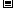 164 164 |
(3) 第二、第三周期的某些元素能形成单质甲和化合物乙,它们具有图b所示的结构单元,甲和乙的晶体类型相同,甲的某种同素异形体与乙在高温时能发生置换反应生成h的单质和CO。若该反应生成的h的单质含有1 mol共价键,则参加反应的乙的质量为_______________g。
(4) 碳元素的某种单质具有平面层状结构,该单质的名称为__________;同一层中的原子构成许多的正六边形,单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图c所示,该物质的化学式为 。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com