
20.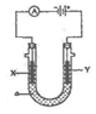 (10分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连。
(10分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连。
(1)若X是锌,Y是碳棒电极,a是饱和NaCI溶液,则①该原理可
制得化工原料有 ;②Y极的电极反应式为
(2)若要用电解方法精炼粗铜,则①电解液a选用 ;②Y电
极反应式是 。(说明:杂质发生的电极反应不必写出)
(3)若要在某铁制小饰品上镀上一层银,则①Y电极的材料是 ;②X电极反应式是 。
19.(7分)
(1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为 (填序号)。
A.9 B.13 C.11-13之间 D.9-11之间
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,混合溶液中c(Na+)
c(CH3COO-)(填“>”、“=”或“<”)。
(3)常温下,已知某NH4Cl溶液中的c(NH4+)=c(Cl一),则该溶液的pH 7(填“>”、“=”或“<”)。
(4)如果将HCl和CH3COONa溶液等浓度、等体积混合,则混合溶液中各离子浓度的大小关系为
18.(6分)下列反应在210℃时达到平衡:
①PCl5(g) PCl3(g)+C12(g) △H1>0 K1=1 mol·L-1
②CO(g)+C12(g) COCl2(g) △H2<O K2=5×104 mol·L-1
③COCl2(g) CO(g)+Cl2(g) K3=?
④2SO2(g)+O2(g) 2SO3(g) △H4<0
(1)反应③的平衡常数K3为 。
(2)要使反应①和反应②的K数值相等,可采取的措施是 (填序号,下同)。
A.降低反应①、②体系中Cl2浓度
B.反应①降低温度,反应②维持210℃
C.反应①、反应②同时升高温度
(3)欲使反应④向正方向移动,可采取的措施是
A.恒温下扩大容器体积 B.减少SO3的物质的量
C.恒压下升温
17.(7分)神舟7号的成功发射,说明我国的空间技术又向前迈进了一步。
(1)发射飞船时肼(N2H4)与NO2作推力能源,两者反应产生氮气和水蒸气。已知:
①N2(g)+2O2(g)=2NO2(g) △H=+67.7 0.1 mol·L-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-5340.1 mol·L-1;
则肼与二氧化氮反应的热化学方程式为:
(2)飞船使用的氢氧燃料电池具有高能、轻便和不污染环境等优点。氢氧燃料电池有酸式和碱式两种,其电池总反应均为:2H2+O2=2H2O。酸式氢氧燃料电池的电解质溶液是强酸溶液,其负极电极反应式可表示为:2H2-4e一=4H+,则其正极反应式为 ;碱式氢氧燃料电池中的电解质溶液是强碱溶液,其正极电极反应式可表示为:O2+2H2O+4e一=4OH一,则其负极反应式为
16.在0.1 mol·L-1Na2CO3溶液中,下列关系正确的是 ( )
A.c(Na+)>c(CO32一)>c(OH一)>c(HCO3一)>c(H+)
B.c(Na+)+c(H+)=c(HCO3一)+c(CO32-)+c(OH一)
C.c(Na+)>c(CO32一)>c(HCO3-)>c(H+)>c(OH一)
D.c(HCO3一)+2c(CO32一)+c(H2CO3)=0.1 mol·L-1
15.目前科学家已开发出一种新型燃料电池一固体氧化物电池,该电池用辛烷(C8H18)作燃料,电池中间部分的固体氧化物陶瓷可传递氧离子。下列说法正确的是 ( )
A.电池工作时,氧气发生氧化反应
B.电池负极的电极反应为:O2+2H2O+4e一=4OH-
C.电池负极的电极反应为:C8H18+25O2-一50e一=8CO2+9H2O
D.若消耗的O2为11.2 L(标准状况),则电池中有1 mol电子发生转移
14. 一定量的混合气体在密闭容器中发生反应为:aM(g)+bN(g) cw(g),达平衡后测得M气体的浓度为0.5 mol·L-1。其它条件不变将密闭容器体积扩大1倍,再达平衡时测得M的浓度为0.3mol·L-1则下列叙述正确的是 ( )
一定量的混合气体在密闭容器中发生反应为:aM(g)+bN(g) cw(g),达平衡后测得M气体的浓度为0.5 mol·L-1。其它条件不变将密闭容器体积扩大1倍,再达平衡时测得M的浓度为0.3mol·L-1则下列叙述正确的是 ( )
A.反应速率增大 B.平衡向右移动
C.N的转化率提高 D.W的体积分数降低
13.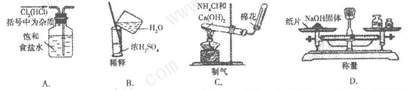 实验是化学研究的基础,下图中所示的实验方法、装置或操作正确的是 ( )
实验是化学研究的基础,下图中所示的实验方法、装置或操作正确的是 ( )
12. 在密闭容器中,反应:CH4(g)+H2O(g) CO(g)+3H2(g)△H>0,达到平衡状态。下列叙述正确的是 ( )
在密闭容器中,反应:CH4(g)+H2O(g) CO(g)+3H2(g)△H>0,达到平衡状态。下列叙述正确的是 ( )
A.增加甲烷的量,上式中△H增大
B.增大水蒸气的量,可提高水蒸气的转化率
C.升高温度,逆反应速率增大,正反应速率减少
D.增大体系压强,该反应的化学平衡常数不变
11.实验室要保存下列试剂:①醋酸钠溶液②氧化钠溶液③硝酸钠④碳酸钠溶液⑤氯化铝溶液,其中不能盛放在带磨口玻璃塞的试剂瓶中的是 ( )
 A.①和③ B.①和④ C.①和④ D.④和⑤
A.①和③ B.①和④ C.①和④ D.④和⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com