
9.在硫酸的工业生产中,下列生产操作及对生产操作主要原因的说明二者都正确的是
A.从沸腾炉出来的炉气需净化,因为炉气中SO2会与杂质反应
B.硫铁矿燃烧前需要粉碎,因为大块的不能燃烧
C.SO3用98.3%的浓H2SO4吸收,目的是防止形成酸雾,以使SO3吸收完全
D.SO2氧化为SO3时需使用催化剂,这样可以提高SO2的转化率
8.将三氧化硫溶解在硫酸中所得到的混合物称为“发烟硫酸”,通常以三氧化硫的质量分数表示其组成。将 0.1185 g发烟硫酸试样溶于水,用 0.125 mol·L-1的NaOH标准溶液滴定。用去此标准溶液20 mL,恰好中和,则试样中SO3的质量分数为
A.15% B.17% C.34% D.60%
7.某温度下CuSO4的溶解度为25 g,若温度不变,将32 g无水CuSO4粉末撒入m g水中,形成饱和溶液并有CuSO4·5H2O晶体析出时,m的取值范围是
A.18 g≤m≤128 g B.36 g<m<180 g
C.18 g<m<128 g D.36 g≤m≤180 g
6.各取pH=2的H2SO4和H2SO3溶液350 mL,分别稀释5倍后,再分别加入0.1 g Zn,在相同条件下让它们充分反应,则
A.两者放出H2体积一样
B.H2SO4放出的H2比H2SO3放出的H2体积小
C.H2SO4放出的H2比H2SO3放出的H2体积大
D.H2SO4的反应速率比H2SO3的反应速率快
5.利用废铜屑制取CuSO4溶液最好的方法是
A.铜屑和浓硫酸混合加热
B.铜屑在空气中燃烧后再溶于稀H2SO4
C.铜屑与稀硫酸混合加热
D.铜屑在空气中灼烧后再溶于浓H2SO4
4.在200 mL 0.5 mol·L-1 NaOH溶液中,加入一定量SO3,在一定条件下蒸发所得溶液,析出的固体物质只有5.0 g,该固体物质的成分可能是(固体物质均不含结晶水)
A.Na2SO4 B.NaHSO4
C.NaOH和Na2SO4 D.Na2SO4和NaHSO4
3.向50 mL 18 mol/L硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量(n)为
A.n=0.9 mol B.0.45 mol<n<0.9 mol
C.n=0.45 mol D.n<0.45 mol
2.已知98%的浓H2SO4的浓度为18.4 mol/L,则49%的硫酸溶液的浓度为
A.9.2 mol/L B.大于9.2 mol/L
C.小于9.2 mol/L D.不能确定
1.下列四种溶液中,一定存在SO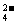 的是
的是
A.向甲溶液中加入BaCl2溶液,产生白色沉淀
B.向乙溶液中加入BaCl2溶液,有白色沉淀,再加入盐酸沉淀不溶解
C.向丙溶液中加入盐酸使之酸化,再加入BaCl2溶液,有白色沉淀产生
D.向丁溶液中加入硝酸酸化,再加入硝酸钡溶液,有白色沉淀产生
7.5×105mol×22.4L·mol-1)×10-3m3·L-1÷(5000m3/台×21%)=16台。
(3)硫充分燃烧后,混合气体中氧气的体积至少要保证反应SO2+1/2O2≒ SO3所需的氧气。设S燃烧生成的二氧化硫为1体积,则需消耗氧气1体积;催化氧化为三氧化硫需氧气0.5体积;空气带入的氮气为1.5体积×79/21=5.64体积,故混合气体中ф(O2)=(0.5/0.5+1+5.64) ×100%=7%(下限)
(4)实际安装送风机台数略多于理论数的原因是:增大空气(氧气)的量,有利于平衡2SO2+O2 ≒ 2 SO3向右移动,从而提高二氧化硫的转化率。但过分增加空气的量,会带走热交换器的热量,降低反应的速率,不利于工业生产。
评注:本题涉及到化工生产的反应原理、条件控制及计算,具有一定的开放性和研究性,代表了新教材的新理念。
例9.“绿色化学”要求从技术上、经济上设计可行的化学反应,使其尽可能减少对环境的负作用。下列化学反应中,不符合绿色化学概念的是
A.用氨水吸收硫酸厂的尾气:SO2+2NH3+H2O=(NH4)2SO3
B.除去硝酸工业尾气中的氮氧化合物:NO2+NO+2NaOH=2NaNO2+H2O
C.制硫酸铜:Cu+2H2SO4=CuSO4+SO2↑+2H2O
D.制硫酸铜:2Cu+O2=2CuO CuO+H2SO4(稀)=CuSO4+H2O
[解析]绿色化学是人类与自然和谐发展的化学,是21世纪化学发展的目标和方向。绿色化学要求我们尽可能研究和寻找能充分利用的无毒害原料,最大限度地节约能源,在工业生产各个环节都争取做到净化和无污染。它要求我们在化工生产中充分考虑催化剂和载体的重复使用,全面回收未反应的原料、助溶剂、稳定剂等物质,拒绝使用无法替代、无法回收、无法再生或不能重复使用的有明显污染的物质,努力做到没有“三废”的排放。在选项A、B、D 中,每一种物质都得到了充分的利用,而且均没有污染产生,但在选项C中,2mol硫酸只能生成1mol硫酸铜,同时还放出了有毒的二氧化硫气体,所以选项C不符合绿色化学的概念。
答案:C。
例10.随着社会的进步和人民生活水平的提高,环境问题越来越受到人们的关注。下列名词中与环境问题无关的是
①温室效应 ②赤潮 ③酸雨 ④光化学烟雾 ⑤臭氧空洞 ⑥潮汐 ⑦大脖子病 ⑧富营养化 ⑨白色污染
A.②⑥⑦ B.⑥ C.①③⑤ D.⑥⑦⑧
[解析]凡是在环境中产生的能影响人类生活和生产,甚至影响人类生存的种种问题都属于环境问题。环境问题中有一部分是自然原因造成的,但更多的是人为因素造成的,如滥采滥用自然资源,任意排放有害物质或不正确地使用化肥、农药,城市人口迅速膨胀而造成的垃圾、污水、噪音、汽车尾气、大型工程建设不当等。
例11.已知氢氧化钙在水中存在下列溶解平衡:Ca(OH)2(s) ≒Ca2++2OH-。在火力发电厂燃烧煤的废气中往往含有二氧化硫、氧气、氮气、二氧化碳等。为了除去有害气体二氧化硫并变废为宝,常常用粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏[CaSO4·2H2O]。
(1)写出上述两个反应的化学方程式:①_____________;②_________________。
(2)试说明用熟石灰的悬浊液,而不用澄清石灰水洗涤废气的理由:________。
(3)在英国进行的一个研究结果表明:高烟囱可以有效地降低地表面二氧化硫的浓度。在二十世纪六七十年代的10年间,由发电厂排放出的二氧化硫增加了35%,但由于建造高烟囱的结果使地面二氧化硫的浓度降低了30%之多。请从全球环境保护的角度,分析这种方法是否可取?答____________________。
[解析](1)①2SO2+O2+2CaCO3=2CaSO4+2CO2
或2SO2+O2+2CaCO3+4H2O=2[CaSO4·2H2O]+2CO2
② 2SO2+O2+2Ca(OH)2=2CaSO4+2H2O
或2SO2+O2+2Ca(OH)2+2H2O=2[CaSO4·2H2O]
(2)氢氧化钙微溶于水,澄清的石灰水中氢氧化钙的浓度小,不利于二氧化硫的吸收。
(3)不可取,因为二氧化硫的排放总量没有减少,进一步形成酸雨仍会造成对全球环境的危害。
评注:工业上处理尾气二氧化硫的方法有多种,在学习这一知识时要注意不要思维定势,要学会多向思考,从二氧化硫是酸性氧化物、具有氧化性和还原性等角度去理解。
实战演练
硫酸工业
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com