
5、如果你是生活在唐朝的商人,你来到长安,能够进行的商贸活动有
①可以到西市与波斯、大食商人进行交易②为了财产安全,你将大部分金银储存在柜坊 ③你通过设在长安的市舶使进行对外贸易④你通过飞钱方法,可以回老家再将钱取出
A.②③④ B.①③④ C.①②④ D.①②③
4.清朝中国古代官营手工业代表生产技艺的最高水平的主要原因是
A 统治者的重视 B 工匠积极性高
C 中央集权的作用 D 市场需求
3、某地发现一座古墓,考古人发掘出的随葬文物有以下物品,请判断此古墓的大致年代①丝织品②景德年间瓷罐③唐三彩④哥窑瓷瓶⑤珐琅彩
A、唐朝 B、北宋 C、南宋 D清朝
2.就说明“至迟到春秋末期,我国已经开始用牛耕地”而言,下列论据中说服力最小的是
A.考古发现的反映春秋时期牛耕的文物
B.春秋时期的典籍中出现的“牛”与“耕”结合在一起的人的名字
C.战国初期的典籍中关于春秋时期“宗庙之牺(祭祀用的牛)为畎亩之勤”的记载
D.成书于战国时期的《山海经》中关于“叔均(传说中人物)是始作牛耕”的记载
1、下面图一到图二两则史料的变化可以直接用来论证
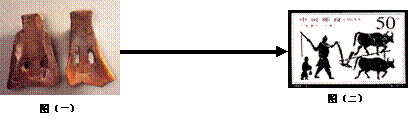
A.我国古代农业经营方式的变化 B.我国古代农业耕作方式的变化
C.我国古代经济结构的变化 D.我国古代手工业技术的进步
12.(2010四川理综卷)标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为p g/ml,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是
A.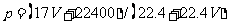 B.
B. 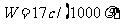
C. 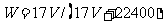 D.C=1000Vρ/(17V+22400)
D.C=1000Vρ/(17V+22400)
答案:A
解析:本题考查基本概念。考生只要对基本概念熟悉,严格按照基本概念来做,弄清质量分数与物质的量浓度及密度等之间的转化关系即可。
7.(2010四川理综卷)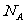 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,22.4L二氯甲烷的分子数约为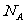 个
个
B.盛有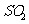 的密闭容器中含有
的密闭容器中含有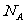 个氧原子,则
个氧原子,则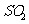 的物质的量为0.5mol
的物质的量为0.5mol
C.17.6g丙烷中所含的极性共价键为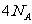 个
个
D.电解精炼铜时,若阴极得到电子数为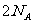 个,则阳极质量减少64g
个,则阳极质量减少64g
答案:B
解析:本题考查微粒数与物质的量、物质的质量等的关系;二氯甲烷在标况下为液态,22.4L不一定为1mol,A项错误;1molSO2中含有氧原子2mol,故含有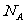 个氧原子的
个氧原子的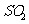 的物质的量为0.5mol,B项正确;17.6g丙烷的物质的量为0.4mol,1mol丙烷中含有极性键8mol,故0.4mol中含有极性键3.2mol,为3.2NA个,C项错误;精炼铜时,阳极为粗铜,当转移2mol电子时,阳极消耗的质量不一定为64g,D项错误。
的物质的量为0.5mol,B项正确;17.6g丙烷的物质的量为0.4mol,1mol丙烷中含有极性键8mol,故0.4mol中含有极性键3.2mol,为3.2NA个,C项错误;精炼铜时,阳极为粗铜,当转移2mol电子时,阳极消耗的质量不一定为64g,D项错误。
5.(2010江苏卷)设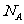 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
A.常温下,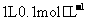 的
的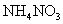 溶液中氮原子数为0.2
溶液中氮原子数为0.2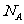
B.1mol羟基中电子数为10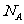
C.在反应中,每生成3mol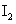 转移的电子数为6
转移的电子数为6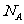
D.常温常压下W W W K S 5 U . C O M
,22.4L乙烯中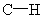 键数为4
键数为4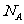
[答案]A
[解析]本题主要考查的是以阿伏伽德罗常数为载体考查如下知识点①考查22.4L/mol的正确使用;②考查在氧化还原反应中得失电子数的计算等内容。A项,无论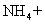 水解与否,根据元素守恒;B项,1mol羟基中有9
水解与否,根据元素守恒;B项,1mol羟基中有9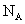 个电子;C项,在该反应中,每生成3mol
个电子;C项,在该反应中,每生成3mol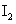 ,转移5
,转移5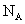 个电子;D项,常温常压下,气体摩尔体积
个电子;D项,常温常压下,气体摩尔体积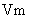 不为22.4L/mol。综上分析得知,本题选A项。
不为22.4L/mol。综上分析得知,本题选A项。
[备考提示]结合阿伏伽德罗常数为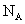 ,判断一定量的物质所含有的某种粒子数目的多少,是高考命题的热点之一,在近几年的各种高考试题中保持了相当强的连续性。这种题型所涉及的指示非常丰富,在备考复习时应多加注意,强化训练,并在平时的复习中注意知识的积累和总结。
,判断一定量的物质所含有的某种粒子数目的多少,是高考命题的热点之一,在近几年的各种高考试题中保持了相当强的连续性。这种题型所涉及的指示非常丰富,在备考复习时应多加注意,强化训练,并在平时的复习中注意知识的积累和总结。
7.(2010上海卷)NA表示阿伏加德罗常数,下列叙述正确的是
A.等物质的量的N2和CO所含分子数均为NA
B.1.7g H2O2中含有的电子数为0.9 NA
C.1mol Na2O2 固体中含离子总数为4 NA
D.标准状况下,2.24L戊烷所含分子数为0.1 NA
答案:B
解析:此题考查了阿伏伽德罗常数知识。阿伏伽德罗常数是指1mol任何微粒中含有的微粒数,等物质的量不一定是1mol,A错;H2O2的相对分子质量为:34,故其1.7g的物质的量为0.05mol,其每个分子中含有的电子为18个,则其1.7g中含有的电子的物质的量为0.9mol,数目为0.9NA,B对;Na2O2固体中,含有的是Na+和O22-两种离子,1mol固体中含有3mol离子,故其中的离子总数为:4 NA,C错;戊烷在标准状况下为液态,故其2.24L不是0.1mol,D错。
易错警示:进行阿伏伽德罗常数的正误判断的主要考查点有:①判断一定量的物质所含的某种粒子数目的多少;②物质的组成;③通过阿伏加德罗常数进行一些量之间的换算等,在解题时要抓住其中的易错点,准确解答。
7.(2010福建卷)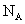 表示阿伏伽德罗常数,下列判断正确的是
表示阿伏伽德罗常数,下列判断正确的是
A.在18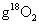 中含有
中含有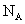 个氧原子
个氧原子
B.标准状况下,22.4L空气含有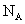 个单质分子
个单质分子
C.1 molCl2参加反应转移电子数一定为2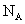
D.含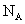 个
个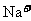 的
的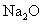 溶解于1L水中,
溶解于1L水中,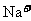 的物质的量浓度为
的物质的量浓度为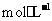
解析:本题考察阿弗加德罗常数的计算和判断
A 18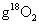 正好是0.5mol,一个氧分子正好含有两个氧原子,所以氧原子的物质的量为1mol,即为1
正好是0.5mol,一个氧分子正好含有两个氧原子,所以氧原子的物质的量为1mol,即为1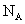
B 空气是混合物
C 在氯气与水的反应中,1molCl2 就只转移1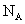 的电子
的电子
D 所得溶液中含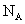 个
个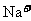 ,可得氢氧化钠的物质的量为1mol,但这时候溶液不是1L,所以物质的量浓度不是1mol/L.
,可得氢氧化钠的物质的量为1mol,但这时候溶液不是1L,所以物质的量浓度不是1mol/L.
答案:A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com