
20.已知A为IIA族的元素,B为IIIA族的元素,他们的原子序数分别为m和n,且A、B为同一周期元素。下列关系式必定错误的是
A.n=m+1 B.n=m+10 C.n=m+11 D.n=m+25
第Ⅱ卷(40分)
19. 合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)
 2NH3(g)(正反应为
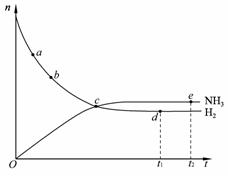
2NH3(g)(正反应为 放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间 t变化的关系如下图所示。下列叙述中,正确的是
放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间 t变化的关系如下图所示。下列叙述中,正确的是
A. 点a的正反应速率比点b的大
B. 点c处正反应速率和逆反应速率相等
C. 点d (t1时刻) 和点 e (t2时刻) 处n(N2)不同
D. 在t2时刻,正反应速率大于逆反应速率
18.实验室中欲加快制取氢气的速率,应采取的措施是 ( )
A.纯锌与稀硫酸反应 B.纯锌与浓硫酸反应
C.含铜、铅等杂质的粗锌与稀硫酸反应  D.粗锌与稀硝酸反应
D.粗锌与稀硝酸反应
17.实验室中用二氧化锰和浓盐酸制氯气,主要操作有:①用药匙向烧瓶中加 二氧化锰,再向分液漏斗中加入浓盐酸,并将导气管放入集气瓶中;②放置酒精灯,根据酒精灯确定铁圈高度,固定铁圈放置石棉网;③将烧瓶固定在铁架台上;④检查装置气密性;⑤装好分液漏斗,连接好导气管。则比较合理的实验操作顺序是(
)
二氧化锰,再向分液漏斗中加入浓盐酸,并将导气管放入集气瓶中;②放置酒精灯,根据酒精灯确定铁圈高度,固定铁圈放置石棉网;③将烧瓶固定在铁架台上;④检查装置气密性;⑤装好分液漏斗,连接好导气管。则比较合理的实验操作顺序是(
)
A.②①④③⑤ B.②③④①⑤ C.②③⑤④① D.①②③④⑤
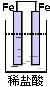
16.以下装置能形成原电池的是( )
A.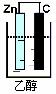 B.
B. C.
C. 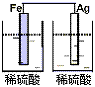 D.
D.
15. X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X与Y组成原 电池时,Y为电池的负极。X、Y、Z三种金属的活动性顺序为
电池时,Y为电池的负极。X、Y、Z三种金属的活动性顺序为
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Y>Z>X
13. 在一定温度下,可逆反应A(g) + 3B(g)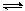 2C(g)
达到平衡的标志是( )
2C(g)
达到平衡的标志是( )
A.C生成的速率与A消耗的速率相等
B.A,B,C的浓度不再变化
C.单位时间生成n mol A,同时生成3n mol B
D.A、B、C、的分子数之比为1 ∶3 ∶ 2
14 .下列关于原电池的叙述中正确的是( )
.下列关于原电池的叙述中正确的是( )
A.正极和负极必须是两种不同的金属
B.原电池是把化学能转化成电能的装置
C.原电池工作时,负极上发生是还原反应
D.锌、铜和盐酸构成的原电池工作时,电子从铜片经导线流向锌片
12.下列措施对增大反应速率明显有效的是 ( )
( )
A.Al在氧 气中燃烧生成A12O3,将Al粉改为Al片
气中燃烧生成A12O3,将Al粉改为Al片
B.Fe与稀硫酸反应制取H2时,改用质量分数为98.3%的浓硫酸
C.Zn与稀硫酸反应时,适当提高溶液的温度
D.Na与水反应时增 大水的用量
大水的用量
11.已知合成氨反应的浓度数据如下:
|
|
N2 + 3H2 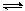 2NH3 2NH3 |
||
起始浓度mol/L |
1.0 |
3.0 |
0 |
|
2秒末浓度mol/L |
0.6 |
1.8 |
0.8 |
当用氨气浓度的增加来表示该化学反应速率时,其速率为( ) A.0.2 mol/(L·s) B. 0.4 mol/(L·s) C.0.6 mol/(L·s) D. 0.8 mol/(L·s)
10.“北大富硒康”中含有微量元素硒(Se),对人体有保健作用。已知硒为第四周期第ⅥA族元素,根据它在周期表中的位置推测,硒不可能具有的性质为( )
A.硒化氢很稳定 B.硒化氢的水溶液显弱酸性
C.非金属性比硫弱 D.其最高价氧化物的水化物酸性强于砷弱于溴
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com