
5. 资源开发:
⑴ 为避免倾倒二氧化碳失败,可将实验进行如下改进,如图17-4。点燃阶梯上蜡烛,从导管中通入二氧化碳,一会儿就可看到下层蜡烛熄灭,然后上面的蜡烛熄灭。当然,通入二氧化碳的速度不可太快,太快蜡烛熄灭的时间差太小,不易分辨。
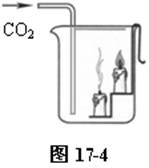
⑵ 证明二氧化碳的密度大,可选用以下实验。
① 如图17-5所示。在铁架台上挂两个纸袋(或塑料袋),调整,其其平衡。向右边的纸袋内倒入二氧化碳,可明显看到杠杆向右侧倾斜。从面证明二氧化碳的密度比空气大。
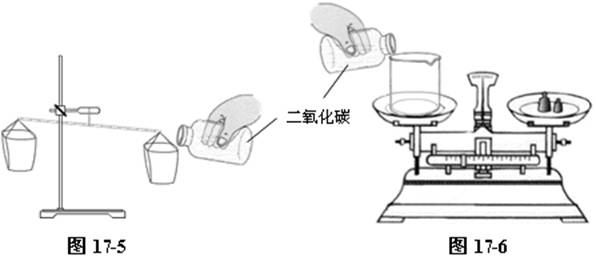
② 如图17-6所示。取一只天平,在天平左边放一只250 mL的烧杯,用砝码平衡。再向烧杯内倒入二氧化碳,可明显看到天平向二氧化碳一侧倾斜。以此证明二氧化碳的密度比空气大。
③ 取一只大的空烧杯(1000 mL以上,也可以用小塑料桶代替),盖上玻璃片,用向上排空气法收集一杯二氧化碳气体备用。
如图17-7,用滴管头醮些洗发精溶液,吹起空气泡,轻轻摆动滴管头,让空气泡落入充满二氧化碳的大烧杯内。空气汽可以二氧化碳中飘浮一段时间。证明二氧化碳的密度比空气大。
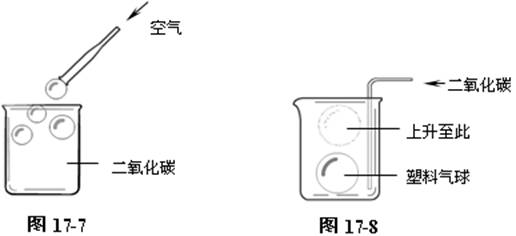
如图17-8所示。还可以用极薄的塑料袋吹成一个小气球,放在大烧杯内,再向烧杯底部能入二氧化碳。气球能缓缓上升到烧杯口部,证明二氧化碳的密度比空气大。
4.探究评价:
⑴ 倾倒二氧化碳的实验需要有一定的经验,不易成功。该实验烧杯容积要适当,过小,倒入的二氧化碳很快充满整个烧杯,导致上下蜡烛几乎同时熄灭。烧杯太大,二氧化碳量不足,下层蜡烛熄灭而上层蜡烛继续燃烧。烧杯宜以150 mL,集气瓶用250 mL为宜。
⑵ 证明二氧化碳溶解性实验效果明显,操作简便,效果很好。
⑶ 二氧化碳与水的反应中,纸花的制作有一定的难度。纸质太软,浸泡时纸张易泡化,纸花不成形,纸质太硬,石蕊在纸花上不易形成较均一的紫色。向纸花上喷酸时,由于喷雾的不均匀,纸花上出现红色斑点,而不是均一的红色。
⑷ 二氧化碳和石灰水反应时,通入二氧化碳的时间要控制好。出现明显的浑浊即停止通入二氧化碳。若继续通入,二氧化碳与碳酸钙继续反应,生成可溶性的碳酸氢钙,溶液又变澄清。

3.探究方案:
⑴ 用铁片弯成一个小阶梯,用酒精灯稍加热。将两支长短相同的蜡烛趁热按在铁片上,待冷却后,蜡烛即固定在铁片上了。将此置于烧杯中。手握集气瓶,将其中新收集的二氧化碳顺烧杯壁缓缓倾倒入烧杯同,可看到小蜡烛由下而上熄灭。如图17-1。由此说明二氧化碳不能燃烧也不能支持燃烧,密度比空气大。
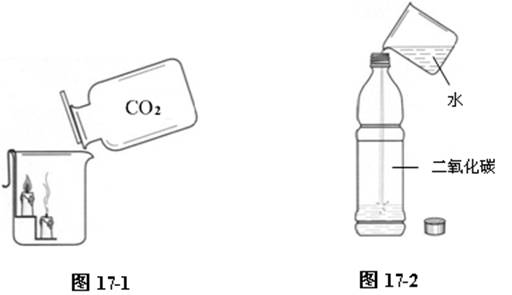
做此实验时,收集的二氧化碳要尽可能满,尽可能纯净。集气瓶用较大的为宜。倾倒时要沿杯壁往下倒,太快上下蜡烛一道熄灭,太慢,下面的蜡烛熄灭了,上面的蜡烛还会继续燃烧。教师最好事先做几次,体验一下倾倒速度。以保证实验的成功。
⑵ 用塑料瓶收集一瓶二氧化碳,倒入约三分之一体积的水,立即旋紧瓶盖,振荡。观察到塑料内陷。如图17-2。证明二氧化碳能溶于水。
⑶ 用吸水性较好且有一度强度的纸折四朵小花,将其完全浸入石蕊试液中,取出晾干后,再浸入石蕊试液中,取出晾干。直到纸花变成明显的紫色为止。
向第一朵小花上喷稀醋酸(或稀盐酸等),纸花变红色。说明石蕊试液遇酸变红色;
向第二朵小花喷水,纸花不变色。说明水不能使石蕊变红色;
将第三朵纸花放入集满二氧化碳的集气瓶中。纸花也不变色,说明二氧化碳不能使石蕊变色。
第四朵纸花先喷水湿润,再放入集满二氧化碳的集气瓶中。纸花变红色。说明此时有酸存在,是二氧化碳与水反应的产物碳酸,如图17-3。
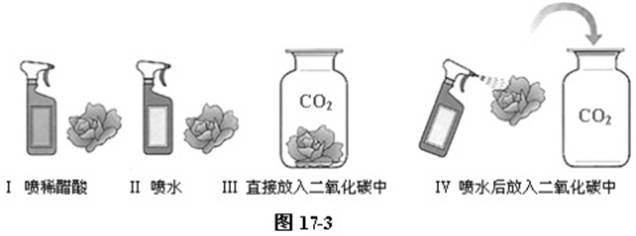
取出第一朵和第四朵变色的纸花,分别放在酒精灯火焰上加热。第一朵纸花不变色,第四朵纸花变紫色。由此说明碳酸不稳定,遇热分解。
⑷ 在试管中取5 mL左右的澄清石灰水,通入二氧化碳,石灰水变浑浊。
2.实验仪器:烧杯、塑料瓶、集气瓶、喷壶、试管等。
实验药品:二氧化碳、蜡烛、石蕊试纸、水、新配制的澄清石灰水等。
1.化学反应原理:
⑴ 一般情况下,二氧化碳不能燃烧也不能支持燃烧,二氧化碳的密度比空气大,是空气密度的1.5倍,故二氧化碳可以灭火。将二氧化碳倾倒入盛有高低不同的两支蜡烛的烧杯中,可见蜡烛由下而上依次熄灭。
⑵ 二氧化碳能溶于水。在集满二氧化碳的塑料瓶中,加入水振荡,二氧化碳溶解,致瓶内压强变小而出现内陷现象。
⑶ 二氧化碳能和水反应,生成碳酸。
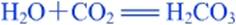
碳酸能使湿润的紫色石蕊试纸变红色。
碳酸很不稳定,受热或浓度较高时易分解。
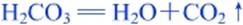
将变红色的石蕊试纸加热,试纸又变成紫色。
⑷ 二氧化碳与石灰水中的氢氧化钙反应,生成难溶性的碳酸钙而使溶液变浑浊。这是室验室检验二氧化碳的常用方法。

6.创新思维:
⑴ 醋酸和纯碱能否用于制取二氧化碳?
不能。
很多资料里都用这种方法作为学生的家庭实验,但笔者做了很多次,效果都很差,反应速率很慢。
⑵ 稀硫酸能否用于制取二氧化碳?
能。
硫酸与块状石灰石或大理石反应时,一开始有大量气泡产生。随着时间的推移,反应速率越来越慢,最后停止。这是由于反应生成了不易溶于水的硫酸钙,阻止了反应的进一步进行。
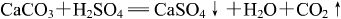
但若将石灰石(或大理石)研成粉末再与稀硫酸反应,则有理想怕反应速度。若稀硫酸的量足够,可保证石灰石(或大理石)反应完全。这是由于石灰石(或大理石)颗粒小,与稀硫酸有很大的接触面积。
但不可用浓硫酸。硫酸浓度大,含水量少。反应后生成的硫酸钙迅速沉淀,使反应立即停止。
⑶ 能否用排水法收集二氧化碳?
二氧化碳能溶于水,在1atm下,1体积水能溶解1体积二氧化碳。这是理论值,并且是饱和状态下的溶解值。二氧化碳溶解达到饱和的需要多长时间呢?
取一支大试管(或50毫升量筒),用排水法收集满二氧化碳,用大拇指堵住试管口取出试管,再倒插入盛有适量水的烧杯中,静置观察,如图16-6。24 h后,试管内液面可升至试管高度的1/2,3-5天内水可充满整个试管。
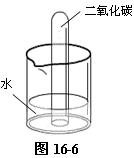
由上述实验可以得出结论,虽然二氧化碳能溶于水,但由于溶解速度是,实验室收集二氧化碳完全可以排水集气法收集。当然,这也应视具体情况,若需收集干燥的二氧化碳,还是用排空气法为宜;收集二氧化碳的量较少时,也不宜用排水法
5. 资源开发:
⑴ 原料选择:
用于制取二氧化碳的药品很多,除大理石和石灰石外,还可以选用的有鸡蛋壳、贝壳等。水泥块和陈旧的石灰块也有较好的制取效果,但由于含杂质较多,反应时,容器中会出现大量的黑色泡沫,外观很不好看。
⑵ 仪器选择:
日常生活中的很多容器都可以用作制取二氧化碳的容器,如矿泉水瓶、牛奶瓶等。
⑶ 制取二氧化碳量较多时,可用如图16-5所示装置制取。
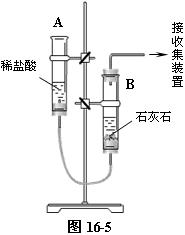
取两支无底的废旧试管,将试管口锉平,一去底部塞上带导管的单孔塞,另一支上下都塞上带导管的单孔塞,并用橡皮管将其连接起来,固定在铁架台上。在A管中加入适量的稀盐酸,在B管中加入石灰石(或大理石)。提起A管,使稀盐酸流入B管内,与石灰石接触反应。不用时,可将A管放低,稀盐酸流入A管内,反应停止。
该装置虽然不是利用启普发生器的原理,但也可以控制反应的进行与停止。
4.探究评价:
⑴ 二氧化碳发生装置的选择是该探究的重点。教材如此安排有利于开发学生的学科能力。教师应引导学生,培养其发散思维,尽可能多地找出发生装置。
⑵ 二氧化碳制取采用上述实验,药品用量少,装置简单,操作方便。但制取的二氧化碳量也少,更换药品很不方便,更不能控制反应的开始与终止。
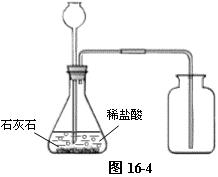
教师实验可采用如下装置。(如图16-4)
3.探究方案:
⑴ 在复习氧气的实验室制法的基础上,归纳出制取气体的发生装置和收集装置选择的思路:
气体的发生装置的选择必须考虑:① 考虑反应物的状态(固态与固态或固态与液态或液态与液态,中学实验中一般不会出现气态与气态物质反应制备气体的情况);② 考虑反应条件(是常温下反应还是加热条件下反应)。
气体的收集装置的选择由气体的性质决定的。不易溶于水的能用排水集气法收集;密度小于空气且不与空气中任何气体反应的用向下排空气集气法收集,密度比空气大且不与空气中任何成分反应的,用向上排空气集气法收集。
⑵ 探究制取二氧化碳的装置。
在上述分析的基础上,教材引导学生从图16-1中选择仪器,组装成制取二氧化碳的实验室装置。其实可选择的仪器远不止这些。
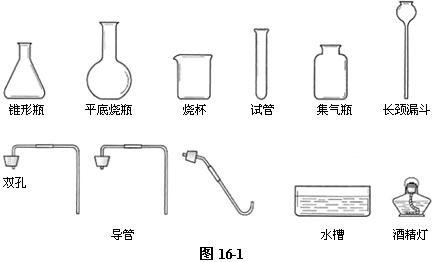
制取二氧化碳用块状固体石灰石(或大理石)与液体稀盐酸反应,因此必须有容器盛装反应物。反应不需要加热,所以该容器的选择范围很大,几乎所有能用带导管的塞子封闭容器口的都可以选择作为该反应的容器。比如试管、锥形瓶、烧瓶、广口瓶,甚至连日常生活中的各种瓶子。
为了使反应开始准备充分后再收集二氧化碳,就有必要在此之前将反应物石灰石(或大理石)和稀盐酸分开。可在装置中加一长颈漏斗或分分液漏斗。若用长颈漏斗,需插入液面以下进行液封,防止气体从长颈漏斗中逸出。还可以选用注射器等,不赘述。
二氧化碳能溶于水,但溶解性不大,1体积水中仅溶解1体积二氧化碳,且溶解的速度比较慢,完全可以用启普发生器器制取。
图16-2是笔者列举的几例制取二氧化碳的装置。可引导学生开动脑筋,还可以找出很多装置。
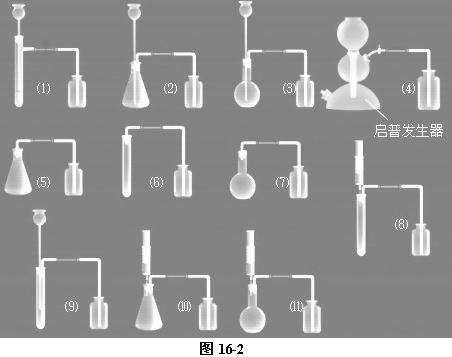
⑶ 制取二氧化碳
学生实验可用最简单的装置。
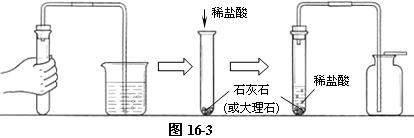
① 检查装置的气密性。装置好装置,用手握住试管,导管另一端插入水中,观察有无气泡产生。
② 在试管内加入适量的石灰石(或大理石),加适量的稀盐酸,塞上带导管的塞子。
③ 用向上排空气法收集气体,用燃着的木条放在集气瓶口试验,若木条熄灭,说明二氧化碳已经收集满。盖上玻璃片,正放在桌面上待用。(如图16-3)
2.实验仪器:试管、烧杯、单孔塞、集气瓶、玻璃片等。
实验药品:石灰石(或大理石)、稀盐酸、澄清石灰水等。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com