
1.化学反应原理
⑴ 氢气可以在氧气(或空气)中燃烧,生成水,放热,产生蓝色火焰。氢气与空气(或氧气)混合,遇明火爆炸。
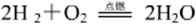
⑵ 氢气具有还原性,可在加热条件下,将氧化铜还原成金属铜。固体由黑色变成紫红色,试管口有水滴出现。

6. 创新思维
⑴ 检验活泼金属和酸反应产生氢气的简单方法:在试管内加入几块锌粒,再加入少量稀硫酸,可以看到锌粒和稀硫酸反应有大量气泡产生,这时用大拇指堵住试管口片刻,松开堵住试管口的大拇指,立刻用燃着的木条点试管中的气体,试管中的气体被点燃,发出尖锐的爆鸣声。
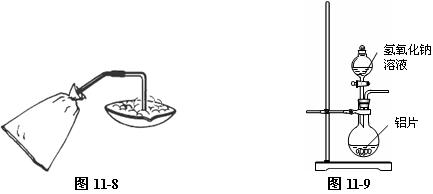
⑵ 2体积氢气跟1体积氧气混合成爆鸣气,它在不遇明火时不会发生爆炸。但遇火则发生强烈爆鸣,用它充填肥皂泡或塑料薄膜袋点火时,会有意想不到的强烈爆鸣,但又十分安全。用塑料薄膜袋把口扎紧在一根连有橡胶管的玻璃管上,先用来储1/3体积氧气,再充2/3体积氢气(最好是先充氧气后充氢气),然后用弹簧夹紧。往预先准备好的盛有肥皂液的蒸发皿内鼓入混合气(如图11-8所示),蒸发皿内会冒起大量气泡。然后移走储气袋。用火柴点燃肥皂泡,会发生震耳的爆鸣声并伴有火光。塑料薄膜储气袋内若有剩余气体,可打开弹簧夹,就着导管口点燃,塑料袋同样“安全”爆破。这后一个实验正好启发同学思考,如果塑料袋换成了玻璃细口瓶该会有怎样的后果?这个实验将使学生牢记,在导管口点燃易燃气体时,一定要先检验它的纯度。
⑶ 利用金属铝和氢氧化钠反应也可制备氢气:

如图11-9所示,在烧瓶中放入铝片和固体氢氧化钠,通过分液漏斗加入水,反应即可发生。由于铝和氢氧化钠反应放热,随着反应的进行,反应速率会越来越快,可以通过滴加水的速度来控制反应速率。
由于氢氧化钠和铝反应时产生热量多,故不适宜用启普发生器制取。
5. 资源开发
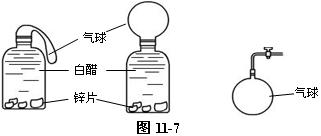
⑴ 用注射器作气体发生装置,适用于制取少量氢气。使用时,先取下注射器的活塞,向针管中加入固体试剂,装上活塞吸入液体试剂,将针尖朝上,推动活塞排出针管中的空气,再将针尖插入橡皮塞密封。使用时,针尖朝上拔掉橡皮塞,推动活塞即可排出氢气。如图11-5。
⑵ 用生活中的很多物品可代替化学仪器做制取氢气实验,材料易得,操作简单,下面仅举二例。
①利用日常生活中容易获得干电池的锌皮、废旧铝制品和酸反应来制取氢气,使用前应将金属材料清洗并将表面的油漆等保护层打磨干净,如用铝制取氢气,应选用稀盐酸,铝和稀硫酸的反应速率比较慢。用小试管作氢气发生,在小试管外套一支略大的试管收集氢气,收集过程中将大试管缓慢向上提起。如图11-6。
② 在较小的塑料牛奶瓶中加入锌片(可从废旧干电池外壳中取得),倒满白醋(主要成分为CH3COOH),在瓶口套上气球,静止,一段时间后,气球胀开,取下气球,伸入一根带玻璃活塞的导管,扎紧气球口,可进行氢气的实验。如图11-7所示。
4. 探究评价
方案⑴装置简单,操作简便,适合学生实验。但由于试管容积小,所能制得氢气量较少,装置不能控制气体的产生与终止。因此教师演示或需要制取较多量氢气时,不宜使用此法。
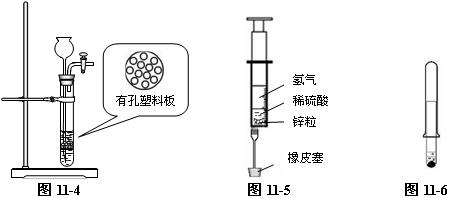
方案⑵制取气体时,可随开随用,随关随停,使用方便,但缺点是需要较多的试剂,更换试剂比较麻烦。为此,可按如图11-4所示改进,其原理与启普发生器相同。这种装置延用了启普发生器即开即用的优点,同时避免了试剂用量多的缺点,是实验制取氢气常好的装置。
3. 探究方案
方案⑴:如图11-1所示,检查装置气密性后,在试管中放入适量锌粒,加入适量稀硫酸(或稀盐酸)塞上塞子,收集氢气。锌跟稀硫酸反应制氢气,如反应速率太慢,可在稀硫酸中加入少量硫酸铜溶液或用稀盐酸代替稀硫酸。
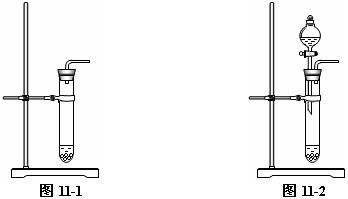
如图11-2所示,可以在上述装置中添加分液漏斗,通过控制添加试剂的速度来控制反应速率,获得较平稳的气流。
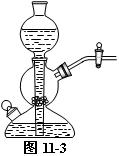
方案⑵:制取较多氢气时,可用启普发生器制取,如图11-3所示。当打开导气管的活塞,球形漏斗中的液体进入容器与窄口上固体接触而产生气体;当关闭活塞,生成的气体将液体压入球形漏斗,使固、液体试剂脱离接触而反应暂行停止,可供较长时间反复使用。启普发生器中的酸液长久使用后会变稀,此时,可把下球侧口的橡皮塞(有的是玻璃塞)拔下,倒掉废酸,塞好塞子,再向球形漏斗中加酸。需要更换或添加固体时,可把装有导管的橡皮塞取下,由中间圆球的侧口加入固体。
使用启普发生器要注意以下几点:
①反应不需条件,而且反应时不能产生大量的热。
②反应物一个是固体(需要块状或粒状,反应时不能变成粉末状),一个是液体。
③生成气体不能是易溶于水的气体。
2. 实验仪器:试管、启普发生器、单孔橡皮塞、双孔子塞、导管、铁架台、分液漏斗、长颈漏斗等。
实验药品:锌粒、稀硫酸或稀盐酸等
1. 化学反应原理
金属锌和稀硫酸反应制氢气:
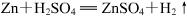 (稀硫酸用1体积浓硫酸跟4体积水混合而成)
(稀硫酸用1体积浓硫酸跟4体积水混合而成)
也可以用金属锌与稀盐酸反应制备氢气:
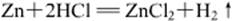 (稀盐酸浓度1∶3)。
(稀盐酸浓度1∶3)。
6.创新思维:
用生活中的红糖制白糖:
称取5 g-10 g红糖放在小烧杯中,加入40 mL水,加热使其溶解,加入0.5 g-1 g活性炭,并不断搅拌,趁热过滤悬浊液,得到无色液体,如果滤液呈黄色,可再加入适量的活性炭,直至无色为止。将滤液转移到小烧杯里,在水浴中蒸发浓缩。当体积减少到原溶液体积的1/4左右时,停止加热。从水浴中取出烧杯,自然冷却,有白糖析出。
5. 资源开发:
⑴ 以上实验都需要比较长的时间,可进行以下改进。
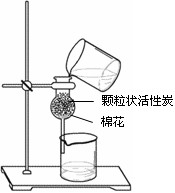
按图14-1所示,在干燥管中放入一小团棉花,再在上方放入适量的颗粒状活性炭,固定在铁架台上。从干燥管上方注入滴有红墨水的溶液,下方立即可收集到无色溶液。效果很好,时间很短,适合课堂演示。
⑵ 制取并收集一瓶氯气:
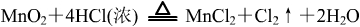
或制取并收集一瓶NO2气体:
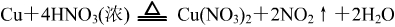
在集气中瓶放入适量的活性炭,用涂有凡士林的玻璃片盖住集气瓶。轻轻振荡,观察。一会儿后,集气瓶中颜色褪出。证明活性炭有很强的吸附性。若有烤过的木炭代替活性炭,也有比较好的实验效果。
4.探究评价:
块状的木炭吸附效果不太理想,往往只能看到的溶液颜色变浅。加之木炭的碎屑不易沉降,使溶液显黑色,不易观察到溶液颜色的改变。
木炭或活性炭暴露在空气中时间较长,往往其吸附已达饱和状态,用此木炭或活性炭实验,效果很差。为此,可将木炭或活性炭先用微火加热较长时间,使其解析后,冷却,研成粉末。将粉末加到红墨水的溶液中,振荡后,过滤。可明显看到溶液由浅红色变无色。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com