
3.探究方案:
⑴ 取出天平,调平衡。待用。
取一块白磷,放入盛水的培养皿中,在水下用小刀切下一粒绿豆大小的白磷,用滤纸吸干表面的水,放入锥形瓶中。(为防止白磷燃烧时,灼裂锥形瓶,可以瓶下事先放入少量的细砂。)将盛白磷的锥形瓶、绑有小气球的玻璃管一起放在天平的左盘中,在右盘添加砝码,并移动游码,使天平平衡。如图13-1所示。
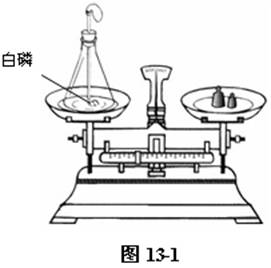
取出锥形瓶及导管,将橡皮塞上的玻璃管放在酒精灯的火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并将白磷引燃。可见白磷燃烧,产生浓厚的白烟。待锥形瓶冷却,白烟沉降后,重新放到托盘天平上,观察天平仍然平衡。
⑵ 在100 mL烧杯中加入约30 mL稀硫酸铜溶液,将几根打磨光亮的铁钉和盛硫酸铜溶液的烧杯一起放在天平上称量,读出读数,记录。如图13-2。
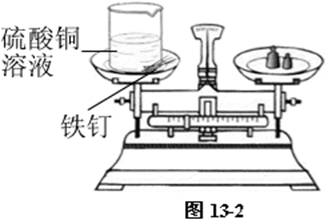
将铁钉浸泡在硫酸铜溶液中,可观察到铁钉表面析出一层紫红色的物质,溶液颜色逐渐变浅。如果时间足够长,可看到溶液的颜色由蓝色变浅绿色。
将反应后烧杯和内容物放到天平上再次称量,读出读数,记录。将两次称量的结果加以比较,质量相等。
2.实验仪器:天平、砝码、锥形瓶、小烧杯、玻璃管、单孔橡皮塞、小气球、酒精灯等。
实验药品:白磷、铁钉(或铁丝)、硫酸铜溶液等。
1.化学反应原理:
⑴ 白磷在密闭的容器内燃烧,生成固体五氧化二磷。
反应前后物质的总质量不变。由此证明质量守恒定律的正确性。
⑵ 铁和硫酸铜溶液反应,生成铜和硫酸亚铁,反应前后,物质的总质量不变。
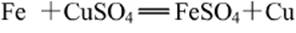
5. 创新思维
由于方案①中采用鼓气扬尘实验的成功率低,将鼓气扬尘变成敲击落尘,操作简单,易于掌握。为了防止蜡烛在罐体振动时翻倒,用中心挖洞的泡沫塑料板固定蜡烛,取一只带盖且密封性良好的金属罐(如奶粉罐),将一个纱布袋绑在罐盖下方,要求留一个口便于添加面粉。把3-4药匙的面粉装入纱布袋中,用坩埚钳夹住燃烧的火柴点燃蜡烛,待烛火燃得较旺时盖上塑料盖,然后用木棒敲击罐盖。如图20-3。
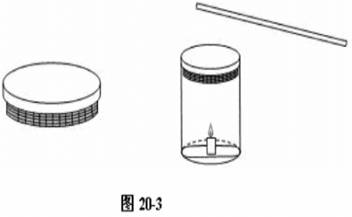
改进后的实验不仅成功率很高,而且除了听到“嘣”的爆破声,看到罐盖被高高掀起,还可以看到火光冲出罐体,直接感受面粉粉尘的燃烧。
在上述实验方案中,也可采用先将面粉吸进导管内(捏瘪洗耳球,将导管的另一端放入盛有淀粉的袋中,松开捏洗耳球的手指,把面粉吸入导管内),然后再吹散的做法,改进后使面粉能最大限度的被吹散,燃烧剧烈、火焰长,利于观察,并且提高了爆炸的成功率高,同时面粉用量少,减少了爆炸后到处飞扬的粉尘。
4. 探究评价
方案①的成功率不高,鼓入空气的速度很难控制。鼓入空气的速度太快有可能将烛火吹灭,扬起的粉尘也太多,可能将烛火扑灭;鼓入空气的速度太慢扬起的粉尘不够,无法剧烈燃烧而爆炸。
方案②实验装置简单,容易制作,材料随手可得,具有实用性、普及性;透明度大、直观性强,实验现象更为明显,不仅能观察到爆炸现象,更能让我们清楚地观察到粉尘的燃烧现象;实验成功率高。
3. 探究方案
方案①:剪去空金属罐和小塑料瓶的上部,并在金属罐和小塑料瓶的底侧各打一个比橡皮管外径略小的小孔。连接好装置,在小塑料瓶中放入面粉,点燃蜡烛,用塑料盖盖住罐(如图20-1所示)。从橡皮管一端鼓入大量的空气(人距离该装置远一些),使面粉充满金属罐,面粉在有限的空间里剧烈燃烧而发生爆炸。
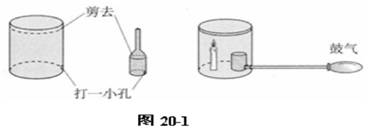
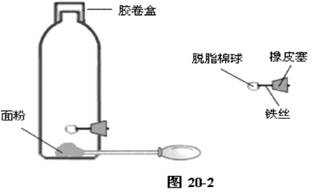
方案②:在饮料瓶的底部打一个孔,孔的大小能插入一根导管,导管的另一端和气囊相连;在瓶壁上打一个较大的孔,孔的大小与橡胶塞一致。在橡皮塞的正中打一个小孔,将一根细铁丝对折绞合在一起后,穿过橡胶塞,在铁丝的前端绞入脱脂棉。将胶卷盒去盖后倒扣在瓶口上,实验器就制作完成了。实验时取适量干燥的面粉于大塑料饮料瓶中,并将胶卷盒倒扣在饮料瓶瓶口上;将带气囊的橡皮管出气口对准瓶中的面粉,并插进粉尘中;拨出橡胶塞,将棉球浸上酒精,点燃酒精棉球并迅速塞进饮料瓶中(如图20-2所示),同时快速按压气囊从橡皮管一端鼓入空气,使饮料瓶中的面粉扬起充满饮料瓶,面粉在饮料瓶中剧烈燃烧而引起爆炸,胶卷盒被高高掀起。
2. 实验仪器:金属罐、小塑料瓶、导管、气囊、胶卷盒(或小塑料瓶)、2 L大塑料饮料瓶、橡皮塞、坩埚钳、铁丝等
实验药品:面粉、蜡烛、脱脂棉、酒精等
1. 化学反应原理
干燥的粉尘遇明火会燃烧,粉尘和空气充分接触时在有限的空间内剧烈燃烧会发生爆炸。
5.资源开发:
⑴ 物质状态的变化,可用碘的升华实验。该实验现象更加明显,对感官的刺激性更强。
先制作一支升华管,在一支一端封口的玻璃管内,放入几粒碘晶体,将玻璃管另一端放在酒精灯外焰上加热熔化,用摄子轻夹熔融的玻璃,使其黏粘在一起,冷却,就制作成了一支封闭的升华管。
用试管夹夹持住升华管上半端,用酒精灯微加热升华管有碘晶体的一端,一会儿后,可观察到有紫色蒸气产生,在玻璃管的另一端,有紫黑色碘晶体形成。如图1-4所示。
该升华管可以反复使用,方便,经济,现象明显。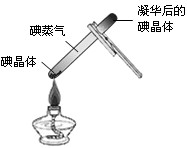
图1-4
⑵ 胆矾研碎不如改用冰糖研碎(无冰糖也可用白砂糖代替)。课前安排学生自带冰糖(或白砂糖)、干净的碗碟和金属汤勺等。实验时取少量的冰糖(或白砂糖)放在碗碟中,用金属汤勺在碗碟中研磨。研碎后,可以亲口尝一尝。此实验可更好地证明糖仅仅是形状发生了改变,并没有生成新的物质。
⑶ 证明有新物质生成的变化,可用镁条燃烧,碳酸氢铵的分解等,比较易于判断有新物质生成。
取一根打磨光亮的镁带,先让学生观察镁条有光亮的银白色,有弹性;再用坩埚钳夹住,在酒精灯上点燃,并迅速放到石棉网的上方,使其继续燃烧。观察到镁条剧烈燃烧,产生耀眼的强光,放出大量的热,并生成白色固体。学生观察所产生的白色固体,并与镁带比较,外观上差异很大,学生较易得出有新物质生成的结论。如图1-5。
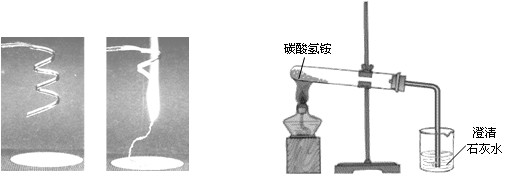
图1-5 图1-6
如图1-6所示,在试管里加入适量的碳酸氢铵晶体,敞口加热。可看到试管口有水滴出现,证明有水生成;同时闻到很强的刺激性气味,证明有氨气产生。再塞上带导管的单孔塞,将导管另一端伸入盛有澄清石灰水的烧杯中,一会儿后,石灰水变浑浊,证明的二氧化碳生成。从面判断,该变化中有新物质生成。
4.探究评价:
这是学生学习化学以来的第一个化学实验,其功效性还在其次,主要是要培养学生对化学学科的学习兴趣。因此,现象明显、生动、新颖更显得重要。
以上四个实验操作都很简单,现象也很明显,特别是对学生感官的刺激是比较强烈的,学生耳目一新。能立即将学生吸引到化学学习的氛围中。
这是学生遇到的第一次化学实验,教师的规范操作对学生影响很大。因此,老师在做以上实验时,一定要注意操作的正确性。本实验涉及到药品装入试管、加热、滴管的使用等多种操作,教师务必重视。
但也正是由于这是学生的第一个化学实验,学生缺乏必要的化学学科知识的基础,还不易判断变化过程中有无新物质生成。实验中生成的氢氧化铜及产生二氧化碳,学生都不易判断出是新的物质,因此教师在实际教学中可以选取一些既贴近学生生活,又能便于学生判断有无新物质生成的事例为好。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com