
1.金属钠能否置换出硫酸铜溶液中的铜?
20.通过“金属和金属材料”和 “燃烧”的复习,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑。在老师的帮助下,用金属钠来探究下列问题:
[问题]
19.下图是实验室常用的实验仪器与装置,根据所学知识回答下列问题:
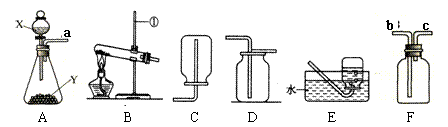
(1)实验室若用B和E装置来制取和收集氧气,发生的反应化学方程式为:
,实验完毕后的操作是:
。
(2)若用A装置制备的气体是氢气,且产生的气体中不含酸性杂质气体,则试剂X常用 ,用图示放置的F装置收集氢气,导管口a应与 (填“b”或“c”)相连。某同学用大小不同的两只试管设计了图甲和乙所示装置来制取少量H2,你认为甲、乙装置中哪一种装置更好__________。
(3)若实验室用A装置制备氧气,Y是黑色粉末,则甲中反应的化学方程式为
。若导管口a和c相连制取并收集氧气,检验气密性后,还须将装置乙 。
(4)若装置A中,X是稀盐酸、Y是石灰石,用A、F两装置组成发生、净化、收集的系列装置,可制得的气体是 。若F中放入饱和NaHCO3溶液,该溶液的作用是除去 ;若F中放入浓硫酸,浓硫酸的作用是 。
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小。NH3极易溶于水,其水溶液呈碱性。
①制取氨气反应的方程式:2NH4Cl + Ca(OH)2 △ CaCl2 + 2NH3↑+ 2X。X的化学式为: 。
②制取并收集NH3,应该从上图中选择的发生装置是 ,收集装置是______。
③NH3是一种碱性气体,干燥时能否选用上述F装置盛装浓硫酸干燥。___________
18.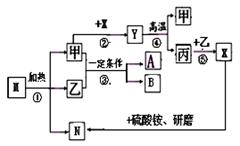 甲、乙、丙都属于氧化物;M是一种不含有金属元素的盐,是常见的化学肥料;A、B是生命活动中不可缺少的物质,其中A属于单质。
甲、乙、丙都属于氧化物;M是一种不含有金属元素的盐,是常见的化学肥料;A、B是生命活动中不可缺少的物质,其中A属于单质。
它们有如下图的转化关系:
(1)写出下列物质的化学式:
M是 ,A是 ,丙是 ;
(2)写出有关反应的化学方程式:
① ,
② ,
⑤ ;
(3)举例说明物质X在生产生活中的应用 (一种即可)。
17.为测定H2SO4与NaOH发生中和反应时放出的热量,在下图的小烧杯中装入一定的NaOH,测量其温度;另取一定量的硫酸,测量
|
试剂 同学 |
使用的 NaOH |
使用的 H2SO4 |
|
甲 |
NaOH固体 |
稀硫酸 |
|
乙 |
NaOH溶液 |
浓硫酸 |
|
丙 |
NaOH溶液 |
稀硫酸 |
其温度,并缓慢地倾入小烧杯中,边加
边用环形玻璃棒搅拌。记录溶液温度的
变化。甲、乙、丙三位同学准备选择右
表中试剂进行实验:
(1)甲、乙、丙三位同学中,有两位
同学选择的试剂是错误的。从溶液温度
改变的因素考虑,指出错误的原因:
① 同学错误的原因是 ;
② 同学错误的原因是 。
(2)写出该中和反应的化学方程式 。
16.铁是人体必需的微量元素之一,没有铁,血红蛋白就不能结合氧分子进行输氧,所以缺少铁元素,人体易患的疾病为 ,医学上经常用硫酸亚铁糖衣片给这种病人补铁。小陈对这种糖衣片产生了兴趣,打算进行探究。
[提出问题]:这种糖衣片中是否含有硫酸亚铁,若有,含量是多少?
[查阅资料]:
①亚铁离子遇具有氧化性的物质时易被氧化。如氢氧化亚铁为白色沉淀,在空气中会迅速被氧化成红褐色的氢氧化铁沉淀,这是氢氧化亚铁的典型特征。 ②亚铁盐溶于水时,会产生少量氢氧根离子而产生沉淀(溶液浑浊)。 ③硝酸具有氧化性。
[实验验证]:
⑴鉴定硫酸亚铁的成分时需加水溶解,加1滴稀盐酸的作用是什么?
能否用稀硫酸代替?_______(填“能”或“不能”)。
⑵为了不影响后续检验亚铁盐,检验硫酸盐可用的试剂是______(选填“A”或“B”)。
A、用硝酸酸化的硝酸钡溶液 B、用盐酸酸化的氯化钡溶液
检验亚铁盐可用的试剂是___________,现象为_______________________________。
⑶含量测定:
①取十粒糖衣片,称其质量为5g,溶于20g水中;溶解药品时要用到玻璃棒,其作用是______________________________。
②向所配溶液中滴加氯化钡溶液至略过量;
证明溶液过量的操作为:静置,向上层清液中滴加__________________溶液,若现象为__________________,则溶液已过量。
③过滤、洗涤沉淀、干燥;
④称量得,沉淀质量为4.66g.试列式计算该糖衣片中硫酸亚铁的质量分数。
[总结反思]:
对硫酸亚铁来说,药片的糖衣可以起的作用是 。
15.通过学习,我们可以从化学的角度看问题。
豆浆机由于快捷方便而进入千家万户。请根据图示回答:
(1)制作材料中的铝合金外壳属于 (填“纯净物”、
“混合物”或“单质”)。铝是活泼金属,而该铝合金外壳
却有较强的抗腐蚀性,原因是(用化学方程式表示)
(2)制作材料中属于有机合成材料的是 (选填一种物质编号);制作手柄的塑料属于 塑料(填“热塑性”或“热固性”);
(3)豆浆已成为众多家庭的早餐饮品,以下是豆浆中一些营养成分的平均质量分数。请根据下表回答:
|
成分 |
水 |
蛋白质 |
脂肪 |
糖类 |
钙 |
磷 |
铁 |
维生素A |
|
质量分数/% |
96.0 |
1.8 |
0.7 |
1.1 |
0.01 |
0.03 |
0.0005 |
0.015 |
①豆浆中含有的微量元素是 ;②青少年缺乏 元素易患有佝偻病。
14.我国科学家侯德榜创造了一种著名的纯碱生产方法-“联合制碱法”。请你回答:
(1)纯碱(Na2CO3)属于
类物质(填“酸”、“碱”或“盐”)。向纯碱的水溶液中滴入酚酞试液,试液变红色,则其pH 7(填“=”、“<”或“>”) 。
。
(2)“联合制碱法”生产过程用化学方程式可简要表示为:
① NH3+CO2+H2O=NH4HCO3 ② NH4HCO3+NaCl=NaHCO3↓+NH4Cl
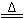 ③ 2NaHCO3 Na2CO3+H2O+CO2↑
③ 2NaHCO3 Na2CO3+H2O+CO2↑
该过程中没有涉及到的基本反应类型是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(3)第②步中加入的是磨细食盐粉。食盐磨细的目的是:

(4)从右图溶解度曲线中,你能获得的信息有:(写出2条)
(5)将第②步所得滤液(NH4Cl与剩余NaCl的混合溶液)
降温,NH4Cl晶体大量析出,而NaCl却仍留在了溶液中。
结合右图,你认为可能原因是:
。
所得NH4Cl属于化学肥料中的 肥,其中氮元素的质量分数为 。(精确到0.1%)
13.在工业、农业以及居民生活中离不开“洗涤”这个问题。请你回答下列问题:
(1)在化学实验室,试管洗涤干净的标志是
(2)关于“油污”的洗涤分析,填空(填序号):
a.有时可用洗涤剂清洗,洗涤剂的作用是( )
b.有时可用汽油清洗,汽油的作用是( )
c.有时可用碱性物质清洗,碱性物质的作用是( )
①与油污反应 ②溶解油污 ③乳化作用
(3)以下各项关于可用“盐酸”洗涤的分析:能用盐酸洗涤的,请写出有关化学方程式,不能用盐酸洗涤的请说明原因。
a.保温瓶内的水垢(主要成分为碳酸钙):
b.玻璃水槽内的铁锈斑:
c.氢气还原氧化铜后试管上的残留物:
d.试管上附着的氢氧化铜固体:
第II卷(非选择题)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com