
20. A. (12分)
(1) 。
(2) 。 。
(3) ,
(4) 。
(5) 。
20. B.(12分)
⑴ , 。
⑵ 。
⑶ , 。
⑷ 。
19.(12分)(1)① 。② , 。
③ 。(2)④ , 。⑤ 。
 ⑥A.
B.
⑥A.
B.
|
实验编号 |
T(℃) |
n (CO)/n(H2) |
|
ⅱ |
|
|
|
ⅲ |
350 |
|
18.(每空2分,共10分)
⑴ 。⑵ 。⑶ 。
⑷ 。
⑸ 。
17.(8分)
(1)① 。② 、 。
(2)
① 。
② 。
③ 。
④ 、 。
16.(8分)
(1) 。
(2) 。
(3) 。
(4) 。
15.(10分)
(1) 。
(2)______________________________________________________________。
(3) 。
(4)_____________________________________________。
_______________________________________________。
(5) 。 ____________。
14.(12分)
(1) 。 (2) (填化学式)。
(3)① (填化学式)。
② 。
③ 。④ 。
13.(11分)(1) ;(2)
(3)B 、D 、E
(4)
(5)
20.  B.(12分)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
B.(12分)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
步骤Ⅰ:称取0.4g花生油样品,置于两个干燥的碘瓶(如图)内,加入10mL四氯化碳,轻轻摇动使油全部溶解。向碘瓶中加入25.00mL含0.01mol IBr的无水乙酸溶液,盖好瓶塞,在玻璃塞与瓶口之间滴加数滴10%碘化钾溶液封闭缝隙,以免IBr的挥发损失。
步骤Ⅱ:在暗处放置30min,并不时轻轻摇动。30min后,小心地打开玻璃塞,用新配制的10%碘化钾10mL和蒸馏水50mL把玻璃塞和瓶颈上的液体冲洗入瓶内。
步骤Ⅲ:加入指示剂,用0.1mol·L-1硫代硫酸钠溶液滴定,用力振荡碘瓶,直至终点。
测定过程中发生的相关反应如下:
①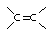 +IBr →
+IBr →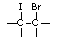 ②IBr+KI=I2+KBr ③I2+2S2O32-=2I-+S4O62-
②IBr+KI=I2+KBr ③I2+2S2O32-=2I-+S4O62-
请回答下列问题:
⑴已知卤素互化物IBr的性质与卤素单质类似,实验中准确量取IBr溶液应用 ,用方程式表示碘瓶必须干燥的原因 。
⑵步骤Ⅱ中碘瓶在暗处放置30min,并不时轻轻摇动的原因是 。
⑶步骤Ⅲ中所加指示剂为 ,滴定终点的现象 。
⑷反应结束后从液体混合物中回收四氯化碳,则所需操作有 。
命题:洪强 校对:陈公明
 扬州中学2010届高三模拟考试化学答题纸
2010.05
扬州中学2010届高三模拟考试化学答题纸
2010.05
成绩
20.A.(12分)CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①CuCl可以由CuCl2用适当的还原剂如S02、SnCl2等还原制得:
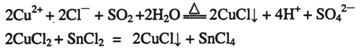
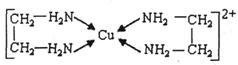 ②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
(1)基态Cu原子的核外电子排布式为______________。H、N、O三种元素的电负性由大到小的顺序是_____。
(2)SO2分子的空间构型为____。与SnCl4互为等电子体的一种离子的化学式为______
 (3)乙二胺分子中氮原子轨道的杂化类型为_______。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是______________________。
(3)乙二胺分子中氮原子轨道的杂化类型为_______。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是______________________。
(4)②中所形成的配离子中含有的化学键类型有__________。
a.配位键 b.极性键 c.离子键 d.非极性键
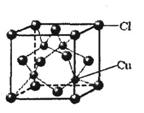
(5)CuCl的晶胞结构如右图所示,其中Cl原子的配位数为_________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com