
17£Æ(±æ¬˙∑÷12∑÷)
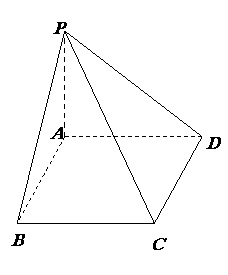 …Ë”–
…Ë”–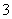 ∏ˆÕ∂«Ú ÷£¨∆‰÷–“ª»À√¸÷–¬ Œ™
∏ˆÕ∂«Ú ÷£¨∆‰÷–“ª»À√¸÷–¬ Œ™ £¨ £œ¬µƒ¡Ω»ÀÀÆ∆Ωœýµ±«“√¸÷–¬ æ˘Œ™
£¨ £œ¬µƒ¡Ω»ÀÀÆ∆Ωœýµ±«“√¸÷–¬ æ˘Œ™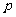
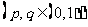 £¨√øŒªÕ∂«Ú ÷æ˘∂¿¡¢Õ∂«Ú“ª¥Œ£¨º«Õ∂«Ú√¸÷–µƒ◊Ð¥Œ ˝Œ™Àʪ˙±‰¡øŒ™
£¨√øŒªÕ∂«Ú ÷æ˘∂¿¡¢Õ∂«Ú“ª¥Œ£¨º«Õ∂«Ú√¸÷–µƒ◊Ð¥Œ ˝Œ™Àʪ˙±‰¡øŒ™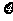 .
.
°°(¢Ò)µ±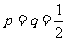 ±£¨«Û
±£¨«Û º∞
º∞ £ª
£ª
(¢Ú)µ±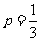 £¨
£¨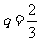 ±£¨«Û
±£¨«Û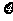 µƒ∑÷≤º¡–∫Õ
µƒ∑÷≤º¡–∫Õ .
.
16£Æ(±æ–°Ã‚¬˙∑÷12∑÷)
“—÷™£∫œÚ¡ø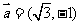 £¨
£¨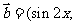
 £¨(
£¨(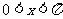 )£¨∫Ø ˝
)£¨∫Ø ˝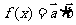 °£
°£
(1)»Ù £¨«Û
£¨«Û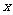 µƒ÷µ£ª
µƒ÷µ£ª
(2)«Û∫Ø ˝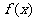 µƒ»°µ√◊Ó¥Û÷µ ±£¨œÚ¡ø
µƒ»°µ√◊Ó¥Û÷µ ±£¨œÚ¡ø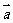 ”Î
”Î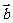 µƒº–Ω«£Æ
µƒº–Ω«£Æ
(∂˛)—°◊ˆÃ‚(14 ~ 15£¨øº…˙÷ªƒÐ¥”÷–—°◊ˆ“ªÃ‚)
14£Æ(◊¯±Íœµ”Î≤Œ ˝∑Ω≥×°◊ˆÃ‚)»Ù÷±œþ °° (
°° (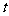 Œ™≤Œ ˝)±ª«˙œþ°°
Œ™≤Œ ˝)±ª«˙œþ°° 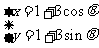 °°(
°°(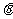 Œ™≤Œ ˝£¨
Œ™≤Œ ˝£¨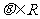 )À˘Ωÿ£¨‘ÚΩÿµ√µƒœ“µƒ≥§∂» «____________.
)À˘Ωÿ£¨‘ÚΩÿµ√µƒœ“µƒ≥§∂» «____________.
15. (º∏∫Œ÷§√˜—°Ω≤—°◊ˆÃ‚)»ÁÕº£¨
(º∏∫Œ÷§√˜—°Ω≤—°◊ˆÃ‚)»ÁÕº£¨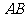 «°—
«°—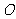 µƒ÷±æ∂£¨
µƒ÷±æ∂£¨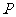 «
«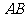 —”≥§œþ…œµƒ“ªµ„°£π˝
—”≥§œþ…œµƒ“ªµ„°£π˝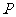 ◊˜°—
◊˜°—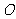 µƒ«–œþ£¨«–µ„Œ™
µƒ«–œþ£¨«–µ„Œ™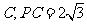 £¨»Ù
£¨»Ù £¨‘Ú°—
£¨‘Ú°—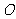 µƒ÷±æ∂
µƒ÷±æ∂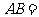 ___________.
___________.
1£ÆºØ∫œ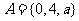 £¨
£¨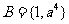 £¨»Ù
£¨»Ù £¨‘Ú
£¨‘Ú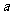 µƒ÷µŒ™(°°°° )
µƒ÷µŒ™(°°°° )
A£Æ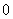 °°°°°°°°°°
B£Æ
°°°°°°°°°°
B£Æ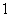 °°°°°°°° °°°° C£Æ
°°°°°°°° °°°° C£Æ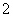 °°°°°° °°°° D£Æ
°°°°°° °°°° D£Æ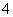
2£Æ“—÷™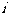 Œ™–È ˝µ•Œª£¨«“”–
Œ™–È ˝µ•Œª£¨«“”–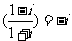 £¨
£¨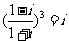 £¨‘Ú
£¨‘Ú (°°°°
)
(°°°°
)
A£Æ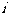 °° °°°°°°°°B£Æ
°° °°°°°°°°B£Æ °° °°°°C£Æ
°° °°°°C£Æ °° °°°°D£Æ
°° °°°°D£Æ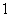
 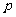 £¨‘Ú £¨‘Ú °±”Î√¸Ã‚°∞»Ù °±”Î√¸Ã‚°∞»Ù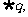 ‘Ú ‘Ú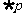 °±ª•Œ™ƒÊ∑Ò√¸Ã‚;
(2)£Æ°∞»Ù °±ª•Œ™ƒÊ∑Ò√¸Ã‚;
(2)£Æ°∞»Ù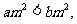 ‘Ú ‘Ú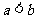 °±µƒƒÊ√¸Ã‚Œ™’Ê√¸Ã‚; °±µƒƒÊ√¸Ã‚Œ™’Ê√¸Ã‚;(3)£Æ√¸Ã‚  £¨√¸Ã‚ £¨√¸Ã‚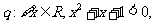 ‘Ú ‘Ú Œ™’Ê; Œ™’Ê;(4).»Ù µ ˝ 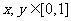 £¨‘Ú¬˙◊„ £¨‘Ú¬˙◊„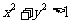 µƒ∏≈¬ Œ™ µƒ∏≈¬ Œ™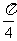 . .°°°° A£Æ 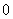 °°°°°°°°°°
B£Æ °°°°°°°°°°
B£Æ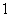 °°°°°°°°°° °°°° C£Æ °°°°°°°°°° °°°° C£Æ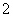 °°°°°° °°°° D£Æ °°°°°° °°°° D£Æ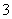 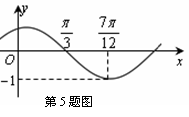 5£Æ∫Ø ˝ 5£Æ∫Ø ˝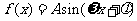 (∆‰÷– (∆‰÷–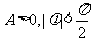 )µƒÕºœÛ»ÁÕºÀ˘ 棨Œ™¡Àµ√µΩ )µƒÕºœÛ»ÁÕºÀ˘ 棨Œ™¡Àµ√µΩ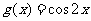 µƒÕºœÒ£¨‘Ú÷ª“™Ω´ µƒÕºœÒ£¨‘Ú÷ª“™Ω´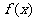 µƒÕºœÒ(°°°° )°°°°°°°°°°°°°°°°°°°°°°°°°°°° µƒÕºœÒ(°°°° )°°°°°°°°°°°°°°°°°°°°°°°°°°°°
A£ÆœÚ”“∆Ω“∆  ∏ˆµ•Œª≥§∂» °°°°°°B£ÆœÚ”“∆Ω“∆ ∏ˆµ•Œª≥§∂» °°°°°°B£ÆœÚ”“∆Ω“∆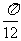 ∏ˆµ•Œª≥§∂» ∏ˆµ•Œª≥§∂»C£ÆœÚ◊Û∆Ω“∆  ∏ˆµ•Œª≥§∂»°° °°°°D£ÆœÚ◊Û∆Ω“∆ ∏ˆµ•Œª≥§∂»°° °°°°D£ÆœÚ◊Û∆Ω“∆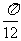 ∏ˆµ•Œª≥§∂» ∏ˆµ•Œª≥§∂»°° 6£Æ∑÷±¿¥◊‘π„÷ð÷¥–≈÷–—ß°¢…Ó€⁄Õ‚π˙”Ô—ß–£°¢÷–…ΩºÕƒÓ÷–—ßµƒ3–£—ß…˙≤Œπ€¥˙±ÌÕ≈±ª∞≤≈≈‘⁄÷Гª÷¡÷Ќµƒ5ÃÏ÷–≤Œπ€…œ∫£ ¿≤©ª·£¨“™«Û√ø–£—ß…˙¥˙±ÌÕ≈≤Œπ€“ªÃÏ«“√øÃÏ÷¡∂ý∞≤≈≈“ª–£—ß…˙≤Œπ€¥˙±ÌÕ≈£¨≤¢“™«Ûπ„÷ð÷¥–≈÷–—ß—ß…˙¥˙±ÌÕ≈∞≤≈≈‘⁄¡ÌÕ‚¡Ω–£—ß…˙¥˙±ÌÕ≈«∞√Ê£¨‘Ú≤ªÕ¨µƒ∞≤≈≈∑Ω∑®π≤”–(°° °°°°) A. 20÷÷°°°°°°°°°°°° B. 30÷÷°°°°°°°° C. 40÷÷°°°°°°°°°°°° D. 60÷÷ °° 7£ÆΩ´“ªø≈˜ª◊”Õ∂÷¿¡Ω¥Œ£¨µ⁄“ª¥Œ≥ˆœ÷µƒµ„ ˝º«Œ™ 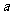 £¨µ⁄∂˛¥Œ≥ˆœ÷µƒµ„ ˝º«Œ™ £¨µ⁄∂˛¥Œ≥ˆœ÷µƒµ„ ˝º«Œ™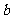 ,…Ë¡ΩÃı÷±œþ ,…Ë¡ΩÃı÷±œþ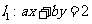 £¨ £¨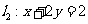 ∆Ω––µƒ∏≈¬ Œ™ ∆Ω––µƒ∏≈¬ Œ™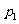 £¨œýΩªµƒ∏≈¬ Œ™ £¨œýΩªµƒ∏≈¬ Œ™ £¨ ‘Œ µ„ £¨ ‘Œ µ„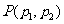 ”Î÷±œþ ”Î÷±œþ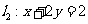 µƒŒª÷√πÿœµ «°°°° (°° °°°°) µƒŒª÷√πÿœµ «°°°° (°° °°°°)°°°° A£Æ 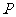 ‘⁄÷±œþ ‘⁄÷±œþ µƒ”“œ¬∑Ω°°°°°°°°°°°°°° B£Æ µƒ”“œ¬∑Ω°°°°°°°°°°°°°° B£Æ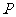 ‘⁄ ‘⁄ ÷±œþµƒ◊Ûœ¬∑Ω ÷±œþµƒ◊Ûœ¬∑Ω°°°° C£Æ 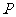 ‘⁄÷±œþ ‘⁄÷±œþ µƒ”“…œ∑Ω°°°°°°°°°°°°°° D£Æ µƒ”“…œ∑Ω°°°°°°°°°°°°°° D£Æ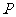 ‘⁄÷±œþ ‘⁄÷±œþ …œ …œ°°  8£Æ
»Á”“Õº ˆ’Û≥∆Œ™°∞…≠µ¬¿≠ƒ∑…∏°±£¨º«µ⁄ 8£Æ
»Á”“Õº ˆ’Û≥∆Œ™°∞…≠µ¬¿≠ƒ∑…∏°±£¨º«µ⁄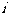 ––µ⁄ ––µ⁄ ¡–µƒ ˝Œ™ ¡–µƒ ˝Œ™ £¨∂‘»Œ“‚’˝’˚ ˝Œ™ £¨∂‘»Œ“‚’˝’˚ ˝Œ™ £¨±ÿ”–’˝’˚ ˝ £¨±ÿ”–’˝’˚ ˝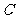 πµ√ πµ√ Œ™∫œ ˝(∫œ ˝µƒ∂®“ «£∫∫œ ˝ «≥˝¡À Œ™∫œ ˝(∫œ ˝µƒ∂®“ «£∫∫œ ˝ «≥˝¡À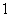 ∫ÕÀ¸±æ…̪πƒÐ±ª∆‰À˚µƒ’˝’˚ ˝’˚≥˝µƒ’˝’˚ ˝£¨≥˝ ∫ÕÀ¸±æ…̪πƒÐ±ª∆‰À˚µƒ’˝’˚ ˝’˚≥˝µƒ’˝’˚ ˝£¨≥˝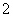 ÷ÆÕ‚µƒ≈º ˝∂º «∫œ ˝)£¨‘Ú’‚—˘µƒ ÷ÆÕ‚µƒ≈º ˝∂º «∫œ ˝)£¨‘Ú’‚—˘µƒ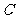 ø…“‘ «(°°°° ) ø…“‘ «(°°°° )°° A£Æ  °°°°°°°°°°°°°° B£Æ °°°°°°°°°°°°°° B£Æ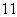 °°°°°°°°°°C£Æ °°°°°°°°°°C£Æ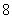 °°°° °°°°°°°°°° D£Æ °°°° °°°°°°°°°° D£Æ µ⁄∂˛≤ø∑÷ ∑«—°‘ÒÂ(π≤ 110°° ∑÷) ∂˛°¢ÃÓø’£∫±æ¥ÛÂπ≤7–°Ã‚£¨øº…˙◊˜¥6–°Ã‚£¨√ø–°Ã‚5∑÷£¨¬˙∑÷30∑÷£Æ (“ª)±ÿ◊ˆÃ‚(9-13Â) 9£Æ“—÷™œÚ¡ø 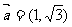 £¨ £¨ £¨»Ù £¨»Ù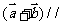 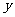 ÷·£¨ ‘Ú ÷·£¨ ‘Ú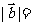 °°°°°°°°°°
£ª °°°°°°°°°°
£ª10£Æ»Áπ˚ 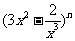 µƒ’πø™ Ω÷–∫¨”–∑«¡„≥£ ˝œÓ£¨‘Ú’˝’˚ ˝ µƒ’πø™ Ω÷–∫¨”–∑«¡„≥£ ˝œÓ£¨‘Ú’˝’˚ ˝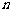 µƒ◊Ó–°÷µŒ™°°°°°°°°°°°°
£ª µƒ◊Ó–°÷µŒ™°°°°°°°°°°°°
£ª 11£Æ“—÷™Õ÷‘≤ 11£Æ“—÷™Õ÷‘≤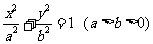 µƒΩπæýŒ™ µƒΩπæýŒ™ £¨«“ £¨«“ “¿¥Œ≥…µ»≤Ó ˝¡–£¨‘ÚÕ÷‘≤µƒ¿Î–ƒ¬ Œ™°° °°°°°°°°°°£ª “¿¥Œ≥…µ»≤Ó ˝¡–£¨‘ÚÕ÷‘≤µƒ¿Î–ƒ¬ Œ™°° °°°°°°°°°°£ª12. ∂‘“ª∏ˆ◊˜÷±œþ‘À∂صƒ÷ µ„µƒ‘À∂Øπ˝≥Ãπ€≤‚¡À8¥Œ,µ√µΩ »Áœ¬±ÌÀ˘ 浃 ˝æð.
‘⁄…œ ˆÕ≥º∆ ˝æðµƒ∑÷Œˆ÷–,“ª≤ø∑÷º∆À„º˚»ÁÕºÀ˘ 浃 À„∑®¡˜≥ÃÕº(∆‰÷– ‘Ú ‰≥ˆµƒSµƒ÷µ «°°°°°°°° . 13£Æ»ÁÕº,‘⁄»˝¿‚◊∂ ¡Ω¡Ω¥π÷±,«“
∑÷± «»˝¿‚◊∂
‘Ú ‘Ú’˝ µ ˝ 6£ÆNa2O2µƒµÁ◊” ΩŒ™Na+[????]2£≠Na+£¨π “ı°¢—Ù¿Î◊”µƒ∏ˆ ˝±»Œ™1°√2£¨A¥ÌŒÛ£ª…˙≥…œýÕ¨¡øµƒO2 ±œ˚∫ƒµƒÀÆ∫Õ∂˛—ıªØúµƒŒÔ÷ µƒ¡øœýÕ¨£¨µ´÷ ¡ø≤ªÕ¨£¨BœÓ¥Ì£ª”…µ√ ßµÁ◊” ÿ∫„÷™∂˛’þ◊™“∆µÁ◊”µƒŒÔ÷ µƒ¡øœýÕ¨£¨CœÓ’˝»∑£ªNa2O2“Úæþ”–«ø—ıªØ–‘∂¯”–∆Ø∞◊–‘£¨SO2“◊”Δ–…´ŒÔ÷ ªØ∫œ…˙≥…ŒÞ…´≤ªŒ»∂®µƒŒÔ÷ £¨π ‘≠¿Ì≤ªÕ¨£¨DœÓ¥ÌŒÛ°£ 5£ÆNa2O2”ÎCO2∫ÕH2O∑¥”¶π˝≥Ã÷–£¨Na2O2º» «—ıªØº¡”÷ «ªπ‘≠º¡£¨C¥ÌŒÛ£¨D’˝»∑£ªNa2O2”ÎÀ·∑¥”¶≤ªΩˆ…˙≥…—Œ∫ÕÀÆ£¨ªπ…˙≥…O2£¨π Na2O2≤ª «ºÓ–‘—ıªØŒÔ£¨A¥ÌŒÛ£ªNa2O2”ÎÀÆ∑¥”¶…˙≥…O2£¨ª·“˝»Î–¬µƒ‘”÷ £¨B¥ÌŒÛ°£ 4£Æƒ∆‘⁄—Œ»Ð“∫÷–œ»”ÎÀÆ∑¥”¶°£ 3£Æ¥ÀÂøº≤È◊€∫œ∑÷ŒˆƒÐ¡¶°£±Ω”ÎÀƪ•≤ªœý»Ð£¨«“ƒ∆µƒ√Ð∂»¥¶”⁄±Ω∫ÕÀÆ÷ƺ‰£¨º”»Îƒ∆∫Û£¨ƒ∆¥¶‘⁄±Ω”ÎÀƵƒ÷–º‰£ª”…”⁄ƒ∆ƒÐ”ÎÀÆ∑¥”¶£¨«“ƒ∆”ÎÀÆ∑¥”¶∑≈≥ˆ«‚∆¯£¨À˘“‘ª· πƒ∆‘⁄±Ω∫ÕÀƵƒΩÁ√Ê¥¶∑¥”¶≤¢ø…ƒÐ◊˜…œœ¬Ã¯∂Ø°£ 2£Æm(NaOH)£Ωn(Na)°§M(NaOH)£Ω°¡40 g/mol£Ω8 g m(H2)£Ωn(Na)°§M(H2)£Ω°¡°¡2 g/mol £Ω0.2 g m[NaOH(aq)]£Ωm(Na)+m(H2O)£≠m(H2)£Ω4.6 g+95.6 g£≠0.2 g£Ω100 g À˘“‘w£Ω°¡100%£Ω8.0%°£ 6£ÆŒ™¡À π”Ó∫Ω‘±‘⁄∑…¥¨÷–µ√µΩ“ª∏ˆŒ»∂®µƒ°¢¡º∫√µƒ…˙¥Êª∑æ≥£¨“ª∞„‘⁄∑…¥¨ƒ⁄∞≤◊∞ ¢”–Na2O2ªÚK2O2ø≈¡£µƒ◊∞÷√£¨À¸µƒ”√Õæ «≤˙…˙—ı∆¯°£œ¬¡–πÿ”⁄Na2O2µƒ– ˆ’˝»∑µƒ «°° (°°C°°) A.Na2O2÷–“ı°¢—Ù¿Î◊”µƒ∏ˆ ˝±»Œ™1°√1 B.Na2O2∑÷±”ÎÀƺ∞CO2∑¥”¶≤˙…˙œýÕ¨¡øµƒO2 ±£¨–Ë“™ÀÆ∫ÕCO2µƒ÷ ¡øœýµ» C.Na2O2∑÷±”ÎÀƺ∞CO2∑¥”¶≤˙…˙œýÕ¨¡øµƒO2 ±£¨◊™“∆µÁ◊”µƒŒÔ÷ µƒ¡øœýµ» D.Na2O2µƒ∆Ø∞◊‘≠¿Ì”ÎSO2µƒ∆Ø∞◊‘≠¿ÌœýÕ¨ [∂‘µ„—µ¡∑] Na2O°˙Na2O°˙NaOH°˙Na2CO3°§10H2O°˙Na2CO3°£A÷–£¨…ʺ∞µƒ «Na°˙Na2Oµƒ±‰ªØ£¨“ÚŒ™Ω Ùƒ∆ «“¯∞◊…´£¨∂¯—ıªØƒ∆Œ™∞◊…´£¨π ø…“‘ø¥µΩ±Ì√Ê—∏ÀŸ±‰∞µ£ªB÷–£¨…ʺ∞µƒ «NaOHŒ¸ ’ø’∆¯÷–µƒÀÆ∑÷∂¯‘⁄±Ì√Ê–Œ≥…»Ð“∫£ªC÷–£¨…ʺ∞µƒ «Na2CO3°§10H2O°˙Na2CO3µƒ±‰ªØ£¨∑ÁªØ∫Ûµ√µΩúÀ·ƒ∆∑€ƒ©£ªD÷–£¨‘⁄“‘…œÀ˘”–±‰ªØ÷–£¨÷ª”–Na°˙Na2Oπ˝≥ÃŒ™—ıªØªπ‘≠∑¥”¶°£ Õ¨≤Ω¡∑œ∞≤·¥∞∏ π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì ∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯ Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com∞Ê»®…˘√˜£∫±æ’æÀ˘”–Œƒ’¬£¨Õº∆¨¿¥‘¥”⁄Õ¯¬Á£¨÷¯◊˜»®º∞∞Ê»®πÈ‘≠◊˜’þÀ˘”–£¨◊™‘ÿŒÞ“‚«÷∑∏∞Ê»®£¨»Á”–«÷»®£¨«Î◊˜’þÀŸ¿¥∫Ø∏Ê÷™£¨Œ“√«Ω´æ°øÏ¥¶¿Ì£¨¡™œµqq£∫3310059649°£ ICP±∏∞∏–Ú∫≈: ª¶ICP±∏07509807∫≈-10 ∂ıπ´Õ¯∞≤±∏42018502000812∫≈ |