
2.(2010福建文数)计算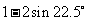 的结果等于( )
的结果等于( )
A.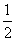 B.
B.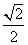 C.
C.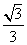 D.
D.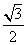
[答 案]B
案]B
[解析]原式=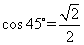 ,故选B.
,故选B.
[命题意图]本题三角变换中的二倍角公式,考查特殊角的三角函数值
(2010全国卷1文数) (1)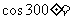
(A)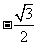 (B)-
(B)-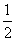 (C)
(C)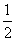 (D)
(D) 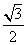
7.(2010江西理数)E,F是等腰直角△ABC斜边AB上的三等分点,则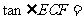 ( )
( )
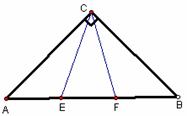 A.
A. 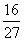 B.
B. 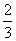 C.
C. 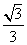
 D.
D. 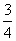
[答案]D
[解析]考查三角函数的计算、解析化应用意识。
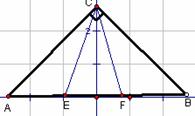 解法1:约定AB=6,AC=BC=
解法1:约定AB=6,AC=BC= ,由余弦定
,由余弦定 理CE=CF=
理CE=CF=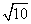 ,再由余弦定理得
,再由余弦定理得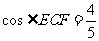 ,
,
解得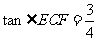
解法2:坐标化。约定AB=6,AC=BC= ,F(1,0),E(-1,0),C(0,3)利用向量的夹角公式得
,F(1,0),E(-1,0),C(0,3)利用向量的夹角公式得
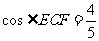 ,解得
,解得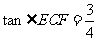 。
。
( 2010重庆文数)(6)下列函数中,周期为
2010重庆文数)(6)下列函数中,周期为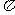 ,且在
,且在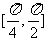 上为减函数的是
上为减函数的是
(A)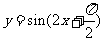 (B)
(B)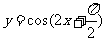
(C)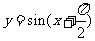 (D)
(D)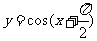
解析:C、D中函数周期为2 ,所以错误
,所以错误
当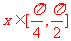 时,
时,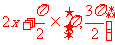 ,函数
,函数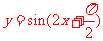 为减函数
为减函数
而函数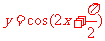 为增函数,所以选A
为增函数,所以选A
 (2010重庆理数)
(2010重庆理数)
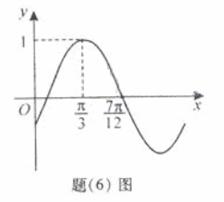
(6)已知函数 的部分图象如题(6)图所示,则
的部分图象如题(6)图所示,则
A.
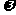 =1
=1 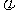 =
= 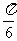 B.
B.  =1
=1 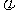 =-
=- 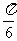 C.
C. 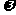 =2
=2 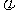 =
=  D.
D. 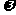 =2
=2 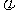 = -
= -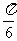
解析: 由五点作图法知
由五点作图法知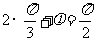 ,
,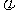 = -
= -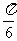
(2010山东文数)(10)观察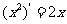 ,
,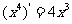 ,
,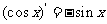 ,由归纳推理可得:若定义在
,由归纳推理可得:若定义在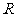 上的函数
上的函数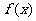 满足
满足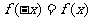 ,记
,记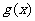 为
为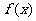 的导函数,则
的导函数,则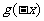 =
=
(A)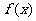 (B)
(B)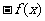 (C)
(C) 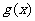
 (D)
(D)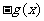
答案:D
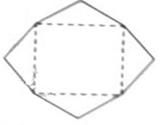 (2010北京文数)(7)某班设计了一个八边形的班徽(如图),它由腰长为1,
(2010北京文数)(7)某班设计了一个八边形的班徽(如图),它由腰长为1,
顶角为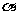 的四个等腰三角形,及其底边构成的正方形所组成,
的四个等腰三角形,及其底边构成的正方形所组成,
该八边形的面积为
(A)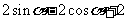 ;
(B)
;
(B)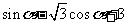
(C)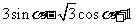 ; (D)
; (D)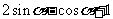
答案:A
(2010四川理数)(6)将函数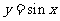 的图像上所有的点向右平行移动
的图像上所有的点向右平行移动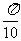 个单位长
个单位长
度,再把所得各点的横坐标伸长到原来的2倍(纵坐标不变),所得图像的函数解析式是
(A)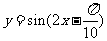 (B)
(B)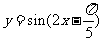
(C)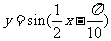 (D)
(D)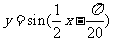
解析:将函数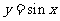 的图像上所有的点向右平行移动
的图像上所有的点向右平行移动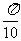 个单位长度,所得函数图象的解析式为y=sin(x-
个单位长度,所得函数图象的解析式为y=sin(x-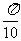 )
)
再把所得各点的横坐标伸长到原来的2倍(纵坐标不变),所得图像的函数解析式是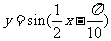 .
.
答案:C
(2010天津文数)(8)
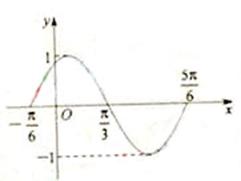
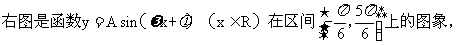 为了得到这个函数的图象,只要将
为了得到这个函数的图象,只要将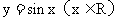 的图象上所有的点
的图象上所有的点
(A)向左平移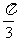 个单位长度,再把所得各点的横坐标缩短到原来的
个单位长度,再把所得各点的横坐标缩短到原来的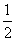 倍,纵坐标不变
倍,纵坐标不变
(B) 向左平移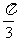 个单位长度,再把所得各点的横坐标伸长到原来的2倍,纵坐标不变
个单位长度,再把所得各点的横坐标伸长到原来的2倍,纵坐标不变
(C) 向左平移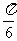 个单位长度,再把所得各点的横坐标缩短到原来的
个单位长度,再把所得各点的横坐标缩短到原来的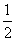 倍,纵坐标不变
(D) 向左平移
倍,纵坐标不变
(D) 向左平移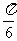 个单位长度,再把所得各点的横坐标伸长到原来的2倍,纵坐标不变
个单位长度,再把所得各点的横坐标伸长到原来的2倍,纵坐标不变
[答案]A
[解析]本题主要考查三角函数的图像与图像变换的基础知识,属于中等题。
由图像可知函数的周期为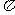 ,振幅为1,所以函数的表达式可以是y=sin(2x+
,振幅为1,所以函数的表达式可以是y=sin(2x+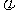 ).代入(-
).代入(-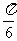 ,0)可得
,0)可得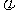 的一个值为
的一个值为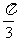 ,故图像中函数的一个表达式是y=sin(2x+
,故图像中函数的一个表达式是y=sin(2x+
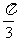 ),即y=sin2(x+
),即y=sin2(x+ 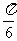 ),所以只需将y=sinx(x∈R)的图像上所有的点向左平移
),所以只需将y=sinx(x∈R)的图像上所有的点向左平移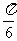 个单位长度,再把所得各点的横坐标缩短到原来的
个单位长度,再把所得各点的横坐标缩短到原来的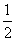 倍,纵坐标不变。
倍,纵坐标不变。
[温馨提示]根据图像求函数的表达式时,一般先求周期、振幅,最后求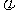 。三角函数图像进行平移变换时注意提取x的系数,进行周期变换时,需要将x的系数变为原来的
。三角函数图像进行平移变换时注意提取x的系数,进行周期变换时,需要将x的系数变为原来的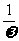
(2010天津理数)(7)在△ABC中,内角A,B,C的对边分别是a,b,c,若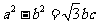 ,
, ,则A=
,则A=
(A)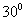 (B)
(B) (C)
(C) (D)
(D)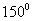
[答案]A
[解析]本题主要考查正弦定理与余弦定理的基本应用,属于中等题。
由由正弦定理得
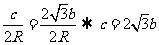 ,
,
所以cosA=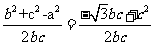 =
=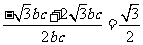 ,所以A=300
,所以A=300
[温馨提示]解三 角形的基本思路是利用正弦、余弦定理将边化为角运算或将角化为边运算。
角形的基本思路是利用正弦、余弦定理将边化为角运算或将角化为边运算。
(2010福建文数)

3.(2010陕西文数)函数f (x)=2sinxcosx是 [C]
(A)最小正周期为2π的奇函数 (B)最小正周期为2π的偶函数
(C)最小正周期为π的奇函数 (D) 最小正周期为π的偶函数
最小正周期为π的偶函数
解析:本题考查三角函数的性质
f (x)=2sinxcosx=sin2x,周期为π的奇函数
(2010辽宁文数)(6)设 ,函数
,函数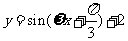 的图像向右平移
的图像向右平移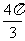 个单位后与原图像重合,则
个单位后与原图像重合,则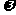 的最小值是
的最小值是
(A)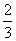 (B)
(B) 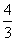 (C)
(C) 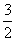 (D)
(D) 3
3
解析:选C.由已知,周期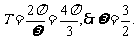
(2010辽宁理数)(5)设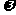 >0,函数y=s
>0,函数y=s in(
in(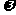 x+
x+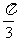 )+2的图像向右平移
)+2的图像向右平移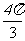 个单位后与原图像重合,则
个单位后与原图像重合,则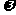 的最小值是
的最小值是
(A) (B)
(B)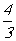 (C)
(C)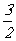 (D)3
(D)3
[答案]C
[命题立意]本题考查了三角函数图像的平移变换与三角函数的周期性,考查了同 学们对知识灵活掌握的程度。
学们对知识灵活掌握的程度。
[解析]将y=sin(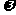 x+
x+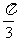 )+2的图像向右平移
)+2的图像向右平移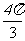 个单位后为
个单位后为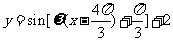
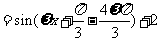 ,所以有
,所以有
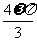 =2k
=2k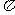 ,即
,即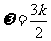 ,又因为
,又因为 ,所以k≥1,故
,所以k≥1,故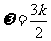 ≥
≥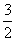 ,所以选C
,所以选C
(2010全国卷2文数)(3)已知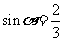 ,则
,则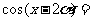
(A) (B)
(B)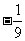 (C)
(C)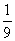 (D)
(D)
[解析]B:本题考查了二倍角公式及诱导公式,∵ sina=2/3,
∴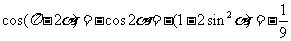
7.(2010湖南文数)在△ABC中,角A,B,C所对的边长分别为a,b,c,若∠C=120°,c=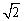 a,则
a,则
A.a>b B.a<b
C. a=b D.a与b的大小关系不能确定
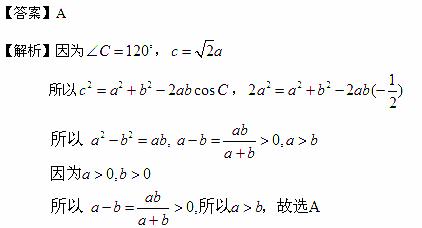
[命题意图]本题考查余弦定理,特殊角的三角函数值,不等式的性质,比较法,属中档题。
(2010浙江理数)(9)设函数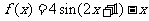 ,则在下列区间中函
,则在下列区间中函 数
数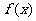 不存在零点的是
不存在零点的是
(A)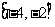 (B)
(B)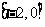 (C)
(C)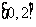 (D)
(D)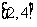
解析:将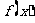 的零点转化为函数
的零点转化为函数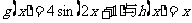 的交点,数形结合可知答案选A,本题主要考察了三角函数图像的平移和函数与方程的相关知识点,突出了对转化思想和数形结合思想的考察,对能力要求较高,属较难题
的交点,数形结合可知答案选A,本题主要考察了三角函数图像的平移和函数与方程的相关知识点,突出了对转化思想和数形结合思想的考察,对能力要求较高,属较难题
(2010浙江理数)(4)设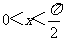 ,则“
,则“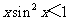 ”是“
”是“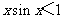 ”的
”的
(A)充分而不必要条件 (B)必要而不充分条件
(C)充分必要条件 (D)既不充分也不必要条件
解析:因为0<x<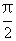 ,所以sinx<1,故xsin2x<xsinx,结合xsin2x与xsinx的取值范围相同,可知答案选B,本题主要考察了必要条件、充分条件与充要条件的意义,以及转化思想和处理不等关系的能力,属中档题
,所以sinx<1,故xsin2x<xsinx,结合xsin2x与xsinx的取值范围相同,可知答案选B,本题主要考察了必要条件、充分条件与充要条件的意义,以及转化思想和处理不等关系的能力,属中档题
(2010全国卷2理数)(7)为了得到函数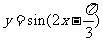 的
的 图像,只需把函数
图像,只需把函数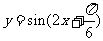 的图像
的图像
(A )向左平移
)向左平移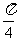 个长度单位
(B)向右平移
个长度单位
(B)向右平移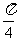 个长度单位
个长度单位
(C)向左平移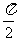 个长度单位
(D)向右平移
个长度单位
(D)向右平移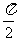 个长度单位
个长度单位
[答案]B
[命题意图]本试题主要考查三角函数图像的平移.
[解析]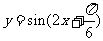 =
= ,
,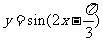 =
=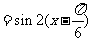 ,所以将
,所以将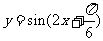 的图像向右平移
的图像向右平移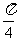 个长度单位得到
个长度单位得到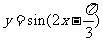 的图像,故选B.
的图像,故选B.
18.(2010上海文数)若△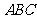 的三个内角满足
的三个内角满足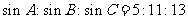 ,则△
,则△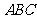
(A)一定是锐角三角形. (B)一定是直角三角形.
(C)一定是钝角三角形. (D)可能是锐角三角形,也可能是钝角三角形.
解析:由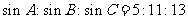 及正弦定理得a:b:c=5:11:13
及正弦定理得a:b:c=5:11:13
由余弦定理得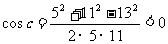 ,所以角C为钝角
,所以角C为钝角
3.(2010天津卷)下列鉴别方法可行的是
A.用氨水鉴别Al3+、Mg2+和Ag+
B.用Ba(NO3)2溶液鉴别Cl-、SO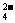 和CO
和CO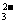
C.用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷
D.用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO
解析:Al3+和Mg2+与氨水反应都只生成沉淀,不溶解,无法鉴别,故A错;SO42-和CO32-与Ba(NO3)2反应都生成白色沉淀,无法鉴别,故B错;1-溴丙烷有三种等效氢,其核磁共振谱有三个峰,而2-溴丙烷有两种等效氢原子,其核磁共振谱有两个峰,故可鉴别,C正确;碳碳双键、醛基都能被酸性KMnO4氧化,KMnO4溶液都退色,故无法鉴别。
答案:C
命题立意:考查阴阳离子和有机物的鉴别,通过鉴别,考查离子或有机物的化学性质。
(2010广东理综卷)32(16分)
碳酸锂广泛应用于陶瓷和医药等领域。以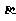 -锂辉石(主要成分为Li2O
-锂辉石(主要成分为Li2O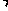 Al2O3
Al2O3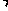 4SiO2)为原材料制备Li2CO3的工艺流程如下:
4SiO2)为原材料制备Li2CO3的工艺流程如下:
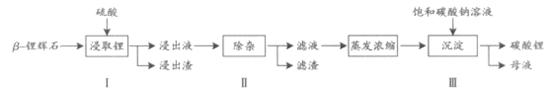
已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的PH分别为3.2、5.2、9.7和12.4;Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g和1.3g.
(1)步骤Ⅰ前,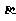 -锂辉石要粉碎成细颗粒的目的是_____________.
-锂辉石要粉碎成细颗粒的目的是_____________.
(2)步骤Ⅰ中,酸浸后得到的酸性溶液中含有Li+、SO42-,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入_____________(填“石灰石”、“氯化钙”或“稀硫酸”)以调节溶液的PH到6.0~6.5,沉淀部分杂质离子,然后分离得到浸出液。
(3)步骤Ⅱ中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有______________.
(4)步骤Ⅲ中,生成沉淀的离子方程式为________________.
(5)从母液中可回收的主要物质是_____________.
解析:(1)粉碎可以增大接触面积,加快反应速率
(2) 要增强溶液的碱性,只能加入石灰石
(3)
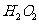 可以氧化
可以氧化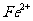 为
为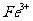 ,石灰乳和
,石灰乳和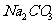 使得
使得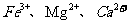 沉淀
沉淀
(4)
步骤Ⅲ生成的沉淀是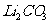 ,离子方程式为:
,离子方程式为: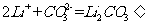
(5)
母液中的溶质是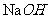 、
、 ,可以回收
,可以回收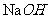 。
。
答案:(1)加快反应速率
(2)石灰石
(3)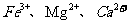
(4)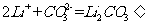
(5)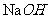 。
。
28.(2010全国卷1)(15分)有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五中溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1) 能确定溶液是(写出溶液标号与相应溶质的化学式):
(2) 不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:
[解析](I)由题干表述可知A和E不是盐,又由纯E为无色油状液体,推知E为硫酸(③步操作进一步确定);(II)由题干和①步操作可知A为氨水; (III)再由②步操作可知F中阳离子为Ag+发生的反应为:Ag++NH3·H2O=AgOH↓+NH4+;AgOH+2NH3·H2O=[Ag(NH3)2]++OH-+2H2O;而常见的盐中只有AgNO3可溶于水,故F为AgNO3;(IV)由③步操作可知B中阴离子应为CO32-,由于此无色无味的气体只能是CO2, B、C、D中能生成沉淀说明不能是HCO3-,而阳离子可是常见的K+、Na+、NH4+等待定(V)同样由②步操作D中能与氨水生成沉淀的无色溶液中常见的为阳离子为Mg2+或Al3+,而阴离子需待下步反应再确定;(VI)由④步操作生成的沉淀为可能为AgCl、AgBr、AgI、BaSO4、H2SiO3(不合理)等,但限于题干所述中学常用试剂,则沉淀应为AgCl和BaSO4,才不溶于HNO3,一个是与AgNO3结合生成的沉淀,一个是与硫酸结合形成的沉淀,故C应该同时含有Ba2+和Cl-即,C为BaCl2,进而推出D中阴离子应该为SO42-,因为题干所述盐溶液中阴离子均不同,故D为Al2(SO4)3或MgSO4其他解析见答案
[答案](1)A NH3·H2O或NH3 ;E H2SO4 F AgNO3 C BaCl2
若C作为不能确定的溶液,进一步鉴别的方法合理,同样给分
(2)B Na2CO3或K2CO3 用洁净的铂丝蘸取少量B,在酒精灯火焰中灼烧,若焰色呈黄色则B为Na2CO3溶液;若透过蓝色钴玻璃观察焰色呈紫色,则B为K2CO3溶液
D Al2(SO4)3或MgSO4 取少量D,向其中滴加NaOH溶液有沉淀生成,继续滴加过量的NaOH溶液,若沉淀溶解,则D为Al2(SO4)3溶液,若沉淀不溶解,则D为MgSO4溶液
[命题意图]考查学生的分析与综合能力,涉及到无机元素及其化合物的性质,离子反应,未知物的推断,物质的检验,常见物质量多与量少的反应不同,现象不同等,此题综合性强,难度大,区分度很好,是一道不可多得的经典好题!
[点评]此题一改过去每年元素推断的通病,思维容量显著增大能力要求高,与2008年全国卷I理综28题有得一拼,比2009年的第29题出得高超一些,相比以前的无机推断显然有质的飞跃,看到命题人在进步!但是此题是不是一点瑕疵没有呢?x显然不是,例如本题条件很宽广,没太明显的限制条件,因而答案是丰富多彩的,这不会给阅卷者带来喜出望外,只会增加难度,不好统一评分标准,也就缺乏公平性!特别是B和C上就有争议,如B还可能是(NH4)2CO3,C还可能是BaBr2、BaI2等,当然限制一下沉淀颜色就排除了C的歧义!
13.(2010浙江卷) 某钠盐溶液中可能含有 等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色。
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)溶液,再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中公含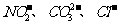 三种阴离子。
三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A. ①②④⑤ B. ③④ C. ③④⑤ D. ②③⑤
试题解析:
本题是离子组合推断、离子鉴别实验综合题。题型难点是:熟悉各种离子的标准检验方法,明确各种离子检验时的干扰因素。本题的难点还有:采用的出题方式和平时不同。
根据最终的离子分析:NO2-,存在时一定没有SO32-,I-。因NO2-,的氧化性可以使他们氧化。Cl-存在下的NO2-的检验:加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体。即证明了NO2-的存在又检验出Cl-的存在。但,仅加入盐酸产生刺激性气体也可能有SO32-的存在。故须先确认SO32-不存在。SO32-,CO32-,SO42-的组合检验可以用:加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色。来确认SO32-, SO42-不存在,CO32-一定存在。故选择③④就可以,顺序是先④后③。
本题答案:B
教与学提示:
本题学生存在的困难是NO2-的检验,因为此内容在选修的《实验化学》中,可能会有所忽视。第二个难点是离子要分成两组分别进行检验。教学中碰到有一些学生:只要碰到离子组合检验与推断的题目就死机的现象。分析原因:各种典型离子的检验方式不是很熟练,没有对各种离子单独检验时的干扰因素,干扰离子进行排除。不重视各种相近实验现象进行区别对待,深入研究相近条件下的不同。教学中从单一离子检验开始,增加干扰,增加组合,增加性质区别等逐步复杂化。要多想为什么,多想如何干扰和排除干扰。
9.(2010四川理综卷)下列离子方程式书写正确的是
A.向明矾溶液中加入过量的氢氧化钡溶液:
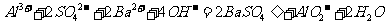
B.向氢氧化亚铁中加入足量的稀硝酸: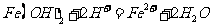
C.向磷酸二氢铵溶液中加入足量的氢氧化钠溶液: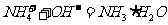
D.向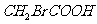 中加入足量的氢氧化钠溶液并加热:
中加入足量的氢氧化钠溶液并加热:

答案: A
解析:本题考查离子方程式正误判断;氢氧化钡溶液过量,Al3+转化为AlO2-,SO42-完全转化为沉淀,A项正确;硝酸有强氧化性,可将Fe2+氧化为Fe3+,硝酸被还原为NO,B不符合客观事实,错误;在磷酸二氢铵中加入足量的氢氧化钠,磷酸二氢根离子中的氢将被中和,C项错误;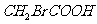 中存在两种官能团,分别是-Br 和-COOH,加入足量的氢氧化钠后加热,与-COOH发生中和反应,与-Br发生水解反应,故应该生成CH2OHCOO-,D项错误。
中存在两种官能团,分别是-Br 和-COOH,加入足量的氢氧化钠后加热,与-COOH发生中和反应,与-Br发生水解反应,故应该生成CH2OHCOO-,D项错误。
12.(2010浙江卷) 下列热化学方程式或离子方程式中,正确的是:
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
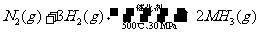 △H=-38.6kJ·
△H=-38.6kJ· mol-1
mol-1
C. 氯化镁溶液与氨水反应: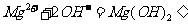
D. 氧化铝溶于NaOH溶液: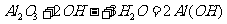
试题解析:
本题考查热化学方程式与离子方程式的书写。A、标准燃烧热的定义,1mol可燃物完全燃烧生成稳定氧化物时方出的热量(标准指298K,1atm)。水液态稳定,方程式系数就是物质的量,故A错。B、根据热化学方程式的含义,与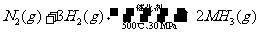 对应的热量是1mol氮气完全反应时的热量,但次反应为可逆反应故,投入0.5mol的氮气,最终参加反应的氮气一定小于0.5mol。所以△H的值大于38.6。B错。D、氢氧化铝沉淀没有沉淀符号。
对应的热量是1mol氮气完全反应时的热量,但次反应为可逆反应故,投入0.5mol的氮气,最终参加反应的氮气一定小于0.5mol。所以△H的值大于38.6。B错。D、氢氧化铝沉淀没有沉淀符号。
本题答案:C
教与学提示:
化学用语的教学是化学学科技术规范,强调准确性,强调正确理解与应用。特别重视热化学方程式的系数与反应热的对应关系。重视离子方程式的拆与不拆的问题。热化学方程式的书写问题由:聚集状态、系数、系数与反应热数值对应、反应热单位、可逆反应的反应热等内容构成。离子方程式的书写问题由:强弱电解质、最简整数比、定组成规律、离子方程式正误判断、守恒、定量离子方程式等内容组成。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com