
7.下面四项是根据生物学原理进行的陈述,其中表述正确的有几项?
①从生态学角度分析,生态系统中流动的能量最初来源于太阳光能
②森林生物群落的群落结构是随着时间的推移会不断变化
③调查遗传病发病率应采用在人群中随机抽样调查方法,研究遗传方式应在患者家系中调查
④近亲结婚会增加后代遗传病的发病率,主要原因在于部分遗传病由隐性致病基因所控制
A.1 B.2 C.3 D.4
6.控制番茄果实颜色(红果对黄果显性)与果实形状(长果对圆果显性)的基因位于两对同源染色体上,现用红色长果番茄与黄色圆果番茄杂交,子代不可能出现的表现型种类及比例是
A.只有一种 B.两种,1∶1 C.三种,1∶2∶1 D.四种,1∶1∶1∶1
5.植物激素中的赤霉素与生长素都能促进茎杆伸长,两者关系可用下图表示,对此认识正确的是
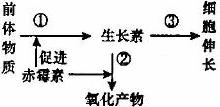 A.赤霉素和生长素都是植物特定器官合成的微量有机物
A.赤霉素和生长素都是植物特定器官合成的微量有机物
B.图中赤霉素对①过程起促进作用,对②过程起抑制作用
C.赤霉素直接促进茎杆伸长,与生长素具有协同作用
D.赤霉素和生长素都能直接扩散进入细胞发挥调节作用
4.分析人类染色体组型发现,有2%-4%的精神病患者的性染色体组成为XYY。导致XYY综合征发生的最可能原因是
A.可能是由父方减数第二次分裂异常所致
B.可能是由父方减数第一次分裂异常所致
C.可能是由母方减数第二次分裂异常所致
D.可能是由母方减数第一次分裂异常所致
3.下列对有关生物知识的叙述不正确的是
A.植物细胞纤维素的合成与高尔基体有关
B.由n个氨基酸形成的蛋白质肽键不一定是n-1个
C.细胞分裂间期不仅消耗A碱基,也消耗U碱基
D.基因对性状的控制是通过控制酶的合成实现的
2.右下图表示在人体细胞核中进行的某一生命活动。据图分析,有关说法正确的是
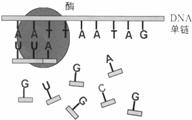 A.参与该生理过程的核苷酸共5种
A.参与该生理过程的核苷酸共5种
B.同一个体不同细胞合成的产物相同
C.该过程必需有RNA聚合酶参与
D.该过程不需要消耗细胞呼吸产生的ATP
1.选择合适的实验材料和恰当的实验方法是实验成功的重要保证。下列关于实验材料选择或实验方法选择的叙述,不正确的是
A.进行还原性糖鉴定时,可以选择含糖丰富的甘蔗为实验材料
B.进行质壁分离和质壁分离复原实验时,采用引流法可使细胞处于不同的液体环境
C.将赫尔希和蔡斯用32P和35S分别标记T2噬菌体的方法,证明DNA是遗传物质
D.观察细胞中DNA、RNA分布时,甲基绿-派洛宁染液要现配现用
16.(13分)(探究创新)某学生欲配制6.0 mol/L的H2SO4 1 000 mL,实验室有三种不同浓
度的硫酸:①480 mL 0.5 mol/L的硫酸;②150 mL 25%的硫酸(ρ=1.18 g/mL);③足量的18 mol/L的硫酸。有三种规格的容量瓶:250 mL、500 mL、1 000 mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为______mol/L(保留1位小数)。
(2)配制该硫酸溶液应选用容量瓶的规格为____
____________________________________________________________________mL。
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18 mol/L的浓硫酸____mL,沿玻璃棒倒入上述混合液中。并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.________________________________________________________________________
________________________________________________________________________;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1-2 cm 处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(4)如果省略操作D,对所配溶液浓度有何影响?______(填“偏大”、“偏小”或“无影
响”)。
(5)进行操作C前还需注意____
____________________________________________________________________。
解析 本题考查了一定物质的量浓度溶液的配制以及有关物质的量浓度的计算。
(1)c==3.0 mol/L
(2)要配制6.0 mol/L的H2SO4溶液1 000 mL,则要选1 000 mL的容量瓶。
(3)所需的18 mol/L的浓硫酸的体积为=0.295 L。
(4)若不洗涤会使溶质损失,则配制的溶液浓度会偏小。
答案 (1)3.0 (2)1 000
(3)295 用适量的水洗涤烧杯和玻璃棒2-3次,洗涤液均注入容量瓶中
(4)偏小
(5)将稀释后的硫酸冷却到室温
15.(12分)(2009·杭州模拟)实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是____
____________________________________________________________________
(填序号),配制上述溶液还需用到的玻璃仪器是___
_____________________________________________________________________
________________________________________________________________________
(填仪器名称)。
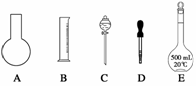
(2)下列操作中,容量瓶所不具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.量取一定体积的液体
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为______g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol/L(填“大于”、“等于”或“小于”,下同)。若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.1 mol/L。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为_ _______mL(计算结果保留一位小数)。如果实验室有15 mL、20 mL、50 mL量筒,应选用________mL量筒最好。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是
________________________________________________________________________
________________________________________________________________________。
解析 (1)五种仪器分别为烧瓶、量筒、分液漏斗、胶头滴管、容量瓶,配制上述溶液肯定不需要烧瓶和分液漏斗,还需要烧杯、玻璃棒。
(2)容量瓶不能用于贮存、加热溶液,它只有一个刻度线,也不能测量容量瓶规格以下的任意体积的液体。
(3)因无480 mL的容量瓶,配制NaOH溶液常用500 mL的容量瓶,m(NaOH)=c·V·M=0.1 mol/L×0.5 L×40 g/mol=2.0 g;定容仰视刻度线,造成加水较多,浓度偏低;洒落溶液会造成溶液浓度偏低。
(4)由稀释前后物质的量相等,V(浓)== L= L=13.6mL,选用15 mL量筒最好,误差小。稀释时将浓硫酸沿器壁缓缓倒入水中,并用玻璃棒不断搅拌。
答案 (1)A、C 烧杯、玻璃棒
(2)B、C、F
(3)2.0 小于 小于
(4)13.6 15 将浓硫酸沿器壁缓缓倒入水中,并用玻璃棒不断搅拌
14.(9分)(2010·辛集模拟)用Na2CO3·10H2O晶体,配制0.2 mol/L的Na2CO3溶液480 mL。
(1)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少__________________________;实验中两次用到玻璃棒,其作用分别是______________、________________。
(2)应称取Na2CO3·10H2O的晶体的质量:___
_____________________________________________________________________。
(3)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液
⑦定容
正确的操作顺序是__________________(填序号)。
(4)根据下列操作对所配溶液的浓度各有什么影响,完成填空。
①碳酸钠失去了部分结晶水 ②用“左码右物”的称量方法称量晶体 ③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈 ⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有____________,偏低的有______________,无影响的有
________。(填序号)
解析 (1)用Na2CO3·10H2O晶体配制Na2CO3溶液,需用到的玻璃仪器有量筒、烧杯、玻璃棒、500 mL容量瓶及胶头滴管;溶解时玻璃棒起搅拌作用,加速固体物质溶解,向容量瓶中转移液体时,玻璃棒起引流作用。
(2)m(Na2CO3·10H2O)=0.5 L×0.2 mol/L×286 g/mol=28.6 g
(4)①和④均使称得Na2CO3·10H2O晶体质量偏大,使配制结果偏高;②和③均使称得Na2CO3·10H2O晶体质量偏小,使配制结果偏低;⑤不影响容量瓶中溶质质量及溶液体积,因此对配制结果无影响。
答案 (1)500 mL容量瓶、胶头滴管 搅拌 引流
(2)28.6 g
(3)⑤①④⑥③⑦②
(4)①④ ②③ ⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com