
30.(18分)图1是某种生物细胞的示意图,I、2.3、4、1′、2′、3′、4′分别表示染色体,A、a、B、b分别表示所在染色体上控制一定-陆状的基因;图2表示细胞分裂过程中不同时期染色体数目的变化。请据图回答问题:
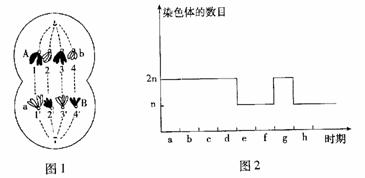
(1)假设该细胞为某高等动物的一个精原细胞,图1中有 个染色体组,其分式及时期是 ,对应图2中的 ,(用图中字母表示)时期,减数第二次分裂后期细胞的基因组成是 。若将该精原细胞的一个DNA分子(两条脱氧核苷酸链)用15N标记,正常情况下该细胞分裂形成的精细胞中含15N的精
细胞所占的比例为 。
(2)该生物的体细胞在有丝分裂的后期,基因的走向是
A.A与B走向细胞的一极,a和b走向细胞的另一极
B.与B走向细胞的一极,A与b走向细胞的另一极
C.A与a走向细胞的一极,B与b走向细胞的另一极
D.走向细胞两极的均为A、a、B、b
(3)若该细胞为某果蝇的一个细胞,基因A(灰身)对a(黑身)显性,B(长翅)对b(残翅)显性,两对基因分别位于两对常染色体上。现有表现型为灰身残翅和黑身长翅的纯合果蝇杂交,F1代雌雄个体间相互交配,则F2中与亲本表现型不同的个体所占比例为 ,与F1基因型相同的个体所占比例为 ,F2代中能稳定遗传的个体所占比例为 。
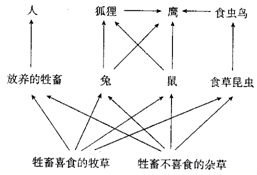 31.(16分)下图表示一个草原生态系统的营养结构,请据图回答问题。
31.(16分)下图表示一个草原生态系统的营养结构,请据图回答问题。
(1)该食物网包含了 条食物链,鹰处于第 营养级。
(2)优良牧草与杂草之间的关系主要表现为 。由于人口压力,许多草原存在 着过度放牧的现象,这种现象首先会导致 减少,若长期如此,草原将退化。要了解 某种优良牧草的种群密度,常用的调查方法是 。
(3)假设放养牧畜的食物90%来自牧畜喜食的牧草,且该系统能量从生产者到消费者的传递效率为10%,从消费者到消费者的能量传递效率为20%。如果人增加的能量为200KJ,那么其中来自牧畜喜食牧草的能量为 KJ。
(4)轻度放牧不会对草原生态系统造成破坏,原因是生态系统具有一定的 能力。草原生态系统与森林生态系统相比较,这种能力相对较小,原因是: 。
(5)该草原的原始植被为贝加尔针茅草原,开垦后种了几年玉米,后因产量下降而弃耕。弃耕一段时间后,该地区又逐渐恢复为贝加尔针茅草原。从群落变化的角度看,这一现象叫做 。
29.(16分)下图是将人的生长激素基因导人细菌细胞B制造工程菌的示意图。已知细菌细 胞B不含质粒A,也不含质粒A上的基因。质粒A导人细菌细胞B后,其上的基因能得到表达。请回答下列问题

(1)目的基因可通过PCR技术获取,这一技术中需要的酶是 。
(2)将目的基因与质粒结合形成重组质粒的过程中,需要的工具酶有 。
(3)若要检测目的基因是否导人,可在培养细菌B的培养基中加入 (氨卞青霉素/四环素),若在培养基上观察到大量细菌B的菌落,表明目的基因已成功导 人细菌B,此时所用的培养基属于 培养基(按用途分)。
(4)若要比较准确地了解转化率,一般可通过统计菌落的数目来推测活菌数目,还可以通过 的方法统计活菌数目;前者统计的活菌数目比实际的数目
(多/少/一样),原因是--。为了保证统计数目的准确,还应该设计 。
28.(16分)
根据废水中所含有害物质的不同,工业上有多种废水的处理方法。
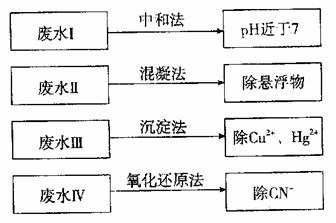
(1)①废水I若采用CO2处理,离子方程式是 。
②废水Ⅱ常用明矾处理。实践中发现废水中的c(HCO-3)越大,净水效果越好,这 是因为 。
③废水III中的汞元素存在如下转化(在空格上填相应的化学式):
Hg2++ =====CH3Hg++H+
我国规定,Hg2+的排放标准不能超过0.05 mg/L。若某工厂排放的废水1 L中含 Hg2+3×10-17mo1,是否达到了排放标准 (填“是”或“否”)。
④废水Ⅳ常用C12氧化CN-成CO2和N2,若参加反应的C12与CN-的物质的量之比 为5:2,则该反应的离子方程式为 。
(2)化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化刹的量,换算成氧的含量(以mg/L计)。某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
I.取V1mL水样于锥形瓶,加入10.00 mL 0.2500 mol/L K2Cr2O7溶液。
II.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热。
III.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液 滴定。终点时消耗硫酸亚铁铵溶液V2 mL。
①I中,量取K2Cr20,溶液的仪器是 。
②Ⅱ中,碎瓷片的作用是 。
③III中,发生的反应为:Cr2O2-7+6Fe2++14 H+==2Cr3++6Fe3+7H2O
由此可知,该水样的化学需氧量COD= (用含c、V1、V2的表达式表示)。
27.(12分)
钠米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。
 (1)工业上二氧化钛的制备是:
(1)工业上二氧化钛的制备是:
I.将干燥后的金红石(主要成分TiO2,主要
杂质SiO2)与碳粉混合装入氯化炉中,在高温
下通入Cl2反应制得混有SiCl4杂质的TiCl4。
II.将SiCl4分离,得到纯净的TiCl4。
III.在TiCl4中加水、加热,水解得到沉淀
TiO2·xH2O。
IV.TiO2·Xh2O高温分解得到TiO2。
①TiCl4与SiCl4在常温下的状态是 。II中所采取的操作名称是 。
②III中反应的化学方程式是 。
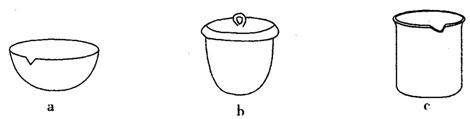
③如IV在实验室完成,应将TiO2·xH2O放在 (填仪器编号)中加热。
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O,其过程大致如下:
a. O2→2O b. O2+H2O→2OH(羟基) c. OH+OH→H2O2
①b中破坏的是 (填“极性共价键”或“非极性共价键”)。
②H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的 (填“氧化性”或“还原性”)。
(3)某研究小组用下列装置模拟“生态马路”部分原理。(夹持装置已略去)
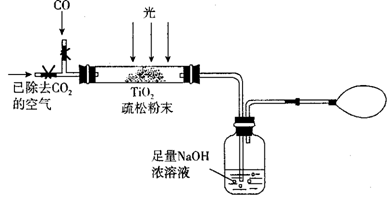
①如缓通入22.4L(已折算成标准状况)CO气体,结果NaOH溶液增重11g,则CO的转化率为 。
②当CO气体全部通入后,还要通一会儿空气,其目的是 。
26.(14分)
在下列物质转化关系中,反应的条件和部分产物已略去。
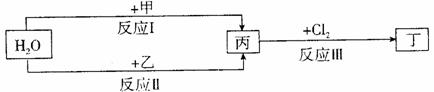
回答下列问题:
(1)若甲、乙是两种常见金属,反应Ⅲ是工业制盐酸的反应。
①反应I中,甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是 。
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中,乙与H2O在高温下反应,除丙外,还生成一种有磁性的物质,则反应Ⅱ的化学方程式是 。
③通过比较反应I、Ⅱ的反应条件,可得出甲的金属性比乙的金属性 (填 “强”或“弱”),比较二者金属性强弱的依据还可以是 (写出一种即可)。
(2)若甲、乙是化合物,且反应Ⅲ是工业制漂白粉的反应。
①反应Ⅲ的化学方程式是 。
②反应I的另一种产物为有机物,则该有机物的电子式是 。
③反应Ⅱ是化合反应。乙可与硫酸铵共热反应制氨气,则此反应的化学方程式是
。
④在饱和氯水中加块状石灰石,能制得较浓HCIO溶液,同时放出一种气体。其反应的离子方程式是 。
25.(16分)
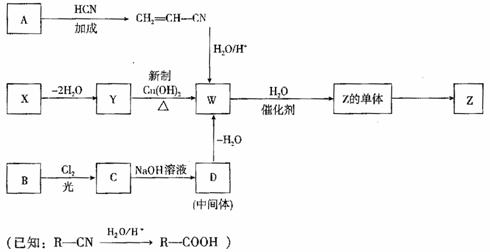 高分子化合物Z在食品、医疗方面有广泛应用。下列是合成Z的流程图:
高分子化合物Z在食品、医疗方面有广泛应用。下列是合成Z的流程图:
(1)烃A的结构简式是 。W中含有的官能团名称是 。
(2)X(C3H8O3)分子中每个碳原子上均连有相同的官能团,X的结构简式是 。
(3)B为烃。核磁共振氢谱显示:B、D均有三种类型氢原子的吸收峰,且峰面积之比均为1:2:3。则B生成C的化学方程式是 。
(4)①Z的单体分子中含甲基,由其生成Z的化学方程式是 。
②W可发生加聚反应,生成的高分子化合物的链节是 。
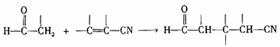 (5)戊二酸(HOOC-CH2一CH2一CH2一COOH)是合成树脂的引发剂。现以CH≡CH、CH3CH2OH、HCN为原料,设计合理方案合成戊二酸,用类似合成Z的流程图表示。
(5)戊二酸(HOOC-CH2一CH2一CH2一COOH)是合成树脂的引发剂。现以CH≡CH、CH3CH2OH、HCN为原料,设计合理方案合成戊二酸,用类似合成Z的流程图表示。
提示:
①
②合成过程中无机试剂任选。
24.(20分)
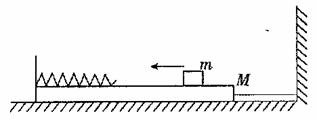
如图所示,质量为M的长方形木板静止在光滑水平面上,木板的左侧固定一劲度系数为k的轻质弹簧,木板的右侧用一根伸直的并且不可伸长的轻绳水平地连接在竖直墙上。 绳所能承受的最大拉力为T0一质量为m的小滑块以一定的速度在木板上无摩擦地向左运动,而后压缩弹簧。弹簧被压缩后所获得的弹性势能可用公式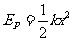 计算,k为劲度系数,z为弹簧的形变量。
计算,k为劲度系数,z为弹簧的形变量。
(1)若在小滑块压缩弹簧过程中轻绳始终未断,并且弹簧的形变量最大时,弹簧对木板 的弹力大小恰好为T,求此情况下小滑块压缩弹簧前的速度v0;
(2)若小滑块压缩弹簧前的速度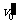 为已知量,并且大于(1)中所求的速度值
为已知量,并且大于(1)中所求的速度值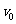 求此情 况下弹簧压缩量最大时,小滑块的速度;
求此情 况下弹簧压缩量最大时,小滑块的速度;
(3)若小滑块压缩弹簧前的速度人于(1)中所求的速度值v0,求小滑块最后离开木板时,相对地面速度为零的条件。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com