
7.下列关于人体血糖平衡调节的叙述中,不正确的是
A.血糖浓度较高时血液中胰岛素的含量会增加
B.血糖平衡是神经系统和体液共同调节的结果
C.正常人在吃甜食过多引起高血糖时,就会出现糖尿
D.降血糖的激素只有胰岛素,升血糖的激素有多种
6.关于人体体温及其调节的叙述,不正确的是
A.体温来源于体内物质代谢过程中所释放出来的热能
B.在寒冷环境下的体温调节有神经调节和体液调节
C.调节体温的主要中枢位于下丘脑
D.在炎热环境下人体的产热量总是小于散热量
5.水和无机盐的平衡对内环境稳态具有重要意义,下列关于人体内水盐平衡的叙述,正确的是
A.K+对维持细胞外液渗透压起决定性作用
B.Na+排出的特点是多吃多排,少吃少排,不吃也排
C.无机盐主要经肾脏随尿液排出体外
D.肾脏排尿的意义只是排出体内多余的水分
4.人在饥饿状态下,体内血液中
①葡萄糖浓度大幅度下降 ②葡萄糖浓度相对稳定 ③胰岛素含量减少
④胰岛素含量增加 ⑤胰高血糖素含量增加 ⑥胰高血糖素含量减少
A.①③⑥ B.②③⑥ C.①④⑤ D.②③⑤
3.在人体内环境中可以发生的生理过程是
A.抗体与相应的抗原发生特异性的结合 B.血浆蛋白的合成
C.丙酮酸氧化分解产生二氧化碳和水 D.食物中的淀粉消化分解成葡萄糖
2.有关人体内环境稳态的叙述,错误的是
A.有3种以上的生理系统参与维持人体内环境稳态
B.人体内环境稳态的失调与外界环境无关
C.人体维持内环境稳态的调节能力有限
D.稳态有利于参与其调节的器官保持机能正常
1.下列属于人体内环境或组成成分的是
①血浆、组织液和淋巴 ②激素、递质小泡和氨基酸
③葡萄糖、O2和胰岛素 ④血红蛋白、CO2和葡萄糖
A.①② B.①③ C.②④ D.③④
7.(2010天津卷)(14分)X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
⑴ L的元素符号为________ ;M在元素周期表中的位置为________________;五种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
⑵ Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___,B的结构式为____________。
⑶ 硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______,其最高价氧化物对应的水化物化学式为_______。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a.+99.7 mol·L-1 b.+29.7 mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
⑷ 用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式:______________;由R生成Q的化学方程式:_______________________________________________。
解析:(1)X、Y、Z、L是组成蛋白质的四种元素且原子序数依次增大,故分别为:H、C、N、O元素;M是地壳中含量最高的元素,为Al,其在周期表的位置为第3周第ⅢA族;再根据五种元素在周期表的位置,可知半径由大到小的顺序是:Al>C>N>O>H。
(2) N和H 1:3构成的分子为NH3,电子式为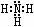 ;2:4构成的分子为N2H4,其结构式为
;2:4构成的分子为N2H4,其结构式为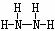 。
。
(3)Se比O多两个电子层,共4个电子层,1→4电子层上的电子数分别为:2、8 、18、6,故其原子序数为34;其最高价氧化物对应的水化物的化学式类似H2SO4,为H2SeO4。
非金属性越强,与氢气反应放出的热量越多,故2→5周期放出的热量依次是:d、c、b、a,则第四周期的Se对应的是b。
(4)Al作阳极失去电子生成Al3+,Al3++3HCO3-==Al(OH)3+3CO2,2Al(OH)3 Al2O3+3H2O。
Al2O3+3H2O。
2.(2010江苏卷)水是最宝贵的资源之一。下列表述正确的是
A.H2O的电子式为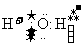
B.4℃时,纯水的pH=7
C.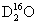 中,质量数之和是质子数之和的两倍
中,质量数之和是质子数之和的两倍
D.273K、101kPa,水分子间的平均距离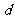 :
: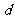 (气态)>
(气态)>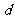 (液态)>
(液态)>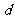 (固态)
(固态)
[答案]C
[解析]本题主要考查的是有关水的化学基本用语。A项,水是共价化合物,其分子的电子式为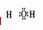 ;B项,温度升高,水的电离程度增大,
;B项,温度升高,水的电离程度增大,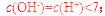 C项,一个
C项,一个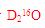 分子中,其质量数为20,质子数为10,D项,在温度压强一定时,它只能呈一种状态。综上分析可知,本题选C项
分子中,其质量数为20,质子数为10,D项,在温度压强一定时,它只能呈一种状态。综上分析可知,本题选C项
5.(2010上海卷)下列判断正确的是
A.酸酐一定是氧化物 B.晶体中一定存在化学键
C.碱性氧化物一定是金属氧化物 D.正四面体分子中键角一定是109o28′
答案:C
解析:此题考查了物质的分类、晶体的构造和分子的构型等知识点。酸酐中大多数是氧化物,但是醋酸酐(C4H6O3)就不是氧化物,A错;惰性气体都是单原子分子,其晶体中只存在分子间作用力,不存在化学键,B错;正四面体分子中,白磷分子的键角是60o,D错。
易混辨析:在化学学习中,有些化学概念极易混淆,比如氧化物和含氧化合物就不完全相同:氧化物由两种元素组成其中一种是氧元素,而含氧化合物只要组成中有氧元素即可,像醋酸酐是含氧化合物就不是氧化物。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com