
21.(9分)斯坦福大学B.M.Trost教授提出了绿色化学的核心概念--原子经济性。我们常用原子利用率来衡量化学反应过程的原子经济性,其计算公式为:

下面是新型自来水消毒剂ClO2的三种制备方法,请填空:
(1)氯酸钠和盐酸法:本方法的方程式为: 2NaClO3+4HCl= 2NaCl+2ClO2↑+Cl2↑+2H2O,此方法的原子利用率为 %(保留一位小数,下同)。
(2)电解亚氯酸钠法:本方法是用惰性电极电解亚氯酸钠溶液,原子利用率为62.2%,其阳极电极反应式为:ClO2--e-=ClO2,阴极电极反应式为: 。
(3)联合工艺法:本方法的反应原理由三步组成:
①电解氯化钠溶液NaCl+3H2O NaClO3+3H2↑
②氢气和氯气合成氯化氢
NaClO3+3H2↑
②氢气和氯气合成氯化氢
③生成二氧化氯2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O
此方法的原子利用率最大为 %。
吉安市高二下学期期末教学质量评价2010.6
20.(11分)信息I: 有机物的转化存在以下计量关系:
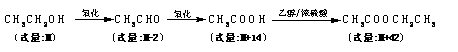

信息II: 芳香族有机物A、B、C、D、E、F之间存在如下转化关系:
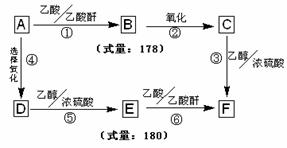
其中:有机物D不能使FeCl3溶液显紫色,它在浓硫酸作用下发生分子内脱水,可形成具有五元环状结构的有机物G。根据上述信息,完成下列问题:
(1)有机物A的分子式为: ;
(2)上述①-⑥转化关系中,属于取代反应的是: (填序号);
(3)请写出G的结构简式: ;
(4)A的一种芳香族类同分异构体H能与NaHCO3反应,则H共有 种结构;
(5)写出反应①的化学方程式: 。
19.(11分)某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色;J分子内有两个互为对位的取代基。在一定条件下各有机物间有如下转化关系:(无机物已略去,部分反应的条件未标明。)

(1)J中所含的含氧官能团的名称为____________________。
(2)E与H发生反应的化学方程式是: ;
反应类型是 。
(3)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物I,以I为单体合成的高分子化合物的名称是 。
(4)已知J有多种同分异构体,写出一种符合下列条件的J的同分异构体的结构简式 。
①与FeCl3溶液作用显紫色;
②与新制Cu(OH)2悬浊液作用产生红色沉淀;
③苯环上的一卤代物有2种。
18.(15分)某兴趣小组同学进行乙醛的银镜反应,实验操作步骤如下:
A.在试管里先注入少量NaOH溶液,振荡,然后加热煮沸。把NaOH溶液倒去后,再用蒸馏水洗净试管备用。 B.在洗净的试管里配制银氨溶液。C.沿试管壁加入乙醛稀溶液。
D.加热。请回答下列问题:
(1)步骤A中加NaOH溶液振荡,加热煮沸的目的是:
。
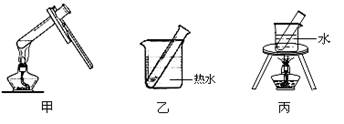
(2)步骤D应选择的加热方法是 (填下列装置编号),理由是
。
(3)乙醛发生银镜反应的化学方程式为:
。
(4)该兴趣小组的同学还对乙醛进行银镜反应的最佳实验条件进行了探究(部分实验数据如下表):
|
实验变量 实验序号 |
银氨溶液的量/mL |
乙醛的量/滴 |
温度/℃ |
反应混合液的pH |
出现银镜的时间/min |
|
1 |
1 |
3 |
65 |
11 |
5 |
|
2 |
1 |
3 |
45 |
11 |
6.5 |
|
3 |
1 |
5 |
65 |
11 |
4 |
①实验1和实验2,探究的是 。
②当银氨溶液的量为1 mL,乙醛的量为3滴,温度为55℃,反应混合液pH为11时,出现银镜的时间为 min。(填范围)
③你认为探究乙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成的银镜的 。
(5)银氨溶液放久后会产生氮化银而引起爆炸,直接排放会污染环境,且造成银资源的浪费。实验室从反应后的废液中(含过量的银氨溶液,假设不含银)回收银的实验流程如下:

已知:[Ag(NH3)2] 在溶液中存在平衡:[Ag(NH3)2]
在溶液中存在平衡:[Ag(NH3)2]
 Ag
Ag +2NH3。
+2NH3。
①写出废液与稀HNO3反应的离子方程式 。
②加入的铁粉要过量的目的是: 。
17.(6分)某市进行学业水平考试实验操作考查,试题分别为:
Ⅰ.试验维生素C的化学性质(主要是还原性)。
Ⅱ.葡萄糖与新制氢氧化铜的反应。
Ⅲ.配制一定物质的量浓度的氯化钠溶液。
⑴试题中设置了“评价与反思”,下列“评价与反思”不合理的是: 。(填序号)
A.应该由监考老师去评价与反思
B.实验结论告诉我:维生素C丸子应该密封保存
C.维生素C能使淀粉的碘溶液褪色
D.配制新制氢氧化铜时要将氢氧化钠与硫酸铜溶液等物质的量混合
E.实验Ⅲ中玻璃棒的作用是搅拌和引流
F.实验Ⅱ中的废水应该回收后再集中处理,不能直接倒入下水道
⑵实验Ⅲ中合理的实验操作顺序是:④ 。(填序号)
①溶解,②计算和称量,③转移和洗涤,④查漏,⑤定容和摇匀
⑶实验Ⅱ考查结束后,发现试管内壁附着一层红色固体。为了洗干净试管,某学习小组尝试往试管中加适量(3mL)稀硝酸,发现红色固体立即消失,溶液呈蓝色,则该反应的离子方程式为: 。
16.一定温度下m g下列物质在足量的氧气中充分燃烧后,产物与足量的Na2O2充分反应,过氧化钠增加n g,且n>m,符合要求的物质是( )
A.甲酸甲酯 B.乙醛 C.乙二酸 D.果糖
吉安市高二下学期期末教学质量评价2010.6
化 学 试 卷
|
座位号 |
|
|
|
|
第Ⅰ卷选择题答题栏(48分)
第Ⅱ卷(非选择题,共52分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com