
9.3黑3白共6个围棋子随意排成一行,其中恰有两个同色围棋子连在一起的概率为( )
A.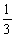 B.
B.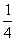
C.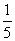 D.
D. 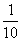
7.已知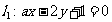 ,
,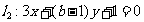 ,若
,若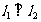 ,则
,则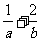 的最小值是( )
的最小值是( )
A.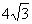 B.
B.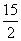 C.
C. D.
D.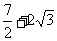
8/已知定义在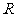 上的奇函数
上的奇函数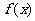 满足:对于任意
满足:对于任意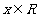 有
有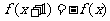 ,对于任意
,对于任意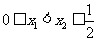 有
有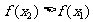 ,则下列各式中正确的是 ( )
,则下列各式中正确的是 ( )
A.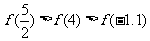 B.
B.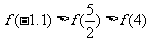
C.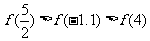 D.
D.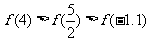
6.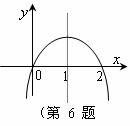 已知函数
已知函数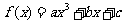 ,其导数
,其导数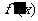 的图象如右图所示,
的图象如右图所示,
则 ( )
A.函数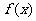 的有极小值
的有极小值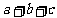
B.函数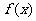 的有极小值
的有极小值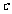
C.函数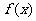 的有最大值
的有最大值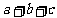
D.函数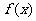 的有最大值
的有最大值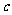
5.已知x、y满足 ,则
,则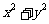 的最小值是 ( )
的最小值是 ( )
A.1
B.2 C. D.
D.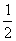
4.将函数 的图象沿向量
的图象沿向量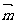 平移后得到函数
平移后得到函数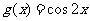 的图象,则
的图象,则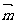 可以是 ( )
可以是 ( )
A.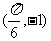 B.
B. 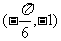 C.
C. D.
D.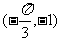
3.在等比数列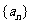 中,
中, ,其中
,其中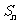 为其前
为其前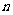 项和,则
项和,则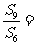 ( )
( )
A.13 B.9 C.3
D.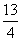
2.若集合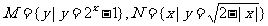 ,则
,则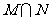 = ( )
= ( )
A.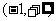 B.
B.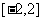 C.
C.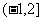 D.
D.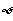
1.点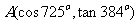 在 ( )
在 ( )
A.第一象限 B.第二象限 C.第三象限 D.第四象限
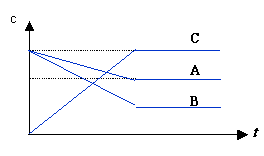
12. 某一反应在一定条件下充分反应,一段时间后C、A、B之间的关系如图所示。试判断该反应的化学方程式及A的转化率。
 13.合成氨工厂常通过测定反应前后混合气体的密度来确定氮的转化率。某工厂测得合成塔中N2、H2混合气体的密度为0.5536g/L(标准状况),从合成塔中出来的混合气体在相同条件下密度为0.693g/L。求该合成氨厂氮气的转化率。
13.合成氨工厂常通过测定反应前后混合气体的密度来确定氮的转化率。某工厂测得合成塔中N2、H2混合气体的密度为0.5536g/L(标准状况),从合成塔中出来的混合气体在相同条件下密度为0.693g/L。求该合成氨厂氮气的转化率。
解析:设起始时N2、H2总物质的量为 ,其中
,其中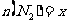 ,
,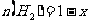 。
。
根据平均分子量的公式,得:
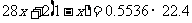
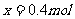
∴ 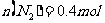


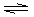

起 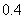
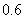
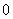
转

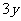
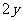
平 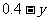
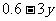
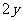
∴ 平衡时气体的总物质的量为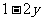 。
。
又∵ 反应前后气体的总质量不变,得:
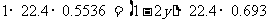
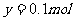
∴ 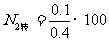 %
% %
%
答案:氮气的转化率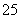 % 。
% 。
11.某化学反应2A=B+D在四种不同条件下进行。B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
|
实验序号 |
|
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
|
2 |
800℃ |
C2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
|
3 |
800℃ |
C3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
(1)在实验1,反应在10至20分钟时间内平均速率为 mol·(L·min)-1。
(2)在实验2,A的初始浓度c2=__________mol·L-1 ,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是__________。
,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是__________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3__________v1(填“>”“=”或“<”=,且c3__________1.0 mol·L-1(填“<”“=”或“>”)。
(4)比较实验4和实验1,可推测该反应是__________反应(填“吸热”或“放热”)。
解析:(1)vA=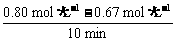 =0.013 mol·(L·min)-1
=0.013 mol·(L·min)-1
(2)对比实验1与实验2可知,反应温度相同,达平衡时的A的浓度相同,说明是同一平衡状态,即c2=1.0 mol·L-1,又因实际反应的速率快,达平衡所需时间短,说明反应中使用了催化剂。
(3)对比实验3与实验1可知,从10 min到20 min,实验1的A的浓度变化值为0.13 mol·L-1,而实验3的A的浓度变化值为0.17 mol·L-1,这就说明了v3>v1。又知从0 min到10 min A的浓度的变化值应大于0.17 mol·L-1,即c3>(0.92+0.17)mol·L-1=1.09 mol·L-1。
(4)对比实验4与实验1可知,两实验的起始浓度相同,反应温度不同,达平衡时实验4的A的浓度小,说明了实验4 A进行的程度大,即温度越高,A的转化率越大,说明正反应为吸热反应。
答案:(1)0.013 (2)1.0 催化剂 (3)> > (4)吸热
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com