
30、(6分)环境问题是人类可持续发展必须解决的一个重要问题,温室效应被列为21世纪人类面临的最大威胁之一,已引起人们的广泛关注。旨在限制发达国家温室气体排放量、抑制全球范围内气候持续变暖的《京都议定书》,已于2005年2月16日正式生效。为减缓二氧化碳使全球变暖的趋势,有科学家提出大胆设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰冷的深海中。但也有科学家担心海水中富含二氧化碳后酸度会增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,同时气候变化也可能改变海洋环流,把海底的二氧化碳又带回海面,另外把二氧化碳压入海底所消耗的能源可能会再增加二氧化碳的排放。 ①二氧化碳在深海中的溶解度比在通常状况下的水中的溶解度 ,
原因是
②海水中富含二氧化碳后酸度会增加原因是: (方程式表示) ③我国科学家陈乾旺等最新研究成果表明,在440 ℃和800大气压条件下,二氧化碳和金属钠反应产生金刚石和碳酸钠,合成的金刚石最大达1.2 mm,完全可以满足工业用途。二氧化碳与金属钠反应生成金刚石和碳酸钠的化学方程式为: 。
①计算分析:
▲▲
▲▲
②结论:原白色固体的成分为 ▲
28.(10分)柠檬酸为无色半透明晶体,无臭、味极酸,易溶于水和乙醇,在潮湿空气中易潮解。水溶液显酸性,加热可以分解成多种产物,与酸、碱等发生反应。主要用于香料或作为饮料的酸化剂。
(1)上述划线部分属于柠檬酸的 ▲ (物理、化学)性质。
(2)柠檬酸(C6H8O7)在氧气中完全燃烧的化学方程式: ▲ 。
(3)工业上柠檬酸由蔗糖发酵制得,发生的主要反应为:
C12H22O11 + 3 A =====2C6H8O7 + 3H2O,A的化学式是 ▲ 。
(4)食品加工业中,可以用压制柑橘所得汁液作为提取柠檬酸的原料。提取过程如下:
①原料提取:柑橘汁液中有不少果胶及固体杂质,需进行初步提纯,自然沉降后用压滤机进行▲ 获得澄清液体。
 ②中和:在①所得原料澄清液中加入石灰浆,至溶液呈青绿色时,即表示已完成中和反应。然后静置沉淀,此沉淀即为果酸钙(以柠檬酸钙为主)。 若用H3R表示柠檬酸的化学式,请书写该中和反应的化学方程式
▲ 。
②中和:在①所得原料澄清液中加入石灰浆,至溶液呈青绿色时,即表示已完成中和反应。然后静置沉淀,此沉淀即为果酸钙(以柠檬酸钙为主)。 若用H3R表示柠檬酸的化学式,请书写该中和反应的化学方程式
▲ 。
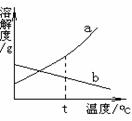
③除盐:所得柠檬酸钙中含有某种盐分,可用70-
80℃热水洗涤,反复多次,直至盐分除净为
止。请根据操作分析该盐分的溶解度曲线可能
是右图中 ▲ 。
④酸解脱色:柠檬酸钙浆液与浓度为35%的硫酸充分反应,静置沉淀,上层清液为柠檬酸溶液,此反应属于 ▲ (填基本反应类型);将暗红色
的柠檬酸用 ▲ 脱色得无色清液。配制35%的硫酸5000g,需要
98%的浓硫酸(密度为1.84g/ mL) ▲ mL。
⑤浓缩结晶:将不饱和柠檬酸液进行恒温浓缩结晶。在此过程中,保持不变的是 ▲ (填写字母):
a.溶液中溶剂的质量 b. 柠檬酸的溶解度
c.溶液中溶质的质量分数 d. 溶液和晶体中柠檬酸总质量
步骤1:收集瓶口处白色固体,加热 ;
步骤2:取该白色固体样品3g;
步骤3:将固体溶于水后,滴入稀盐酸到不再产生气泡;
步骤4:测出收集到气体的质量为1.1g
27.(14分)氢氧化钠是一种重要化工原料,也是实验室中常见的化学药品。
[观察](1)实验室中盛放氢氧化钠溶液的试剂瓶是 ▲ (a、细口瓶;b、广口瓶),瓶塞是 ▲ (a、橡皮塞;b、玻璃塞)。
(2)盛放氢氧化钠溶液的试剂瓶的瓶口有白色固体。
[解释]形成白色固体的原因是: ▲ 。
[问题]白色固体中含有哪些物质?
[资料](1)NaOH和 Na2CO3 受热不分解;
(2)NaOH的熔点为318.4℃,沸点为1390℃;Na2CO3的熔点为851℃。
[设计与实验](请你帮助甲、丙实验小组完成实验报告)
实验小组甲:
|
实验过程与数据 |
分析与结论 |
|
(1)取3g白色固体,加热 (2)冷却后称得固体的质量为2.9g |
白色固体中含有 ▲ |
实验小组乙:
|
实验步骤 与现象 |
分析与结论 |
|
(1)取少量样品,溶于水中 (2)滴入澄清的石灰水产生白色沉淀,继续滴加至不再产生白色沉淀为止,过滤 (3)在滤液中加入无色酚酞,溶液显红色 |
原白色固体中 一定含有NaOH和 Na2CO3 |
实验小组丙:
|
实验步骤 |
实验现象 |
分析与结论 |
|
(1)取少量样品,溶于水 (2)滴入CaCl2溶液 (3)继续滴入CaCl2溶液到不再产生沉淀, ▲ (操作名称 ) (4) ▲ |
▲ ▲ |
原白色固体中一定含有 Na2CO3,一定不含NaOH |
[交流与评价]
三个实验小组代表汇报了各自的实验及其结论后,老师肯定了小组甲和小组丙的实验探究,同时指出了实验小组乙中存在的错误。这个错误是: ▲ 。
[拓展]老师提供了一个可证明原白色固体中成分的探究示例:
26.(5分)请根据下列装置图,回答有关问题:

(1) 实验室用B、C装置制取二氧化碳的化学方程式为 ▲
(2) 若用高锰酸钾制取氧气,可选用的发生装置是 ▲ (填字母)。
(3) 实验室收集氢气可用D或E装置的原因分别是 ▲ 、
▲ 。
(4) 实验室收集二氧化碳时,验满的方法是 ▲ 。
25.(8分)甲、乙、丙都属于氧化物;M是一种不含有金属元素的盐,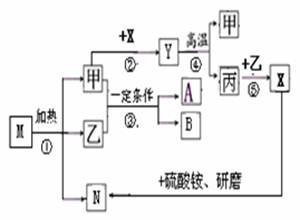 是常见的化学肥料;A、B是生命活动中不可缺少的物质,其中A属于单质。它们有如下图的转化关系:
是常见的化学肥料;A、B是生命活动中不可缺少的物质,其中A属于单质。它们有如下图的转化关系:
(1)写出下列物质的化学式:
M是 ▲ 、N是 ▲
A是 ▲ 、丙是 ▲ ;
(2)反应③发生的条件是 ▲ ;
(3)写出有关反应的化学方程式:
② ▲ 、
⑤ ▲ ;
(4)举例说明物质X在生产生活中的应用 ▲ (一种即可)。
24.(6分)2009年“中国水周”活动的宣传主题为“落实科学发展观,节约保护水资源”。
(1) 水 ▲ (选填:“属于”或“不属于”)六大类营养素之一。
(2) 珍惜水、保护水,让水造福人类。作为青少年,下列生活习惯应该摒弃的是 ▲ 。
A.用盆接水洗菜 B.用养鱼水浇花草C.使用节水龙头 D.丢弃未喝完的矿泉水瓶
(3) ①监测某工厂排放污水的酸碱度,可选用 ▲ 进行测定。方法是 ▲ 。
②配制0.5%的某消毒溶液,主要玻璃仪器有烧杯,玻棒,量筒, ▲ 。
23.(4分)从H、C、O、Ca四种元素中,选择适当元素填写符合下列要求的化学式(各写一个):
(1)相对分子质量最小的氧化物 ▲ ; (2)具有还原性的气态氧化物 ▲ ;
(3)白糖、红糖主要成分的化学式 ▲ ; (4)可用作补钙剂的盐 ▲ ;
22. (5分)在日常生活生产中,我们要合理地使用化学物质,请在“生石灰、硫酸铜、醋酸、干冰、熟石灰、聚乙烯塑料”中选择合适的物质名称填空:
(1)常用来改良酸性土壤的碱 ▲ ;(2)食醋中含有的酸 ▲ ;
(3)常用作袋装食品干燥剂的是 ▲ ;(4)常用于人工降雨的是 ▲ ;
(5) 通常用于食品包装材料的是 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com