
25.向铜片中加入某浓度的硫酸120 mL,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500 mL,再加入足量锌粉,使之充分反应收集到标准状况下氢气2.24 L,过滤残留固体,干燥后称量,质量减轻了7.5 g。
⑴求溶解的铜的质量。 ⑵求原硫酸的物质的量浓度。
泸县二中2010年春期高2012级期末考试
24.(10分)下图是元素周期表中1-20号元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:
(a)B、C、I是非金属单质,其中C、I在常温常压下是固体;
(b)反应①、②是化工生产中的重要反应,生成的E、F均为两种元素组成的气态化合物,其中F是形成酸雨的污染物之一。
(c)化合物A能形成喀斯特洞穴中石笋、石钟乳等景观。

请回答:
(1)用化学式表示:A为 ,H为 ;
(2)上述用字母所表示的物质中属于离子化合物的是 (填字母)。
(3)反应F+B→G的化学方程式为 ;
反应H(浓)+I→E+F的化学方程式为 。
23.(9分)在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是 ;用电子式表示X与氢元素形成化合物的过程: 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是: ,D与E能形成一种结构类似于二氧化碳的分子,该分子式为 。
(3)元素R与Y同主族,其氢化物能用于刻蚀玻璃,刻蚀玻璃时发生的化学方程式是: 。
(4)E元素常形成E22-离子,其电子式为 ,与E22-离子电子数相等的气态单质分子的化学式为 。
22.(8分)一包白色固体物质,可能由Na2SO4、Na2SO3、CuSO4、CaCl2、Na2SiO3中的一种或几种组成,其实验现象如下:
①取少量白色固体加入适量水,得到无色溶液。
②取①所得的溶液少量,滴入稀硫酸,有带刺激性气味气体放出,同时产生白色沉淀。
③另取①所得的溶液,加入氯化钡溶液,有白色沉淀生成,再加入足量稀盐酸,沉淀部分溶解。
根据上述实验现象,回答以下问题。
(1)原白色固体中肯定存在的物质是 ;不能肯定是否存在的物质是 。
(2)写出实验③中沉淀溶解的反应的离子方程式。
(3)用最简单的实验方法进一步确定未肯定的物质是否存在。
21.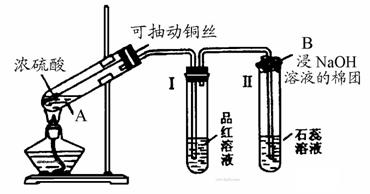 (15分)浓硫酸与铜的反应用了右图所示的装置,请回答下列问题。
(15分)浓硫酸与铜的反应用了右图所示的装置,请回答下列问题。
(1)Ⅰ中的现象是 ;装置Ⅱ用来证明SO2是 氧化物。
(2)写出A处反应的化学方程式 ;
B处反应的离子方程式 。
(3)反应结束,待试管A内液体冷却后,将试管中的液体慢慢倒入一只盛有少量水的烧杯中,观察溶液的颜色。这一步操作的目的是要证实 。
(4)B中除用碱液外,还可用一种 (填化学式)等物质代替。
你所选用的代用物吸收SO2的化学反应方程式为: 。
(5)在本实验中,要简单地使反应停止,其操作方法是 。
31.(2010山东卷)(8分)[化学-----化学与技术]
玻璃钢可由酚醛树脂和玻璃纤维制成。
(1)酚醛树脂有苯酚和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向已有苯酚的反应釜中____加入甲醛,且反应釜应装有____装置。K^S*5U.C#O%下
(2)玻璃纤维由玻璃拉丝得到。普通玻璃是由石英砂、______和石灰石(或长石)高温熔融而成,主要反应的化学方程式为_____________________________________。
(3)玻璃钢中玻璃纤维的作用是__________。玻璃钢具有___________等优异性能(写出亮点即可)。
(4)下列处理废旧热固性酚醛塑料的做法合理的是_________。
a.深埋 b.粉碎后用作树脂填料
c.用作燃料 d.用有机溶剂将其溶解,回收树脂
解析:(1)为防止温度过高,应间歇性加入甲醛,并且有散热装置
(2) 利用碱石灰、纯碱、石英砂生成波兰的方程式为
Na2CO3+SiO2 Na2SiO3+CO2 CaCO3+SiO2
Na2SiO3+CO2 CaCO3+SiO2 CaSiO3+CO2
CaSiO3+CO2
(3) 玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料,其中玻璃纤维的作用是增强体 ,合成材料是基体;他的优点有: 强度高、质量轻、耐腐蚀、抗冲击、绝缘性能好等优良性能
(4)废旧合成材料的再生利用主要是三条途径:①通过再生和改性,重新做成多种有用的材料和制品;②采用热裂解或化学处理方法使其分解,用于制备多种化工原料;③将废旧的聚合物作为燃料回收利用热能;故b、c正确。因为塑料深埋地下一百年也不会腐烂,造成严重的白色污染,故a错;酚醛塑料不能溶解于有机溶剂,故d错。
6.(2010四川理综卷)节能减排对发展经济、保护环境有重要意义。下列措施不能减少二氧化碳排放的是
A.利用太阳能制氢 B.关停小火电企业
C.举行“地球一小时”熄灯活动 D.推广使用煤液化技术
答案:D
解析:本题考查化学与社会的关系;利用太阳能制氢,减少了化石燃料的使用,同时也减少了CO2的排放,A项符合;火力发电消耗大量的煤炭资源,同时会排放出CO2及有害气体,关停小火电企业,有利用节能减排,B项符合;举行“地球一小时”熄灯活动有效的节约的能源, C项符合; 煤液化技术,提高了煤的利用率,但不能减少CO2的排放,D项不符合。
4.(2010上海卷)下列有关物质性质的描述不符合事实的是
A.有机物不导电 B.金刚石是自然界最硬的物质
C.SO2可用作食品防腐剂 D.NO可用于某些疾病的治疗
答案:A
解析:此题考查了常见物质的性质。大多数的有机物不导电,但聚乙炔塑料就能导电,A错;金刚石是自然界中最硬的物质,B对;二氧化硫可做食品和干果的防腐剂,C对;NO可用于心血管疾病的治疗,D对。
易错警示:有机物是一类特殊的有机物,在理解其性质注意描述中的一般指的是大多数的有机物,在理解时绝对话极易造成错误理解。比如有机物都不导电、有机物都不是电解质等。
1.(2010上海卷)下列做法不能体现低碳生活的是
A.减少食物加工过程 B.注意节约用电
C.尽量购买本地的、当季的食物 D.大量使用薪柴为燃料
答案:D
解析:此题考查了化学与生产生活的联系。低碳生活的核心是减少二氧化碳的排放,减少食物加工过程,减少二氧化碳排放,能体现,排除A;目前电力的主要来源是火电,节约用电能减少二氧化碳排放,能体现,排除B;本地食物能减少运输消耗、当季食物能减少贮存的能量消耗,能体现,排除C;薪柴为燃料能产生大量二氧化碳,不能体现低碳思想,符合要求。
易错警示:解答此题的易错点是不能准确理解“低碳”的含义,而造成错误选择。由于二氧化碳气体的大量排放,地球气候异常表现的越来越显著,对人类生活的影响也越来越大,故此在生产生活中要尽可能节约能源,减少二氧化碳排放。
6. 答案D
[解析]本题考查反应中产生的温室气体。A项,制玻璃的反应为:Na2CO3+SiO2
 Na2SiO3+CO2;B项,碳燃烧可产生CO2气体;C项,铁矿石与C或CO反应可生成CO2;这三项均生成CO2,即产生温室气体。D项,NH3与CO2反应生成(NH4)2CO3,没有产生CO2。
Na2SiO3+CO2;B项,碳燃烧可产生CO2气体;C项,铁矿石与C或CO反应可生成CO2;这三项均生成CO2,即产生温室气体。D项,NH3与CO2反应生成(NH4)2CO3,没有产生CO2。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com