
32.(6分)最后一空2分,答AC得1分,答C得2分,其他每空1分
(1)CH4+H2O CO+3H2
CO+3H2
(2)①CO2+Ca(OH)2=CaCO3↓+H2O
②3CO+Fe2O3 3CO2+2Fe
3CO2+2Fe
③吸收水分,除去二氧化碳
④C
32.(6分)一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料合成一系列化工原料和燃料的化学。下图为一碳化学的一种简易流程,回答下列问题:
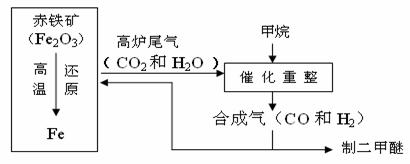
(1)利用高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为 。
(2)课外小组的同学从上述流程中收集到一瓶“合成气”,用下图所示装置进行研究(已知高温条件下,甲烷和氧化铁反应生成CO2和H2O,3H2 +Fe2O3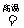 3H2O + 2Fe),以确定“合成气”的成分。
3H2O + 2Fe),以确定“合成气”的成分。

①A中澄清石灰水变浑浊,反应的化学方程式为 。
②C中一氧化碳与氧化铁反应的化学方程式为 。
③B装置中盛有足量的氢氧化钠颗粒,其作用是 。
④实验测量D和E的质量反应后分别增加9.0g和8.8g,推测原混合气体的组成为(假设混合气在C装置中反应完全) (填字母)。
A.CO、H2、CO2 B.CO、H2、CH4 C.CO、H2、CH4、CO2 D.CO2、H2、CH4
33. (7分,每空l分。)
(1)Na2CO3+Ca(OH)2==== CaCO3↓+2NaOH
(2)假设四不合理,因为氢氧化钙溶液与碳酸钠溶液不能共存。
(3)若氢氧化钙过量与氯化钙不发生反应
(4)
|
实 验 步 骤 |
实 验 现 象 和 结 论 |
|
取甲同学实验后的清液放在试管中,在通入足量的二氧化碳(或滴入Na2CO3溶液),观察 |
溶液无变化,则不含氢氧化钙 |
|
溶液变浑浊,则含氢氧化钙 |
(5)10% 6.5%
顺义区
33. (7分) 工业用碳酸钠溶液与石灰水反应制烧碱。对于碳酸钠溶液与石灰水是否恰好完全反应,化学小组同学将其产物进行过滤,并对滤液进行如下探究。
提出假设:假设一:滤液中只含氢氧化钠
假设二:滤液中含氢氧化钠和氢氧化钙
假设三:滤液中含氢氧化钠和碳酸钠
假设四:滤液中含氢氧化钠、氢氧化钙和碳酸钠
甲同学设计了如下实验方案:已知:Na2CO3 + CaCl2= 2NaCl+CaCO3↓(白色)
|
实验步骤 |
实验现象 |
结论 |
|
取少量滤液放在试管中,再滴入氯化钙溶液 |
若生成白色沉淀 |
碳酸钠过量 |
|
若无明显现象 |
恰好反应 |
试回答:
(1)写出碳酸钠溶液与石灰水反应的化学方程式 。
(2)哪种假设不合理,试说明理由 。
(3)乙同学认为甲同学设计方案还不能说明碳酸钠溶液和澄清石灰水恰好完全反应,她的理由
是 。
(4)丙同学认为要说明碳酸钠溶液与石灰水是否恰好完全反应,还需在甲同学实验方案的基础
上进行实验。她的实验方案是:
|
实验步骤 |
实验现象和结论 |
|
|
|
|
|
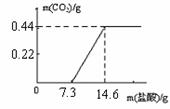 (5)取18.6g氢氧化钠样品(样品中的杂质是碳酸钠),加水溶解得到溶液A,取A溶液的1/10向其中逐滴加入一定浓度的稀盐酸,并同时记录放出CO2的质量和消耗盐酸的质量(所得数据如右图)。试计算:
(5)取18.6g氢氧化钠样品(样品中的杂质是碳酸钠),加水溶解得到溶液A,取A溶液的1/10向其中逐滴加入一定浓度的稀盐酸,并同时记录放出CO2的质量和消耗盐酸的质量(所得数据如右图)。试计算:
①盐酸中溶质的质量分数为 。
②样品中碳元素的质量分数为 。
32.(5分,每空l分。)
(1)瘪气球逐渐涨大 2 NaOH+CO2 = Na2CO3+H2O
(2)2HCl+Fe = FeCl2+H2↑ C装置中的稀盐酸流入B装置中,B装置中铁逐渐减少,表面有气泡,溶液由无色变成浅绿色;C装置的稀盐酸中有气泡冒出。
(3)a c b
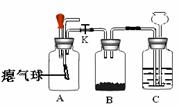
32.(5分)老师用右图所示装置为同学们做了一个实验。A装置中装有体积比约为3:1的空气和二氧化碳的混合气;B装置中
盛有足量铁粉;C装置中盛有足量的稀盐酸。
(1)关闭活塞K,当将A装置中胶头滴管里足量的浓氢氧化钠
溶液挤入瓶中,可以观察到A装置中的现象是 ;A装置发生反应的化学方程式为 。
(2)立即打开活塞K,一段时间后,关闭活塞K。B装置中发生反应的化学方程式为 ;在整个实验过程中,可以观察到装置B、C中的实验现象是 。
(3)C装置的作用是 (填字母)。
a.提供药品 b.控制气体总量 c.调节装置内的压强 d.可用来储存气体
33.(共8分,每空1分)
(1)猜想:O2 CO2(或CO、CH4等)
实验:用带火星木条试验,木条复燃。(或将气体通入石灰水,石灰水变浑浊等)
(2)① 过滤 使溶液中的氯化铜完全反应
Fe + CuCl2 = FeCl2 + Cu(或Zn + CuCl2 = ZnCl2 + Cu等)
② 使过量的A完全除去 溶液中不再有气泡产生
 昌平
昌平
33.(8分)已知一种固体化合物由氢、氧、碳、铜四种元素组成,向盛有该化合物的试管
中加入稀盐酸时,固体逐渐溶解,有大量气泡产生,得到蓝绿色的氯化铜溶液。
(1)探究产生的气体是什么。
猜想:①可能是氢气;② ▲ ;③ ▲ ……
实验:请针对你②和③猜想中的一种,设计实验方案,验证你的猜想 ▲ 。
(2)从蓝绿色溶液中提取金属铜。有关实验方案如下:

①操作Ⅰ的名称为 ▲ ;加入过量A的目的是 ▲ ;
有关反应的化学方程式为 ▲ 。
②操作II中加入足量B的目的是 ▲ ;确定此目的已经达到的依据是 ▲ 。
32. (共5分,每空1分)
(共5分,每空1分)
(1)① 4P + 5O2 2P2O5
 ② 有大量白烟产生,水由导气管流入集气瓶中,体积约为其容积的1/5
② 有大量白烟产生,水由导气管流入集气瓶中,体积约为其容积的1/5
(2)① Fe2O3 + 3CO 2Fe + 3CO2
② 缺少尾气处理装置(或应加上尾气处理装置)
③ 检验一氧化碳是否发生反应和吸收其产物二氧化碳
32.(5分)根据下表内容进行活动与探究,请你参与并回答问题:
|
实验名称 |
实验设计 |
问题与结论 |
||
|
(1) 空气中氧气 含量的测定 |
(燃烧匙中的药品为红磷) |
①该实验应用的化学方程式为: ▲ ; ②实验中应该观察到的现象是: ▲ 。 |
||

|
一氧化碳还
原氧化铁
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com