
2.复数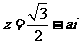 ,
,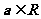 ,且
,且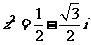 ,则
,则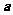 的值为
( )
的值为
( )
A. B.
B.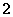 C.
C.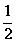 D.
D.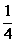
1.设集合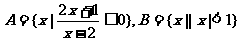 ,则
,则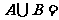 ( )
( )
A.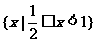 B.
B.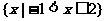
C.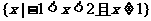 D.
D.
38、神舟系列飞船的成功发射和顺利回收标志着我国载人航天技术的研究已经进入世界领先行列,许多航天技术问题不断地被科学家研究解决,如:如何保证宇宙飞船燃料补给;如何提供在往返路程中宇航员呼吸所需要的氧气和消除呼吸过程中产生的二氧化碳等。请回答下列问题:
(1)下表是星体上“大气”(相当于地球上的空气)的主要成分。它们中可能成为宇宙飞船燃料补给站的星体是: ▲
|
星体名称 |
星体是“大气”主要成分 |
|
金星 |
二氧化碳、硫酸 |
|
火星 |
二氧化碳 |
|
冥王星 |
甲烷 |
(2)科学家发现在宇宙飞船飞过冥王星“大气”时,甲烷并没有被点燃,请分析其原因: ▲
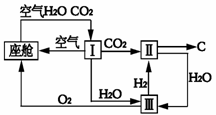 (3)新型航天飞行器座舱内空气更新过程如右图所示:
(3)新型航天飞行器座舱内空气更新过程如右图所示:
A:装置Ⅱ是CO2和H2的反应装置,该反应的化学
方程式为 ▲ (可不写反应条件)。
B:从装置Ⅰ、Ⅱ、Ⅲ可看出,O2的来源是CO2和
H2O,若宇航员每天呼出的气体中含1012gCO2和
180g水蒸气,则通过Ⅰ、Ⅱ、Ⅲ装置完全转化后可
得到O2 ▲ g。
37、杭州市是著名的国家级旅游风景区,如图所示的是在西湖边行驶的电动观光车,有关技术参数如下表。
|
空车质量 |
1180kg |
电动机额定功率 |
4kw |
|
满载乘员 |
11人 |
电动机额定电压 |
48V |
|
轮胎与地接触面积 |
4×250cm2 |
最大车速 |
45km/h |
|
电动机效率 |
80% |
平路续驶里程 |
≤80km |
根据技术参数,求解下列问题:
(1)设乘员质量均为60kg,求满载时车对水平路面的压强。
(2)电动机以额定功率工作半小时消耗多少电能?若这一过程中,观光车以36km/h的速度沿水平路面匀速行驶,求车在行驶过程中受到的阻力。
35、 右图是某一农田生态系统示意图,请据图回答:
右图是某一农田生态系统示意图,请据图回答:
(1)该生态系统中,非生物成分除了水、空气、土壤外,还应该有_______ 。
(2)请将下列生物与在生态系统中所起的相应作用
之间连线。
生物 作用
禾谷类 分解者
昆虫、野兔、鹰 生产者
细菌、真菌 消费者
(3)仔细观察该图,试写出一条食物链:_______________________________ 。
⑷该区域经常使用某长效有机磷杀虫剂,可在生态系统中造成富集,这一杀虫剂的残留物质将会在图中所示的 体内浓度最高。
⑸在维护这一农田生态系统过程中,你有什么合理化的建议?(写出二点)
|
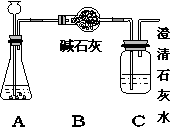 36、某化学学习小组用足量
36、某化学学习小组用足量
的稀盐酸对15g石灰石样品
(杂质不溶于水且不与酸反
应)进行科学探究。实验装
置如下:
有关数据如下:
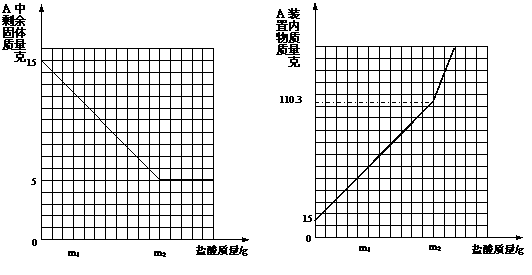
当A装置中无气体产生时测得B装置的质量增加了4.7g;C装置的质量没发生变化且无明显现象。请你回答:
(1)石灰石样品中碳酸钙的质量为 g。
(2)15g样品最多能生成二氧化碳气体的质量为 g。
(3)所用稀盐酸的溶质质量分数是多少?写出计算过程。

34、2009年世界环境日纪念活动在墨西哥举行,环境日主题为“地球需要你:团结起来应对气候变化”,而“温室效应”是引起气候变化的一个主要原因。某科学探究小组为探究影响大气“温室效应”的因素,进行太阳光照射下N2 、O2、CO2及空气温室效应强度的比较实验。请你参与他们制取N2 、O2、CO2过程,填写有关空格。
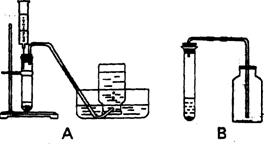 (1)用500mL集气瓶装满一瓶空气。
(1)用500mL集气瓶装满一瓶空气。
(2)另取一个500mL的集气瓶,采用 ▲ 法收集从液氮瓶中放出的N2。
(3)现用右图中装置A分别制取一瓶O2和一瓶CO2(均为500 mL); 则制取O2反应的化学方程式为 ▲ , 制取CO2反应的化学方程式为 ▲ 。该实验制取O2和CO2,与用装置B相比较,用装置A的优点(写出一点) ▲。
33、受蒙古气旋和冷空气影响,2010年3月19日至20日,我国出现今年以来最强的一次沙尘暴天气过程。金华也出现了多年不见的浮尘天气,空气质量为“重污染”。所谓沙尘暴可简化为如下情景:快速向上刮起的大风将大量沙尘颗粒扬起后悬浮在空中(不动),这时风对沙尘的作用力与沙尘的重力平衡,其作用力大小可近似表达为F=ρSV2,其中ρ为空气密度,S为沙尘颗粒的横截面积,V为风速。如果沙粒的密度ρ沙为3×103千克/米3,沙粒半径r为2.5×10-4米,地面的空气密度ρ0为1.25千克/米3,那么要形成沙尘暴现象,地面的风速至少为 ▲ 米/秒。(沙粒可近似看成球体,且体积V = πr3)。
32、雷利是英国物理学家,他曾用下列两种方法测定氮气的密度。
方法一:将除去水蒸气和二氧化碳的空气通过烧红的装有铜屑的玻璃管,使空气中的氧气全部除去,测得氮气的密度为1.2572kg/L。
方法二:将氨气(NH3)通过赤热的装有氧化铜的玻璃管,生成氮气和水蒸气,除去水蒸气后测得氮气的密度为1.2508g/L。若两次测定的状况相同,请问:
(1)方法二中发生反应的化学方程式为 ▲ ;
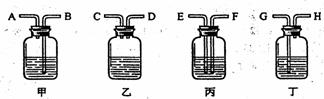 (2)欲除去空气中的水蒸气和二氧化碳,可供选择的装置如下图所示(不可重复使用),在你选择的装置中,用相应的字母表示导管口的连接顺序____▲____。
(2)欲除去空气中的水蒸气和二氧化碳,可供选择的装置如下图所示(不可重复使用),在你选择的装置中,用相应的字母表示导管口的连接顺序____▲____。
(3)请分析两种方法所测定的氮气密度数值不同的原因?__________▲___________________。
31、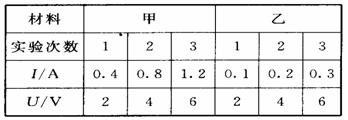 在探究导体的导电能力与材料关系的实验时,某小组的同学选取了导电能力不受温度影响的材料甲和乙,它们的长度、横截面积均相同,分别测出通过它们的电流与它们两端的电压。记录数据如下表所示:
在探究导体的导电能力与材料关系的实验时,某小组的同学选取了导电能力不受温度影响的材料甲和乙,它们的长度、横截面积均相同,分别测出通过它们的电流与它们两端的电压。记录数据如下表所示:
分析数据发现,每次实验中,通过材料甲、乙的电流与其两端电压的比值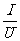 都相等。同学们把电流与电压的比值
都相等。同学们把电流与电压的比值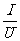 叫做“a”。
叫做“a”。
(1)“a”值越大,表明导体的导电能力越____▲____。如果把材料乙均匀拉长,其“a”值将______▲_____ (填“增大”、“不变”或“减小”)。
(2)进一步归纳能得出的结论是:当电压一定时,导体中的电流与“a”的关系是____▲_____。
(3)如果要从材料甲、乙中选择一种做输电用的导线,你建议应该选择材料_____▲____。
30、纯碱(Na2CO3)属于盐,向纯碱溶液中滴入酚酞试液,溶液变成红色,说明纯碱溶液呈碱性,其pH>7,我国科学家侯德榜创造了一种著名的纯碱生产方法“联合制碱法”。
(1)“联合制碱法”生产过程可用化学方程式简要表示为:
① NH3+CO2+H2O==NH4HCO3
② NH4 HCO3+NaCl==NaHCO3 ↓+NH4Cl
③ 2NaHCO3==Na2CO3+H2O+CO2 ↑
该过程中没有涉及的基本反应类型是( ▲ )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(2)第②步中加入的是磨细的食盐粉。食盐磨细的目的是:_____▲______。
(3)将第②步所得滤液(NH4Cl与剩余NaCI的混合溶液)降温,NH4Cl晶体大量析出,而NaCl却仍留在了溶液中。你认为NH4Cl先结晶的原因可能是:_____▲_____。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com