
8.下列化学式既能表示物质的组成,又能表示物质的一个分子的是
A.NaOH B.SiO2 C.Fe D.C2H4
7.下列变化中,不需要破坏化学键的是
A.碘升华 B.加热氯酸钾使其分解 C.氯化氢溶于水 D.氯化钠溶于水
6.下列实验不能作为判断依据的是
A.钠和镁分别与冷水反应,判断钠和镁金属性强弱
B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属性强弱
C.硅酸钠溶液中通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱
D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属性强弱
5. 右图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是
右图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是
A.X的氢化物比R的氢化物稳定
B.原子半径大小顺序是Z>Y>X>R
C.Z的单质能与Y的某些化合物发生置换反应
D.X、Z可形成化合物XZ 5,分子中各原子均满足最外层8电子结构
4.下列说法或物质性质的比较中正确的是
A.同周期元素的原子,半径越小越容易失去电子
B.所有主族元素的最高正化合价数与它的族序数数值相等
C.酸性:H2CO3<H3PO4<H2SO4<HClO4
D.热稳定性:SiH4>NH3>H2O>HF
3.运用元素周期律可以分析、推断某些元素的一些性质,但下列推断中有明显错误的是
A.氢氧化铍[Be(OH)2]的碱性比氢氧化镁弱
B.单质砹(At)为有色固体, AgAt不溶于水也不溶于稀酸
C.硫酸锶(SrSO4)是难溶于水的白色固体
D.硒化氢(H2Se)是无色、有毒,比H2S稳定的气体
2.下列说法中,不正确的是
A.溴的非金属性比氯强 B.钠的金属性比镁强
C.硝酸的酸性比磷酸强 D.水的热稳定性比氨强
1.对元素周期表和元素周期律的发现有突出贡献的科学家是 A.拉瓦锡 B.阿伏加德罗 C.门捷列夫 D.道尔顿
24.已知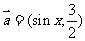 ,
, .
.
(1)若 求
求 的值;(2)设
的值;(2)设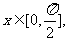 求
求 的最小值。
的最小值。
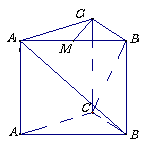 25
25 (本小题满分8分)如图,直三棱柱
(本小题满分8分)如图,直三棱柱 中,
中, ,
,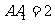 ,
, ,
M是A1B1的中点
,
M是A1B1的中点
(1) 求证C1M^平面 ;
;
(2) 求异面直线 与
与 所成角的余弦值
所成角的余弦值
22.(本小题满分8分)设等差数列 的前
的前 项和为
项和为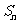 , 已知
, 已知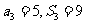 .
.
(Ⅰ)求首项 和公差
和公差 的值; (Ⅱ)若
的值; (Ⅱ)若 ,求
,求 的值.
的值.
23 (本小题满分8分)求圆心在直线4 x
+ y = 0上,并过点P(4,1),Q(2,-1)的圆的方程
(本小题满分8分)求圆心在直线4 x
+ y = 0上,并过点P(4,1),Q(2,-1)的圆的方程
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com