
28.下列各分子中所有原子都满足最外层为8电子结构的是 A. BeCl2 B. PCl3 C. PCl5 D. N2
27.二氧化碳固体俗称干冰,下列说法正确的是 A.二氧化碳分子不可再分
B.干冰升华需要破坏共价键
C二氧化碳分子由碳原子和氧气分子构成
D.二氧化碳分子是保持干冰化学性质的最小微粒
26.下列化合物中,阳离子半径与阴离子半径的比值,最小的是 A.NaCl B.BeI2 C.LiBr D.LiI
25.下列不能说明氯的非金属性比硫强的事实是 A. HCl受热不分解,H2S受热分解 B.向H2S的水溶液中通入氯气溶液变浑浊,反应方程式为H2S+Cl2==S↓+2HCl C.与Na化合时,硫显-2价,氯显-1价 D.与Fe化合时,硫将Fe氧化至+2价,氯将Fe氧化至+3价
24.下列实验不能达到预期目的的是
|
代号 |
实验内容 |
实验目的 |
|
A |
Cl2、Br2分别与H2反应 |
比较氯与溴的非金属性强弱 |
|
B |
向饱和Na2SiO3溶液中通入二氧化碳 |
比较碳与硅的非金属性强弱 |
|
C |
把碳酸钠与亚硫酸钠放置在空气中 |
比较碳与硫的还原性强弱 |
|
D |
向氯化铜溶液中加入铁丝 |
比较铁与铜的还原性强弱 |
23.短周期元素X、Y、Z在元素周期表中的位置如右下图所示,下列说法正确的是( )
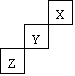 A.X、Y、Z三种元素中,X的非金属性最强
A.X、Y、Z三种元素中,X的非金属性最强
B.Y的氢化物的稳定性比Z的弱
C.Y的最高正化合价为+7
D.X的单质的熔点比Z的低
22.下列说法正确的是 A.ⅦA族元素的非金属性一定比ⅥA族元素的非金属性强 B.第三周期元素的阳离子半径从左到右逐渐减小 C.ⅥA族元素的氢化物中,因为H2O的沸点最高,所以其稳定性也最好 D.同周期非金属氧化物对应的水化物的酸性从左到右依次增强
21.几种短周期元素的原子半径和主要化合价见下表,下列有关说法中,正确的是
|
元素代号 |
X |
Y |
Z |
L |
M |
Q |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.099 |
0.077 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+7、-1 |
+4、-4 |
-2 |
A.等物质的量的X、Y的单质与足量盐酸反应,生成H2一样多 B.Y与Q形成的化合物不可能跟氢氧化钠溶液反应 C.Z的氢化物的稳定性强于L的氢化物的稳定性 D.在化学反应中,M原子与其它原子易形成共价键而不易形成离子键
20.门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是: A.X单质不易与水反应 B.XO2可被碳或氢还原为X C.XCl4的沸点比SiCl4的高 D.XH4的稳定性比SiH4的高
19.短周期元素中,原子最外电子层只有1个或2个电子的元素
A.是非金属元素 B.是稀有气体元素 C.是金属元素 D.无法确认为哪一类元素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com