
1.(2010上海文数)已知集合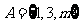 ,
, ,
,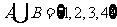 则
则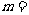 2 。
2 。
解析:考查并集的概念,显然m=2
35.(6分)(1)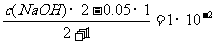 ,c(NaOH) = 4×10-2mol/L;
,c(NaOH) = 4×10-2mol/L;
(2)20mL×c(HA) = 12.5mL×4×10-2mol/L,c(HA) = 2.5×10-2mol/L;
(3)Ka = 
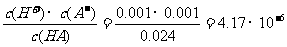
34.(6分)(解:设第一次平衡时(即1min时),有a mol 的X转化为Z。
 X(g) + Y(g)
X(g) + Y(g)  2Z(g)
2Z(g)
 开始时: 2 2 0
开始时: 2 2 0
 变化量: a a 2
a
变化量: a a 2
a
 平衡时:2-a 2-a 2 a
平衡时:2-a 2-a 2 a
 第一次平衡时,
第一次平衡时, 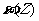 =
=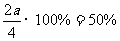 ,故a=1(1分)
,故a=1(1分)
 (1)v(X)=
(1)v(X)=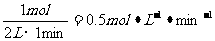
 (1分)
(1分)
 (2)K=
(2)K=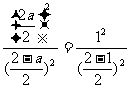 =4(1分)(未用浓度表示即K=
=4(1分)(未用浓度表示即K= =4不给分)
=4不给分)
 (3) 2min时,
(3) 2min时, 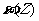 =
=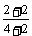 ×100%=66.7%
×100%=66.7%
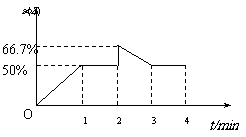
 由于反应前后气体的分子数不变,所以加入
由于反应前后气体的分子数不变,所以加入
 2mol Z重新达到平衡时,Z的体积分数与第一
2mol Z重新达到平衡时,Z的体积分数与第一
 次平衡时相同 ,即为50%(1分),画图完全
次平衡时相同 ,即为50%(1分),画图完全
 正确给2分(若画出4min后不扣分,但必须正确)
正确给2分(若画出4min后不扣分,但必须正确)
33.(10分)Ⅰ.(1)甲基橙 黄 橙 (2)1000W/53V
Ⅱ.(2)碱式滴定管(或移液管来)
(3)滴定过程中,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶中溶液颜色的变化,直到滴定终点。
(4)V(NaOH)=10.00mL V(HCl)=[(20.40mL-0.50mL)+(24.10mL-4.00)]/2=20.00mL
根据:c(NaOH)V(NaOH)=c(HCl)V(HCl) 则:c(NaOH)=0.4000mol/L
(5)样品中m(NaOH)=0.4000mol/L×0.250L×40g/mol=4.00g
则烧碱的纯度为:4.0g/5.0g×100%=80.00%
32. (7分)(1)溶液由蓝色变为紫色,最后变为粉红色(1分,未写全颜色变化不给分)
(7分)(1)溶液由蓝色变为紫色,最后变为粉红色(1分,未写全颜色变化不给分)
 存在平衡CoCl42- +6H2O
存在平衡CoCl42- +6H2O 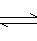 Co(H2O)62+
+4Cl-,加水使平衡向正反应方向移动(2分,平衡表达式1分,其余语言描述1分,只要写出平衡表达式和说明平衡向正反应方向移动就给2分,能进行说明紫色更好)
Co(H2O)62+
+4Cl-,加水使平衡向正反应方向移动(2分,平衡表达式1分,其余语言描述1分,只要写出平衡表达式和说明平衡向正反应方向移动就给2分,能进行说明紫色更好)
 K=
K=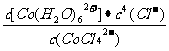 (2分,将水写入表达式中不给分)
(2分,将水写入表达式中不给分)
 (2)<(1分)
变小(1分,不按要求书写不给分)
(2)<(1分)
变小(1分,不按要求书写不给分)
31.(9分)(1)量筒、温度计(2)否;金属易导热,热量散失导致误差大。
(3)①-56.8(或-56.85)KJ/mol
②NaOH (aq) + HCl(aq) = NaCl(aq) + H2O(l) △H=-56.8KJ/mol(用离子方程式表达也可)
(4)NH3·H2O是弱电解质,电离需要吸热
30.(5分)(1)c2<c1<c3或c3>c1>c2; (2)V1=V2<V3; (3)n1=n3>n2;
(4)υ1 = υ2 =υ3 ;υa = υb <υc。
29.(6分)(1)10-14 ,10-12 ; (2)2∶9; (3)0.004。
28.(8分)(1)放热 > (2) 增大 (3)增大 减小
(4) 减小 (5)变深 变浅
27.(7分)(1)Cu,AgNO3 (2)正极,Ag+ +e-=Ag↓,Cu-2e-=Cu2+ (3)铜,银
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com