
25、(天津一中2010届高三上学期第三次月考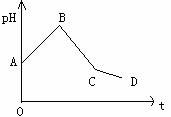 ,13)将等物质的量浓度的CuSO4和NaCl等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如右图,则下列说法正确的是:
,13)将等物质的量浓度的CuSO4和NaCl等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如右图,则下列说法正确的是:
A.阳极产物一定是Cl2,阴极产物一定是Cu
B.BC段表示在阴极上是H+放电产生了H2
C.整个过程中阳极先产生Cl2,后产生O2
D.CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+
24、(2010年苏、锡、常、镇四市高三教学情况调查一,12)下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+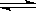 AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
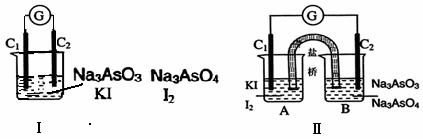
下列叙述中正确的是
A.甲组操作时,微安表(G)指针发生偏转
B.甲组操作时,溶液颜色变深
C.乙组操作时,C2做正极
D.乙组操作时,C1上发生的电极反应为I2 +2e-=2I-
23、(江苏省南京市2010届高三第二次模拟考试,6)A、B、C、D、E、F为原子序数依次增大的短周期元素,其中A与E同主族,B与F同主族,E与F同周期,已知常温下A、E单质的状态不同,D原子的核电荷数是B原子最外层电子数的2倍,F单质是一种重要的半导体材料。下列说法正确的是( )
A.原子半径由达到小的顺序是: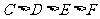
B.由A、C、D三种元素组成的化合物中可能含有离子键
C.F、C、B元素最高价氧化物对应的水化物的酸性依次增强
D.F与D形成的化合物质地坚硬,既不与酸反应也不与碱反应
高频考点八 电化学问题
22、(福建省永春一中、培元中学、季延中学、石光华侨联中2010届高三上学期期末联考,6)四种短周期元素X、Y、Z、W在元素周期表中的相对位置如下表所示,Y、Z质子数
之和为21,下列说法中不正确的是 ( )
|
B.X、Y、W的氢化物中,Y的氢化物沸点最高
C.Z的阳离子与Y的阴离子电子层结构相同
D.W元素的简单离子半径大于Z元素的简单离子半径
21、(山东省实验中学2010届高三第二次诊断性测试,12)X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
B.元素X不能与元素Y形成化合物X2Y2
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
D.元素W、R的最高价氧化物的水化物都是强酸
20、(2010海淀区高三年级第二学期适应性练习,9)下表是元素周期表的一部分,有关说法正确的是
|
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
||||||
|
2 |
|
|
|
a |
b |
|
|
||||||
|
3 |
d |
e |
f |
g |
|
h |
i |
①a、b、e、f四种元素的元素的原子半径:e > f > b > a
②h、i两种元素阴离子的还原性:h > i
③a、g两种元素氢化物的稳定性:a > g
④d、e、f三种元素最高价氧化物对应的水化物的碱性依次增强
⑤八种元素中d元素的单质还原性最强,i元素的单质氧化性最强
A.①③④ B.②③⑤ C.②④⑤ D.①③⑤
19、(山东省潍坊市2010届高三教学质量抽样检测C,5)核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪组原子均可产生NMR现象 ( )
A.18O 31P B.19F 12C
C.元素周期表中IIIA族所有元素的原子 D.元素周期表中第三周期元素的所有原子
18、(福建省上杭一中、武平一中、长汀一中2010届高三上学期期末联考,9)已知在酸性条件下能发生下列反应:Cu+→Cu+Cu2+(未配平)。NH4CuSO3与足量的10 mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法一定合理的是
A. 该反应显示硫酸具有酸性
B. NH4CuSO3中硫元素被氧化
C. 刺激性气味的气体是氨气
D. 反应中硫酸作氧化剂
高频考点七 原子结构 元素周期律与化学键
17、(浙江省绍兴一中2009-2010学年第一学期高三期末调测,15)Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是 ( )
A.Na2O2只作氧化剂
B.Na2FeO4既是氧化产物又是还原产物
C.O2是还原产物
D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移
16、(安徽省合肥市2010年高三第一次教学质量检测,8)甲醇广泛用作燃料电池的燃料,可用天然气来合成,已知:
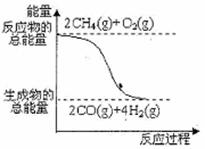 ①2CH4(g)+O2(g)=2CO(g)+4H2(g); △H=-71kJ·mol-1
①2CH4(g)+O2(g)=2CO(g)+4H2(g); △H=-71kJ·mol-1
②CO(g)+2H2(g)=CH3OH(l) ; △H=-90.5kJ·mol-1
下列描述错误的是( )
A.CO(g)+2H2(g)==CH3OH(g)
△H>-90.5kJ·mol-1
B.在甲醇燃料电池中,甲醇所在电极为正极
C.CH4(g)+1/2o2(g)===CH3(OH)(l)
△H=-126kJ·mol-1
D.反应①中的能量变化如右图所示
高频考点六 氧化还原反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com