
29.(15分)请设计CO2在高温下与木炭反应生成CO的实验。
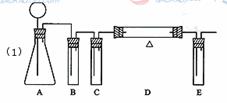
(1)在下面方框中,A表示有长颈漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置,连接胶管及尾气处理不分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如下:
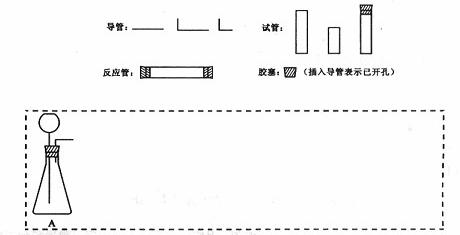
(2)根据方框中的装置图,在答题卡上填写该表
|
仪器符号 |
仪器中所加物质 |
作用 |
|
A |
石灰石、稀盐酸 |
石灰石与盐酸生成CO2 |
|
|
|
|
(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中。改进后的优点是 ;
(4)验证CO的方法是 。
[解析](1)这里与一般的物质制备思路是一致的,思路是先制备CO2,再净化除杂,干燥,接着再与C在高温下反应制CO,再除去未反应完的CO2,我们这里只需要画装置简图即可,这是自1998年高考科研测试首次出现,至今高考终于再现了!(见答案)
(2)与2009年27题相似这在今年的训练题中比较流行,如湖北省部分重点中学联考,黄冈中学模拟题等均再现了,不难学生能够作答和得分(见答案)
(3)这在以前题目中出现了多次,一般学生能答对
(4)此问答案很多可以点燃,看火焰看产物;也可以E后面再接个灼热CuO的玻璃管后面再接个放澄清石灰水的洗气瓶,看玻璃管和石灰水的现象;也可应直接用PdCl2溶液等
[答案]

(3) 可以通过控制加酸的量,来控制气体产生的快慢;同时小试管中充满盐酸,可以起到液封的作用,防止反应剧烈时气体经漏斗冲出
(4) 点燃气体,火焰呈蓝色,再用一个内壁附着有澄清石灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊
[命题意图]实验综合能力考查,主要考查实验方案的设计,仪器的组装,装置图的绘制,试剂的合理选择,装置的改进及评价,物质的的检验等
[点评]前面已经说过本题与2009年的27题思路一致,不过能力要求更高,学生最不会就是这种设计型的实验,去年的是个雏形,改革不彻底,实验原理早在前些年高考里面考过两次,并且学生都能动笔!今年提供的题目原理并不复杂,思路显然不唯一,因而提供的参考答案并不完美,例如(1)E后面再连接其他算不算错?(2)E中吸收CO2用澄清石灰石似乎不合理(考过多遍,浓度低,效果差,应用NaOH之类强碱),考生用用其他得不得分?(4)检验CO超纲,且答案不唯一,学生用其他合理答案能否得分?这些都是大家所关注的,希望能够引起命题人的注意,不要人为的制造不公平,一些优秀考生反而不能得分!
28.(15分)有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五中溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1) 能确定溶液是(写出溶液标号与相应溶质的化学式):
(2) 不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:
[解析](I)由题干表述可知A和E不是盐,又由纯E为无色油状液体,推知E为硫酸(③步操作进一步确定);(II)由题干和①步操作可知A为氨水; (III)再由②步操作可知F中阳离子为Ag+发生的反应为:Ag++NH3·H2O=AgOH↓+NH4+;AgOH+2NH3·H2O=[Ag(NH3)2]++OH-+2H2O;而常见的盐中只有AgNO3可溶于水,故F为AgNO3;(IV)由③步操作可知B中阴离子应为CO32-,由于此无色无味的气体只能是CO2, B、C、D中能生成沉淀说明不能是HCO3-,而阳离子可是常见的K+、Na+、NH4+等待定(V)同样由②步操作D中能与氨水生成沉淀的无色溶液中常见的为阳离子为Mg2+或Al3+,而阴离子需待下步反应再确定;(VI)由④步操作生成的沉淀为可能为AgCl、AgBr、AgI、BaSO4、H2SiO3(不合理)等,但限于题干所述中学常用试剂,则沉淀应为AgCl和BaSO4,才不溶于HNO3,一个是与AgNO3结合生成的沉淀,一个是与硫酸结合形成的沉淀,故C应该同时含有Ba2+和Cl-即,C为BaCl2,进而推出D中阴离子应该为SO42-,因为题干所述盐溶液中阴离子均不同,故D为Al2(SO4)3或MgSO4其他解析见答案
[答案](1)A NH3·H2O或NH3 ;E H2SO4 F AgNO3 C BaCl2
若C作为不能确定的溶液,进一步鉴别的方法合理,同样给分
(2)B Na2CO3或K2CO3 用洁净的铂丝蘸取少量B,在酒精灯火焰中灼烧,若焰色呈黄色则B为Na2CO3溶液;若透过蓝色钴玻璃观察焰色呈紫色,则B为K2CO3溶液
D Al2(SO4)3或MgSO4 取少量D,向其中滴加NaOH溶液有沉淀生成,继续滴加过量的NaOH溶液,若沉淀溶解,则D为Al2(SO4)3溶液,若沉淀不溶解,则D为MgSO4溶液
[命题意图]考查学生的分析与综合能力,涉及到无机元素及其化合物的性质,离子反应,未知物的推断,物质的检验,常见物质量多与量少的反应不同,现象不同等,此题综合性强,难度大,区分度很好,是一道不可多得的经典好题!
[点评]此题一改过去每年元素推断的通病,思维容量显著增大能力要求高,与2008年全国卷I理综28题有得一拼,比2009年的第29题出得高超一些,相比以前的无机推断显然有质的飞跃,看到命题人在进步!但是此题是不是一点瑕疵没有呢?x显然不是,例如本题条件很宽广,没太明显的限制条件,因而答案是丰富多彩的,这不会给阅卷者带来喜出望外,只会增加难度,不好统一评分标准,也就缺乏公平性!特别是B和C上就有争议,如B还可能是(NH4)2CO3,C还可能是BaBr2、BaI2等,当然限制一下沉淀颜色就排除了C的歧义!
27.(15分)在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为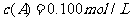 、
、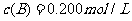 及
及 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。
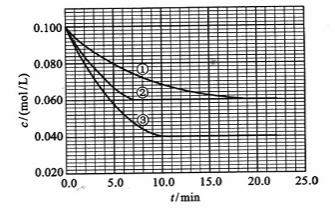
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②_______________;
③_______________;
(2)实验②平衡时B的转化率为_________;实验③平衡时C的浓度为____________;
(3)该反应的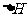 _________0,判断其理由是__________________________________;
_________0,判断其理由是__________________________________;
(4)该反应进行到4.0min时的平均反应速度率:
实验②: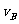 =__________________________________;
=__________________________________;
实验③: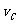 =__________________________________。
=__________________________________。
[解析](1)②使用了(正)催化剂;理由:因为从图像可看出,两者最终的平衡浓度相同,即最终的平衡状态相同,而②比①所需要的时间短,显然反应速率加快了,故由影响反应速率和影响平衡的因素可知是加入(正)催化剂;③升高温度;理由:因为该反应是在溶液中进行的反应,所以不可能是改变压强引起速率的改变,又由于各物质起始浓度相同,故不可能是改变浓度影响反应速率,再由于③和①相比达平衡所需时间短,平衡时浓度更小,故不可能是改用催化剂,而只能是升高温度来影响反应速率的
(2)不妨令溶液为1L,则②中达平衡时A转化了0.04mol,由反应计量数可知B转化了0.08mol,所以B转化率为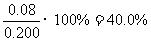 ;同样在③中A转化了0.06mol,则生成C为0.06mol,体积不变,即平衡时C(c)=0.06mol/L
;同样在③中A转化了0.06mol,则生成C为0.06mol,体积不变,即平衡时C(c)=0.06mol/L
(3) 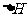 ﹥0;理由:由③和①进行对比可知升高温度后A的平衡浓度减小,即A的转化率升高,平衡向正方向移动,而升温是向吸热的方向移动,所以正反应是吸热反应,
﹥0;理由:由③和①进行对比可知升高温度后A的平衡浓度减小,即A的转化率升高,平衡向正方向移动,而升温是向吸热的方向移动,所以正反应是吸热反应,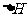 ﹥0
﹥0
(4)从图上读数,进行到4.0min时,实验②的A的浓度为:0.072mol/L,则△C(A)=0.10-0.072=0.028mol/L,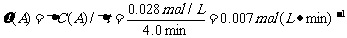 ,∴
,∴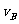 =2
=2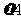 =0.014mol(L·min)-1;进行到4.0mi实验③的A的浓度为:0.064mol/L:△C(A,)
=0.10-0.064=0.036mol/L,
=0.014mol(L·min)-1;进行到4.0mi实验③的A的浓度为:0.064mol/L:△C(A,)
=0.10-0.064=0.036mol/L,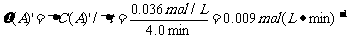 ,∴
,∴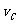 =
=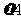 =0.0089mol(L·min)-1
=0.0089mol(L·min)-1
[答案](1)②加催化剂;达到平衡的时间缩短,平衡时A的浓度未变
③温度升高;达到平衡的时间缩短,平衡时A的浓度减小
(2)40%(或0.4);0.06mol/L;(3)﹥;升高温度向正方向移动,故该反应是吸热反应
(4)0.014mol(L·min)-1;0.008mol(L·min)-1
[命题意图]考查基本理论中的化学反应速率化学平衡部分,一些具体考点是:易通过图像分析比较得出影响化学反应速率和化学平衡的具体因素(如:浓度,压强,温度,催化剂等)、反应速率的计算、平衡转化率的计算,平衡浓度的计算,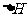 的判断;以及计算能力,分析能力,观察能力和文字表述能力等的全方位考查。
的判断;以及计算能力,分析能力,观察能力和文字表述能力等的全方位考查。
[点评]本题所涉及的化学知识非常基础,但是能力要求非常高,观察和分析不到位,就不能准确的表述和计算,要想此题得满分必须非常优秀才行!此题与2009年全国卷II理综第27题,及安微卷理综第28题都极为相似,有异曲同工之妙,所以对考生不陌生!
26.(21分)
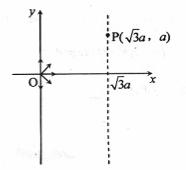 如下图,在
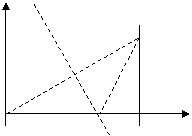
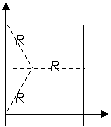
如下图,在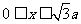 区域内存在与xy平面垂直的匀强磁场,磁感应强度的大小为B.在t=0时刻,一位于坐标原点的粒子源在xy平面内发射出大量同种带电粒子,所有粒子的初速度大小相同,方向与y轴正方向的夹角分布在0-180°范围内。已知沿y轴正方向发射的粒子在
区域内存在与xy平面垂直的匀强磁场,磁感应强度的大小为B.在t=0时刻,一位于坐标原点的粒子源在xy平面内发射出大量同种带电粒子,所有粒子的初速度大小相同,方向与y轴正方向的夹角分布在0-180°范围内。已知沿y轴正方向发射的粒子在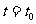 时刻刚好从磁场边界上
时刻刚好从磁场边界上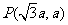 点离开磁场。求:
点离开磁场。求:
⑴ 粒子在磁场中做圆周运动的半径R及粒子的比荷q/m;
⑵ 此时刻仍在磁场中的粒子的初速度方向与y轴正方向夹角的取值范围;
⑶ 从粒子发射到全部粒子离开磁场所用的时间。
[答案]⑴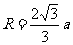
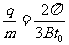
⑵速度与y轴的正方向的夹角范围是60°到120°
⑶从粒子发射到全部离开所用 时间 为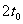
[解析] ⑴粒子沿y轴的正方向进入磁场,从P点经过做OP的垂直平分线与x轴的交点为圆心,根据直角三角形有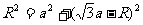
解得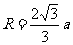
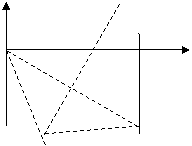
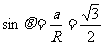 ,则粒子做圆周运动的的圆心角为120°,周期为
,则粒子做圆周运动的的圆心角为120°,周期为
粒子做圆周运动的向心力由洛仑兹力提供,根据牛顿第二定律得
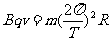 ,
,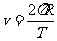 ,化简得
,化简得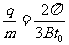
⑵仍在磁场中的粒子其圆心角一定大于120°,这样粒子角度最小时从磁场右边界穿出;角度最大时从磁场左边界穿出。
角度最小时从磁场右边界穿出圆心角120°,所经过圆弧的弦与⑴中相等穿出点如图,根据弦与半径、x轴的夹角都是30°,所以此时速度与y轴的正方向的夹角是60°。
角度最大时从磁场左边界穿出,半径与y轴的的夹角是60°,则此时速度与y轴的正方向的夹角是120°。
 所以速度与y轴的正方向的夹角范围是60°到120°
所以速度与y轴的正方向的夹角范围是60°到120°
⑶在磁场中运动时间最长的粒子的轨迹应该与磁场的右边界相切,在三角形中两个相等的腰为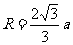 ,而它的高是
,而它的高是
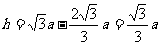 ,半径与y轴的的夹角是30°,这种粒子的圆心角是240°。所用 时间 为
,半径与y轴的的夹角是30°,这种粒子的圆心角是240°。所用 时间 为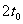 。
。
所以从粒子发射到全部离开所用 时间 为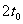 。
。
25.(18分)
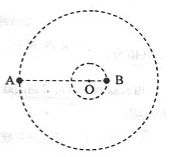 如右图,质量分别为m和M的两个星球A和B在引力作用下都绕O点做匀速周运动,星球A和B两者中心之间距离为L。已知A、B的中心和O三点始终共线,A和B分别在O的两侧。引力常数为G。
如右图,质量分别为m和M的两个星球A和B在引力作用下都绕O点做匀速周运动,星球A和B两者中心之间距离为L。已知A、B的中心和O三点始终共线,A和B分别在O的两侧。引力常数为G。
⑴ 求两星球做圆周运动的周期。
⑵ 在地月系统中,若忽略其它星球的影响,可以将月球和地球看成上述星球A和B,月球绕其轨道中心运行为的周期记为T1。但在近似处理问题时,常常认为月球是绕地心做圆周运动的,这样算得的运行周期T2。已知地球和月球的质量分别为5.98×1024kg 和 7.35 ×1022kg 。求T2与T1两者平方之比。(结果保留3位小数)
[答案]⑴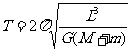 ⑵1.01
⑵1.01
[解析] ⑴A和B绕O做匀速圆周运动,它们之间的万有引力提供向心力,则A和B的向心力相等。且A和B和O始终共线,说明A和B有相同的角速度和周期。因此有
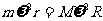 ,
,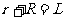 ,连立解得
,连立解得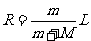 ,
,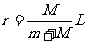
对A根据牛顿第二定律和万有引力定律得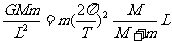
化简得 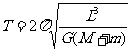
⑵将地月看成双星,由⑴得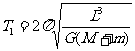
将月球看作绕地心做圆周运动,根据牛顿第二定律和万有引力定律得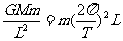
化简得 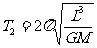
所以两种周期的平方比值为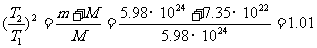
24. (15分)
(15分)
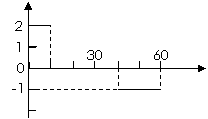
汽车由静止开始在平直的公路上行驶,0 ~60s内汽车的加速度随时间变化的图线如右图所示。
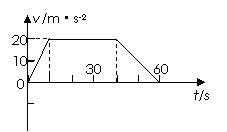
⑴画出汽车在0~60s内的v-t图线;
⑵求在这60s内汽车行驶的路程。
[答案]⑴速度图像为右图。
 ⑵900m
⑵900m
[解析]由加速度图像可知前10s汽车匀加速,后20s汽车匀减速恰好停止,因为图像的面积表示速度的变化,此两段的面积相等。最大速度为20m/s。所以速度图像为右图。然后利用速度图像的面积求出位移。
⑵汽车运动的面积为匀加速、匀速、匀减速三段的位移之和。
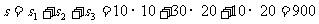 m
m
23. (16分)
(16分)
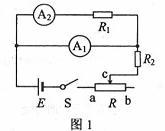
一电流表的量程标定不准确,某同学利用图1所示电路测量该电流表的实际量程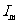 。
。
所用器材有:量程不准的电流表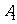 ,内阻
,内阻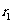 =10.0
=10.0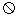 ,量程标称为5.0mA;标准电流表
,量程标称为5.0mA;标准电流表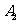 ,内阻
,内阻 =45.0
=45.0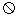 ,量程1.0mA;标准电阻
,量程1.0mA;标准电阻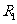 ,阻值10.0
,阻值10.0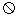 ;滑动变阻器R,总电阻为300.0
;滑动变阻器R,总电阻为300.0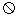 ;电源E,电动势3. 0V,内阻不计;保护电阻
;电源E,电动势3. 0V,内阻不计;保护电阻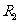 ;开关S;导线。
;开关S;导线。
回答下列问题:
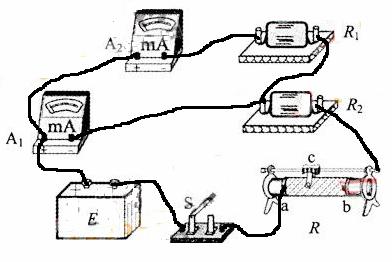
(1)在答题卡上(图2所示)的实物图上画出连线。
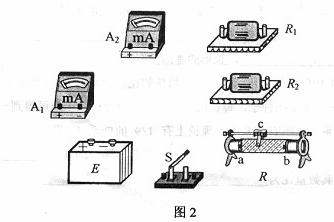
(2)开关S闭合前,滑动变阻器的滑动端c应滑动至 端。
(3)开关S闭合后,调节滑动变阻器的滑动端,使电流表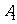 满偏;若此时电流表
满偏;若此时电流表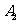 的读数为
的读数为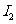 ,则
,则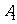 的量程
的量程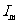 = 。
= 。
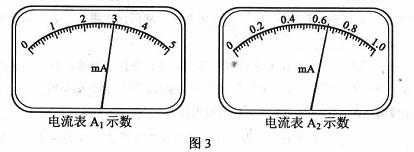
(4)若测量时,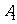 未调到满偏,两电流表的示数如图3所示,从图中读出
未调到满偏,两电流表的示数如图3所示,从图中读出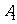 的示数
的示数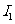 = ,
= ,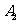 的示数
的示数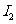 = ;由读出的数据计算得
= ;由读出的数据计算得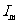 = 。(保留3位有效数字)
= 。(保留3位有效数字)
 (5)写出一条提高测量准确度的建议:
。
(5)写出一条提高测量准确度的建议:
。
[答案]⑴连线如图
⑵阻值最大
⑶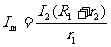
⑷6.05mA
[解析]⑴连线如图
⑵在滑动变阻器的限流接法中在接通开关前需要将滑动触头滑动到阻值最大端
⑶闭合开关调节滑动变阻器使待测表满偏,流过的电流为Im。根据并联电路电压相等有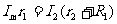 得
得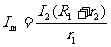
⑷待测表未满偏有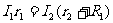 ,将A2的示数0.66mA和其他已知条件代入有
,将A2的示数0.66mA和其他已知条件代入有
 Ma
Ma
但图中A1的示数3.0mA量程为5.0mA,根据电流表的刻度是均匀的,则准确量程为6.05mA
⑸
22.(18分)
图1是利用激光测转的原理示意图,图中圆盘可绕固定轴转动,盘边缘侧面上有一小段涂有很薄的反光材料。当盘转到某一位置时,接收器可以接收到反光涂层所反射的激光束,并将所收到的光信号转变成电信号,在示波器显示屏上显示出来(如图2所示)。
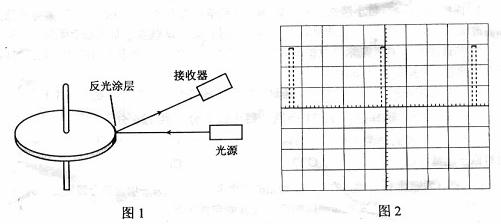
(1)若图2中示波器显示屏横向的每大格(5小格)对应的时间为5.00×10-2 s ,则圆盘的转速为__________________转/s。(保留3位有效数字)
(2)若测得圆盘直径为10.20 cm,则可求得圆盘侧面反光涂层的长度为 ________ cm。(保留3位有效数字)
[答案]⑴4.55转 /s ⑵2.91cm
[解析]⑴从图2可知圆盘转一圈的时间在横坐标上显示22格,由题意知图2中横坐标上每格表示1.00×10-2s,所以圆盘转动的周期是0.22s,则转速为4.55转 /s
⑵反光引起的电流图像在图2中横坐标上每次一格,说明反光涂层的长度占圆盘周长的22分之一为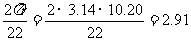 cm。
cm。
[命题意图与考点定位]匀速圆周运动的周期与转速的关系,以及对传感器所得图像的识图。
21.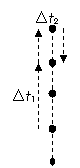 一简谐振子沿x轴振动,平衡位置在坐标原点。
一简谐振子沿x轴振动,平衡位置在坐标原点。 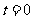 时刻振子的位移
时刻振子的位移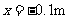 ;
;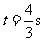 时刻
时刻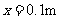 ;
;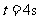 时刻
时刻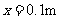 。该振子的振幅和周期可能为
。该振子的振幅和周期可能为
A.0. 1 m,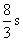 B.0.1 m, 8s C.0.2 m,
B.0.1 m, 8s C.0.2 m,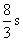 D.0.2
m,8s
D.0.2
m,8s
[答案]A
[解析]在t=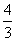 s和t=4s两时刻振子的位移相同,第一种情况是此时间差是周期的整数倍
s和t=4s两时刻振子的位移相同,第一种情况是此时间差是周期的整数倍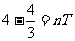 ,当n=1时
,当n=1时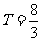 s。在
s。在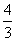 s的半个周期内振子的位移由负的最大变为正的最大,所以振幅是0.1m。A正确。
s的半个周期内振子的位移由负的最大变为正的最大,所以振幅是0.1m。A正确。
第二种情况是此时间差不是周期的整数倍则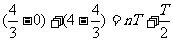 ,当n=0时
,当n=0时 s,且由于
s,且由于 是
是 的二倍说明振幅是该位移的二倍为0.2m。如图答案D。
的二倍说明振幅是该位移的二倍为0.2m。如图答案D。
[命题意图与考点定位]振动的周期性引起的位移周期性变化。
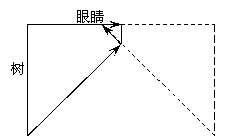
20.某人手持边长为6cm的正方形平面镜测量身后一棵树的高度。测量时保持镜面与地面垂直,镜子与眼睛的距离为0.4m。在某位置时,他在镜中恰好能够看到整棵树的像;然后他向前走了6.0 m,发现用这个镜子长度的5/6就能看到整棵树的像,这棵树的高度约为
A.5.5m B.5.0m C.4.5m D.4.0m

 [答案]B
[答案]B
[解析]如图是恰好看到树时的反射光路,由图中的三角形可得
 ,即
,即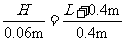 。人离树越远,视野越大,看到树所需镜面越小,同理有
。人离树越远,视野越大,看到树所需镜面越小,同理有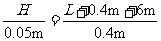 ,以上两式解得L=29.6m,H=4.5m。
,以上两式解得L=29.6m,H=4.5m。
[命题意图与考点定位]平面镜的反射成像,能够正确转化为三角形求解
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com