
24.硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3 MgO、CaO等,生产工艺流程示意如下:

(1) 将菱锌矿研磨成粉的目的是_____。
(2) 完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)2+□____+□_____==□Fe(OH)3 +□CI-
(3)针铁矿(Goethite)是以德国诗人歌德(Go ethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是_______。
ethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是_______。
(4)根据下表数据,调节“滤液 2”的pH时,理论上可选用的最大区间为______。
2”的pH时,理论上可选用的最大区间为______。
|
|
Mg(OH)2 |
Zn(OH)2 |
MgCO3 |
CaCO3 |
|
开始沉淀的pH |
10.4 |
6.4 |
- |
- |
|
沉淀完全的pH |
12.4 |
8.0 |
- |
- |
|
开始溶解的pH |
- |
10.5 |
- |
- |
|
Ksp |
5.6× |
- |
6.8× |
2.8×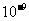 |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是______(选填序号).
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3 的质量分数不低于________。
23.(15分)J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
(1)M的离子结构示意图为_____;元素T在周期表中位于第_____族。
(2)J和氢组成的化合物分子有6个原子,其结构简式为______。
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为_____。
(4)L的最简单气态氢化物甲的水溶液显碱性。
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为______。
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是_______(选填序号)。
|
选项 |
a |
b |
c |
d |
|
x |
温度 |
温度 |
加入H2的物质的量 |
加入甲的物质的量 |
|
y |
甲的物质的量 |
平衡常数K |
甲的转化率 |
生成物物质的量总和 |
(5)由J、R形成的液态化合物JR2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215k J。
该反应的热化学方程式为________。
J。
该反应的热化学方程式为________。
12.化合物Bilirubin在一定波长的光照射下发生分解反应,反应物尝试随反应时间变化如右图所示,计算反应4~8 min间的平均反应速率和推测反应16 min 反应物的浓度,结果应是

A. 2.5 和2.0
和2.0 B. 2.5
B. 2.5 和2.5
和2.5
C. 3.0 和3.0
和3.0 D. 5.0
D. 5.0 和3.0
和3.0
11.铅蓄电池的工作原理为: 研读 右图,下列判断不正确的是
研读 右图,下列判断不正确的是
 A.K 闭合时,d电极反应式:
A.K 闭合时,d电极反应式:

B.当电路中转移0.2mol电子时,I中消耗的 为0.2 mol
为0.2 mol
C.K闭合时,II中 向c电极迁移
向c电极迁移
D.K闭合一段时间后,II可单独作为原电池,d电极为正极
10.下列关于电解质溶 液的正确判断是
液的正确判断是
A.在pH = 12的溶液中, 、
、 、
、 、
、 可以常量共存
可以常量共存
B.在pH= 0的溶液中, 、
、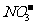 、
、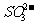 、
、 可以常量共存
可以常量共存
C.由0.1 mol· 一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH=
一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH=
D.由0.1 mol· 一元碱HA溶液的pH=3, 可推知NaA溶液存在A-
+ H2O⇋HA + OH-
一元碱HA溶液的pH=3, 可推知NaA溶液存在A-
+ H2O⇋HA + OH-
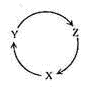
9.下表各组物质中,满足下图物质一步转化关系的选项是
|
选项 |
X |
Y |
Z |
|
A |
Na |
NaOH |
NaHCO3 |
|
B |
Cu |
CuSO4 |
Cu(OH)2 |
|
C |
C |
CO |
CO2 |
|
D |
Si |
SIO2 |
H2SiO3 |
8.下列有关化学研究的正确说法是
A.同时改变两个变量来研究反映速率的变化,能更快得出有关规律
B.对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同
C.依据丁大尔现象可将分散系分为溶液、胶体与浊液
D.从HF、HCl、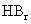 、HI酸性递增的事
、HI酸性递增的事 实,推出F、Cl、Br、I的非金属递增的规律
实,推出F、Cl、Br、I的非金属递增的规律
7. 表示阿伏伽德罗常数,下列判断正确的是
表示阿伏伽德罗常数,下列判断正确的是
A.在18 中含有
中含有 个氧原子
个氧原子
B.标准状况下,22.4L空气含有 个单质分子
个单质分子
C.1 mol参加反应转移电子数一定为2
D.含 个
个 的
的 溶解于1L水中,
溶解于1L水中, 的物质的量浓度为
的物质的量浓度为
6.下列关于有机物的正确说法是
A.聚乙烯可发生加成反应
B.石油干馏可得到汽油、,煤油等
C.淀粉、蛋白质完全水解的产物互为同分异构体
D.乙酸乙酯、油脂与NaOH溶液反应均有醇生成。
20.(本小题满分10分)
已知圆C的圆心在坐标原点,且过点M( ).
).
(1)求圆C的方程;
(2)已知点P是圆C上的动点,试求点P到直线 的距离的最小值;
的距离的最小值;
(3)若直线l与圆C相切,且l与x,y轴的正半轴分别相交于A,B两点,求△ABC的面积最小时直线
l的方程.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com