
19.在如图所示的电路中,两个相同的小灯泡L1和L2分别串联一个带铁芯的电感线圈L和一个滑动变阻器R。闭合开关S后,调整R,使L1和L2发光的亮度一样,此时流过两个灯泡的电流均为I。然后,断开S。若t′时刻再闭合S,则在t′前后的一小段时间内,正确反映流过L1的电流L1、流过L2的电流l2随时间t变化的图像是
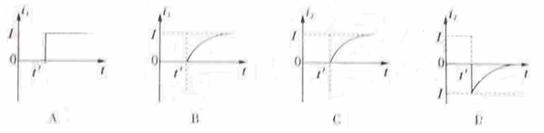
[答案]B
[解析]本题考查通电自感,与滑动变阻器R串联的L2,没有自感直接变亮,电流变化图像和A中图线,C D错误。与带铁芯的电感线圈串联的L1,自感强电流逐渐变大,B正确。
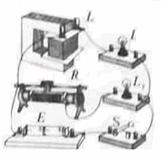
18. 用控制变量法,可以研究影响平行板电容器电容的因素(如图)。设两极板正对面积为S,极板间的距离为d,静电计指针偏角为θ。实验中,极板所带电荷量不变,若
用控制变量法,可以研究影响平行板电容器电容的因素(如图)。设两极板正对面积为S,极板间的距离为d,静电计指针偏角为θ。实验中,极板所带电荷量不变,若
A.保持S不变,增大d,则θ变大
B.保持S不变,增大d,则θ变小
C.保持d不变,减小S,则θ变小
D.保持d不变,减小S,则θ不变
[答案]A
 [解析]由
[解析]由 知保持S不变,增大d,电容减小,电容器带电能力降低,电容器电量减小,静电计所带电量增加,θ变大;保持d不变,减小S,电容减小,θ变大。正确答案A。
知保持S不变,增大d,电容减小,电容器带电能力降低,电容器电量减小,静电计所带电量增加,θ变大;保持d不变,减小S,电容减小,θ变大。正确答案A。
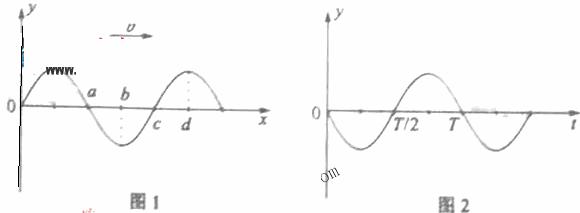
17.一列横波沿x轴正向传播,a、b、c、d为介质中沿波传播方向上四个质点的平衡位置。某时刻的波形如图1所示,此后,若经过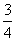 周期开始计时,则图2描述的是
周期开始计时,则图2描述的是
A.a处质点的振动图象 B.b处质点的振动图象
C.c处质点的振动图象 D.d处质点的振动图象
[答案]B
[解析]由波的图像经过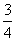 周期a到达波谷,b到达平衡位置向下运动,c到达波峰,d到达平衡位置向上运动,这是四质点在0时刻的状态,只有b的符合振动图像,答案B。
周期a到达波谷,b到达平衡位置向下运动,c到达波峰,d到达平衡位置向上运动,这是四质点在0时刻的状态,只有b的符合振动图像,答案B。
16.一物体静置在平均密度为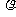 的球形天体表面的赤道上。已知万有引力常量为G,若由于天体自转使物体对天体表面压力恰好为零,则天体自转周期为
的球形天体表面的赤道上。已知万有引力常量为G,若由于天体自转使物体对天体表面压力恰好为零,则天体自转周期为
A.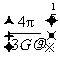 B.
B.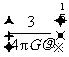 C.
C.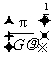 D.
D.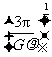
[答案]D
[解析]赤道表面的 物体对天体表面的压力为零,说明天体对物体的万有引力恰好等于物体随天体转动所需要的向心力,有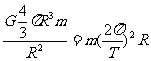 ,化简得
,化简得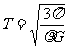 ,正确答案为D 。
,正确答案为D 。
15.太阳因核聚变释放出巨大的能量,同时其质量不断减少。太阳每秒钟辐射出的能量约为4×1026 J,根据爱因斯坦质能方程,太阳每秒钟减少的质量最接近
A.1036 kg B.1018 kg C.1013 kg D.109 kg
[答案] D
[解析]根据爱因斯坦的质能方程,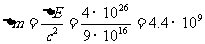 kg,D正确
kg,D正确
14.对于红、黄、绿、蓝四种单色光,下列表述正确的是
A.在相同介质中,绿光的折射率最大 B.红光的频率最高
C.在相同介质中,蓝光的波长最短 D.黄光光子的能量最小
[答案]C
[解析]红、黄、绿、蓝四种单色光的频率依次增大,光从真空进入介质频率不变,B 错。由色散现象同一介质对频率大的光有大的折射率,A错。频率大的光在真空中和介质中的波长都小,蓝光的波长最短,C正确。频率大,光子能量大,D错。
28.答案(17分)
(1)醛基
(2)加成反应
(3)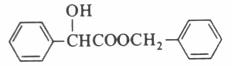
(4)
(5)13
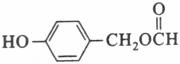
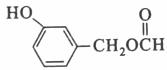
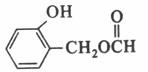
(写出任意一种均给分)
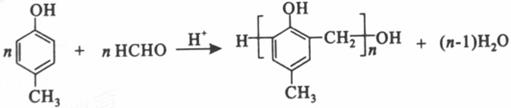
(6)
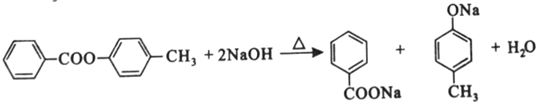
(7)

[解析]本题考查有机合成和推断。(1)根据A 扁桃酸的反应,结合提供的信息,可以推断A为
扁桃酸的反应,结合提供的信息,可以推断A为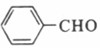 ,其含氧官能团的名称为醛基。(2)
,其含氧官能团的名称为醛基。(2) 与氢气的反应属于醛基的加成反应。(3)C为
与氢气的反应属于醛基的加成反应。(3)C为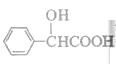 和
和 发生酯化反应的产物,其结构简式为
发生酯化反应的产物,其结构简式为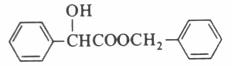 。(4)由醛的银镜反应可知,A发生银镜反应生成
。(4)由醛的银镜反应可知,A发生银镜反应生成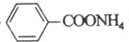 、Ag、NH3和H2O,化学方程式为:
、Ag、NH3和H2O,化学方程式为:  。(5)扁桃酸的同分异构体属于甲酸酯且含有酚羟基,则苯环上有两种可能:①含有HCOOCH2-和-OH,二者在苯环上共用三种位置关系;②含有HCOO-、-OH、-CH3,三者在苯环上共用十种位置关系,因此其同分异构体总共有13种,其结构简式可以为
。(5)扁桃酸的同分异构体属于甲酸酯且含有酚羟基,则苯环上有两种可能:①含有HCOOCH2-和-OH,二者在苯环上共用三种位置关系;②含有HCOO-、-OH、-CH3,三者在苯环上共用十种位置关系,因此其同分异构体总共有13种,其结构简式可以为 等。(6)
等。(6)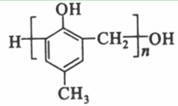 为甲醛和
为甲醛和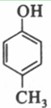 的缩聚反应。(7)根据转化关系,E为
的缩聚反应。(7)根据转化关系,E为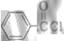 ,F为
,F为 ,二者发生取代反应生成
,二者发生取代反应生成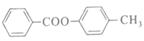 ,
, 与NaOH溶液发生水解反应:
与NaOH溶液发生水解反应: 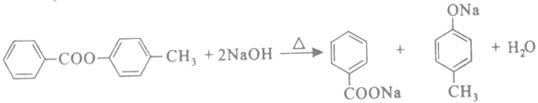 。
。

28.(17分)
镇痉药物C、化合物N以及高分子树脂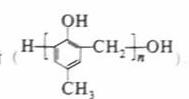 的合成路线如下:
的合成路线如下:
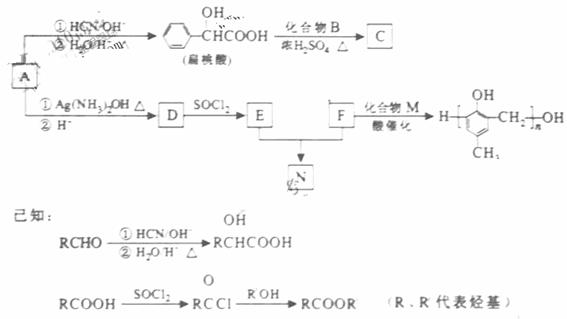
(1)A的含氧官能团的名称是 。
(2)A在催化剂作用下可与H2反应生成B。该反应的反应类型是 。
(3)酯类化合物C的分子式是C15H14O3,其结构简式是 。
(4)A发生银镜反应的化学方程式是 。
(5)扁桃酸(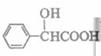 )有多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有 种,写出其中一种含亚甲基(―CH2―)的同分异构体的结构简式 。
)有多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有 种,写出其中一种含亚甲基(―CH2―)的同分异构体的结构简式 。
(6)F与M合成高分子树脂的化学方程式是 。
(7)N在NaOH溶液中发生水解反应的化学方程式是 。
27.答案(13分)
(1)
(2)淀粉KI试纸变蓝

 (3)
(3)

(4)打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D震荡。静至后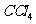 层溶液变为紫红色
层溶液变为紫红色
(5)确认C的黄色溶液中无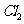 ,排除
,排除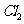 对溴置换碘实验的干扰。
对溴置换碘实验的干扰。
(6)原子半径逐渐增大
[解析]本题考查化学实验的设计和分析。(1)A中产生的黄绿色气体为Cl2,其电子式为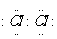 。(2)氯气遇淀粉KI试纸时,发生反应:Cl2+2KI=I2+2KCl,产生的I2遇淀粉变蓝,可以证明氯气的氧化性强于碘。(3)B中Cl2与NaBr发生置换反应,离子方程式为:Cl2+2Br-=2Cl-+Br2。(4)C中NaBr与氯气反应生成NaCl和Br2,将C中溶液滴入D中,发生反应:Br2+2KI=I2+2KBr,此时D中溶液分层,下层为碘的四氯化碳溶液,显紫红色,可以说明溴的氧化性强于碘。(5)过程Ⅲ主要为了确认C的黄色溶液中无Cl2,排出对溴置换碘实验的干扰。(6)Cl、Br、I单质的氧化性逐渐减弱,是因为从Cl到I,原子半径逐渐增大,得电子能力逐渐减弱。
。(2)氯气遇淀粉KI试纸时,发生反应:Cl2+2KI=I2+2KCl,产生的I2遇淀粉变蓝,可以证明氯气的氧化性强于碘。(3)B中Cl2与NaBr发生置换反应,离子方程式为:Cl2+2Br-=2Cl-+Br2。(4)C中NaBr与氯气反应生成NaCl和Br2,将C中溶液滴入D中,发生反应:Br2+2KI=I2+2KBr,此时D中溶液分层,下层为碘的四氯化碳溶液,显紫红色,可以说明溴的氧化性强于碘。(5)过程Ⅲ主要为了确认C的黄色溶液中无Cl2,排出对溴置换碘实验的干扰。(6)Cl、Br、I单质的氧化性逐渐减弱,是因为从Cl到I,原子半径逐渐增大,得电子能力逐渐减弱。
27.(13分)
为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
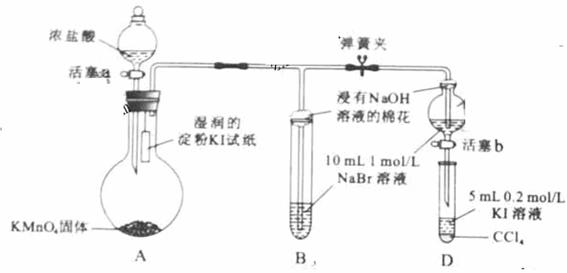
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是 。
(2)验证氯气的氧化性强于碘的实验现象是 。
(3)B中溶液发生反应的离子方程式是 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 。
(5)过程Ⅲ实验的目的是 。
(6)氯、溴、碘单质的氧化性逐渐减北的原因:同主族元素从上到下 ,得电子能力逐渐减弱。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com