
7. БэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
БэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.БъзМзДПіЯТЃЌ22.4LЖўТШМзЭщЕФЗжзгЪ§дМЮЊ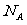 Иі
Иі
B.ЪЂга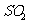 ЕФУмБеШнЦїжаКЌга
ЕФУмБеШнЦїжаКЌга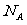 ИібѕдзгЃЌдђ
ИібѕдзгЃЌдђ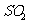 ЕФЮяжЪЕФСПЮЊ0.5mol
ЕФЮяжЪЕФСПЮЊ0.5mol
C.17.6gБћЭщжаЫљКЌЕФМЋадЙВМлМќЮЊ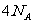 Иі
Иі
D.ЕчНтОЋСЖЭЪБЃЌШєвѕМЋЕУЕНЕчзгЪ§ЮЊ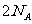 ИіЃЌдђбєМЋжЪСПМѕЩй64g
ИіЃЌдђбєМЋжЪСПМѕЩй64g
6.НкФмМѕХХЖдЗЂеЙОМУЁЂБЃЛЄЛЗОГгаживЊвтвхЁЃЯТСаДыЪЉВЛФмМѕЩйЖўбѕЛЏЬМХХЗХЕФЪЧ
A.РћгУЬЋбєФмжЦЧтЁЁЁЁЁЁЁЁЁЁЁЁ B.ЙиЭЃаЁЛ№ЕчЦѓвЕ
C.ОйааЁАЕиЧђвЛаЁЪБЁБЯЈЕЦЛюЖЏЁЁЁЁ D.ЭЦЙуЪЙгУУКвКЛЏММЪѕ
(Жў)бЁПМЬтЃКЙВ45ЗжЁЃЧыПМЩњДгИјГіЕФ2ЕРЮяРэЬтЁЂ2ЕРЛЏбЇЬтЁЂ2ЕРЩњЮяЬтжаУППЦШЮбЁвЛЬтзіД№ЃЌВЂгУ2BЧІБЪдкД№ЬтПЈЩЯАбЫљбЁЬтФПЕФЬтКХЭПКкЁЃзЂвтЫљзіЬтФПЕФЬтКХБиаыгыЫљЭПЬтФПЕФЬтКХвЛжТЃЌдкД№ЬтПЈбЁД№ЧјгђжИЖЈЮЛжУД№ЬтЁЃШчЙћЖрзіЃЌдђУПбЇПЦАДЫљзіЕФЕквЛЬтМЦЗжЁЃ
35ЃЎ[ЛЏбЇ--бЁаоЛЏбЇгыЩњЛю](15Зж)
(Ђё)КЯН№ЪЧЩњЛюжаГЃгУЕФВФСЯЃЌЧыЛиД№ЯТСаЮЪЬтЃК
(1)ЩњЬњКЭИжЪЧКЌЬМСПВЛЭЌЕФЬњЬМКЯН№ЃЌКЌЬМСПдк2%-4.3%ЕФГЦЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃВЛатИждкПеЦјжаБШНЯЮШЖЈЃЌВЛвзЩњатЃЌгаЧПЕФПЙИЏЪДФмСІЃЌЦфКЯН№дЊЫижївЊЪЧЁЁЁЁЁЁЁЁЁЁ ЃЛЁЁЁЁ (2)ИжЬњЕФИЏЪДИјЩчЛсдьГЩЕФЫ№ЪЇЪЧОоДѓЕФЃЌЫљвдВЩШЁИїжжДыЪЉЗРжЙИжЬњЕФИЏЪДЪЧЪЎЗжБивЊЕФЃЌЧыСаОйШ§жжЗРжЙИжЬњИЏЪДЕФЗНЗЈЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛЁЁЁЁ
(3)ЧрЭЕФжївЊКЯН№дЊЫиЮЊЁЁЁЁЁЁЁЁЁЁ ЃЌЛЦЭЕФжївЊКЯН№дЊЫиЮЊЁЁЁЁЁЁЁЁЁЁ ЃК
(4)ДЂЧтКЯН№ЪЧвЛРрФмЙЛДѓСПЮќЪеЧтЦјЃЌВЂгыЧтЦјНсКЯГЩН№ЪєЧтЛЏЮяЕФВФСЯЁЃШчячФјКЯН№ЃЌЫќЮќЪеЧтЦјПЩНсКЯГЩН№ЪєЧтЛЏЮяЃЌЦфЛЏбЇЪНПЩНќЫЦЕиБэЪОЮЊ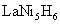 (
(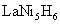 жаИїдЊЫиЛЏКЯМлОљПЩПДзїЪЧСу)ЃЌЫќИњ
жаИїдЊЫиЛЏКЯМлОљПЩПДзїЪЧСу)ЃЌЫќИњ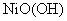 ПЩзщГЩФјЧтПЩГфЕчЕчГиЃК
ПЩзщГЩФјЧтПЩГфЕчЕчГиЃК
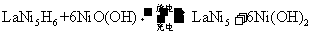
ИУЕчГиЗХЕчЪБЃЌИКМЋЗДгІЪЧЁЁЁЁЁЁ ЁЃЪаУцЩЯГіЪлЕФБъГЦШнСПЮЊ2000 mA hЕФ1НкФјЧтЕчГижСЩйгІКЌгаячФјКЯН№ЁЁЁЁЁЁ g(вбжЊ1ЗЈРЕкЕчСПЮЊ96500ПтТиЛђАВХрЁЄУы)ЁЃ
(Ђђ)гаЛњЛЏКЯЮягыЩњЛюЯЂЯЂЯрЙиЁЃЧыЛиД№ЯТСагаЙиЮЪЬтЃК
(1)УоЛЈЁЂВЯЫПЁЂаЁТѓжївЊГЩЗжЗжБ№ЮЊЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁ ЃЌЫќУЧоЌЖМЪєгкЬьШЛгаЛњИпЗжзгЛЏКЯЮяЃЛ
(2)ЮЖОЋЪЧХытПГЃгУЕФЕїЮЖЦЗЃЌЦфжївЊГЩЗжЕФЛЏбЇУћГЦЮЊЁЁЁЁЁЁ ЃЛЁЁ
(3)НтШШеђЭДвЉАЂЫОЦЅСжжївЊГЩЗжЕФНсЙЙМђЪНЮЊЁЁЁЁЁЁ ЁЃ
36ЃЎ[ЛЏбЇ--бЁаогаЛњЛЏбЇЛљДЁ](15Зж)
PCЪЧвЛжжПЩНЕНтЕФОлЬМЫсѕЅРрИпЗжзгВФСЯЃЌгЩгкЦфОпгагХСМЕФФЭГхЛїадКЭШЭадЃЌвђЖјЕУЕНСЫЙуЗКЕФгІгУЁЃвдЯТЪЧФГбаОПаЁзщПЊЗЂЕФЩњВњPCЕФКЯГЩТЗЯпЃК
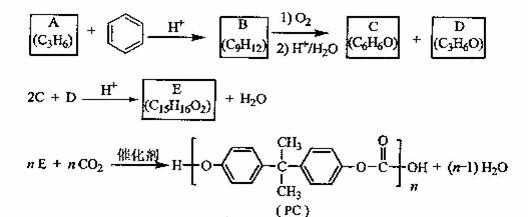
вбжЊвдЯТаХЯЂЃК
ЂйAПЩЪЙфхЕФCCl4ШмвКЭЪЩЋЃЛ
ЂкBжагаЮхжжВЛЭЌЛЏбЇЛЗОГЕФЧтЃЛЁЁЁЁ
ЂлCПЩгыFeCl3ШмвКЗЂЩњЯдЩЋЗДгІЃКЁЁЁЁ
ЂмDВЛФмЪЙфхЕФCCl4ЭЪЩЋЃЌЦфКЫДХЙВеёЧтЦзЮЊЕЅЗхЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)AЕФЛЏбЇУћГЦЪЧЁЁЁЁ ЃЛЁЁ
(2)BЕФНсЙЙМђЪНЮЊ--ЃЛЁЁ ЁЁ
(3)CгыDЗДгІЩњГЩEЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁ ЃЛ
(4)DгаЖржжЭЌЗжвьЙЙЬхЃЌЦфжаФмЗЂЩњвјОЕЗДгІЕФЪЧЁЁЁЁ ЁЁ(аДГіНсЙЙМђЪН)ЃЛЁЁЁЁ
(5)BЕФЭЌЗжвьЙЙЬхжаКЌгаБНЛЗЕФЛЙгаЁЁЁЁ жжЃЌЦфжадкКЫДХЙВеёЧтЦзжаГіЯжБћСНзщЗхЃЌЧвЗхУцЛ§жЎБШЮЊ3ЃК1ЕФЪЧЁЁЁЁЁЁЁЁ (аДГіНсЙЙМђЪН)ЁЃ
(вЛ)БиПМЬт(11ЬтЃЌЙВ129Зж)
26ЃЎ(14Зж)
ЁЁЁЁ ЮяжЪA-GгаЯТЭМЫљЪОзЊЛЏЙиЯЕ(ВПЗжЗДгІЮяЁЂЩњГЩЮяУЛгаСаГі)ЁЃЦфжаAЮЊФГН№ЪєПѓЕФжївЊГЩЗжЃЌОЙ§вЛЯЕСаЗДгІПЩЕУЕНBКЭCЁЃЕЅжЪCПЩгыEЕФХЈШмвКЗЂЩњЗДгІЃЌGЮЊзЉКьЩЋГСЕэЁЃ
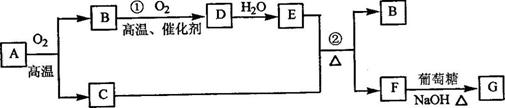
ЧыЛиД№ЯТСаЮЪЬтЃК
ЁЁЁЁ (1)аДГіЯТСаЮяжЪЕФЛЏбЇЪНЃКBЁЁЁЁЁЁЁЁЁЁ ЁЂEЁЁЁЁЁЁЁЁЁЁ ЁЂGЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁЁЁ (2)РћгУЕчНтПЩЬсДПCЮяжЪЃЌдкИУЕчНтЗДгІжабєМЋЮяжЪЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌвѕМЋЮяжЪЪЧЁЁЁЁЁЁЁЁЁЁ ЃЌЕчНтжЪШмвКЪЧЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁЁЁ (3)ЗДгІЂкЕФЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁЁЁ (4)НЋ0.23 mol BКЭ0.11 molбѕЦјЗХШыШнЛ§ЮЊ1 LЕФУмБеШнЦїжаЃЌЗЂЩњЗДгІЂйЃЌдквЛЖЈЮТЖШЯТЃЌЗДгІДяЕНЦНКтЃЌЕУЕН0.12 mol DЃЌдђЗДгІЕФЦНКтГЃЪ§K=ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃШєЮТЖШВЛБфЃЌдйМгШы0.50 molбѕЦјКѓжиаТДяЕНЦНКтЃЌдђBЕФЦНКтХЈЖШЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАдіДѓЁБЁЂЁАВЛБфЁБЛђЁАМѕаЁЁБ)ЃЌбѕЦјЕФзЊЛЏТЪЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАЩ§ИпЁБЁЂЁАВЛБфЁБЛђЁАНЕЕЭЁБ)ЃЌDЕФЬхЛ§ЗжЪ§ЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАдіДѓЁБЁЂЁАВЛБфЁБЛђЁАМѕаЁЁБ)ЁЃ
27ЃЎ(15Зж)
ЁЁЁЁ ФГЛЏбЇаЫШЄаЁзщЮЊЬНОПSO2ЕФаджЪЃЌАДЯТЭМЫљЪОзАжУНјааЪЕбщЁЃ

ЧыЕНД№FСаЮЪЬтЃК
ЁЁ (1)зАжУAжаЪЂЗХбЧСђЫсФЦЕФвЧЦїУћГЦЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЌЦфжаЗЂЩњЗД гІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЛ
гІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЛ
ЁЁ (2)ЪЕбщЙ§ГЬжаЃЌзАжУBЁЂCжаЗЂЩњЕФЯжЯѓЗжБ№ЪЧЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁ ЃЌетаЉЯжЯѓЗжБ№ЫЕУїSO2ОпгаЕФаджЪЪЧЁЁЁЁЁЁЁЁЁЁ КЭЁЁЁЁЁЁЁЁЁЁ ЃЛзАжУBжаЗЂЩњЗДгІЕФРызгЗНГЬЪН
ЮЊЁЁЁЁЁЁЁЁ ЃЛ
ЁЁ (3)зАжУDЕФФПЕФЪЧЬНОПSO2гыЦЗКьзїгУЕФПЩФцадЃЌЧыаДГіЪЕбщВйзїМАЯжЯѓЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁ (4)ЮВЦјПЩВЩгУ ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁШмвКЮќЪеЁЃ
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁШмвКЮќЪеЁЃ
28ЃЎ(14Зж)
ЁЁЁЁ ФГЭЌбЇдкгУЯЁСђЫсгыаПжЦШЁЧтЦјЕФЪЕбщжаЃЌЗЂЯжМгШыЩйСПСђЫсЭШмвКПЩМгПьЧтЦјЕФЩњГЩЫйТЪЁЃЧыЛиД№ЯТСаЮЪЬтЃК
ЁЁ (1)ЩЯЪіЪЕбщжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНгаЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁ (2)СђЫсЭШмвКПЩвдМгПьЧтЦјЩњГЩЫйТЪЕФдвђЪЧЁЁЁЁЁЁЁЁЁЁ ЃЛ
(3)ЪЕбщЪвжаЯжга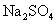 ЁЂ
ЁЂ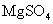 ЁЂ
ЁЂ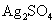 ЁЂ
ЁЂ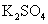 ЕШ4жаШмвКЃЌПЩгыЪЕбщжа
ЕШ4жаШмвКЃЌПЩгыЪЕбщжа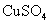 ШмвКЦ№ЯрЫЦзїгУЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЛ
ШмвКЦ№ЯрЫЦзїгУЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЛ
ЁЁ (4)вЊМгПьЩЯЪіЪЕбщжаЦјЬхВњЩњЕФЫйТЪЃЌЛЙПЩВЩШЁЕФДыьКгаЁЁЁЁЁЁЁЁ (Д№СНжж)ЃЛ
ЁЁ (5)ЮЊСЫНјвЛВНбаОПСђЫсЭЕФСПЖдЧтЦјЩњГЩЫйТЪЕФгАЯьЃЌИУЭЌбЇЩшМЦСЫШчЯТвЛЯЕСаЪЕбщЁЃНЋБэжаЫљИјЕФЛьКЯШмвКЗжБ№МгШыЕН6ИіЪЂгаЙ§СПZnСЃЕФЗДгІЦПжаЃЌЪеМЏВњЩњЕФЦјЬхЃЌМЧТМЛёЕУЯрЭЌЬхЛ§ЕФЦјЬхЫљашЪБМфЁЃ
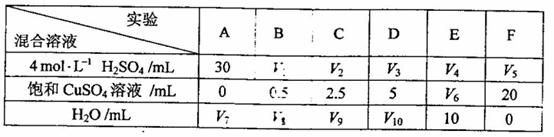
ЁЁЁЁ ЂйЧыЭъГЩДЫЪЕбщЩшМЦЃЌЦфжаЃКV1=ЁЁЁЁЁЁ ЃЌV6=ЁЁЁЁЁЁ ЁЁЃЌV9=ЁЁЁЁЁЁ ЃЛ
ЁЁЁЁ ЂкЗДгІвЛЖЮЪБМфКѓЃЌЪЕбщAжаЕФН№ЪєГЪЁЁЁЁЁЁ ЩЋЃЌЪЕбщEжаЕФН№ЪєГЪЁЁЁЁЁЁ ЩЋЃЛ
ЁЁЁЁ ЂлИУЭЌбЇзюКѓЕУГіЕФНсТлЮЊЃКЕБМгШыЩйСП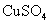 ШмвКЪБЃЌЩњГЩЧтЦјЕФЫйТЪЛсДѓДѓЬсИпЁЃЕЋЕБМгШыЕФ
ШмвКЪБЃЌЩњГЩЧтЦјЕФЫйТЪЛсДѓДѓЬсИпЁЃЕЋЕБМгШыЕФ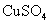 ШмвКГЌЙ§вЛЖЈСПЪБЃЌЩњГЩЧтЦјЕФЫйТЪЗДЖјЛсЯТНЕЁЃЧыЗжЮіЧтЦјЩњГЩЫйТЪЯТНЕЕФжївЊдвђЁЁЁЁЁЁЁЁЁЁ
ЁЃ
ШмвКГЌЙ§вЛЖЈСПЪБЃЌЩњГЩЧтЦјЕФЫйТЪЗДЖјЛсЯТНЕЁЃЧыЗжЮіЧтЦјЩњГЩЫйТЪЯТНЕЕФжївЊдвђЁЁЁЁЁЁЁЁЁЁ
ЁЃ
ЁЁЁЁ ЩњЖМБиаызіД№ЁЃЕк33Ьт-Ек38ЬтЮЊбЁПМЬтЃЌПМЩњИљОнвЊЧѓзіД№ЁЃ
13ЃЎЯТБэжаЦРМлКЯРэЕФЪЧ

12ЃЎИљОнгвЭМЃЌПЩХаЖЯГіЯТСаРызгЗНГЬЪНжаДэЮѓЕФЪЧ
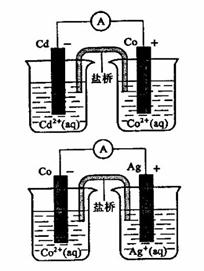 ЁЁ AЃЎ
ЁЁ AЃЎ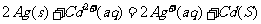
ЁЁ BЃЎ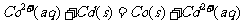
ЁЁ CЃЎ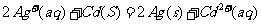
ЁЁ DЃЎ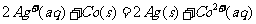
11ЃЎМКжЊЃК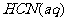 гы
гы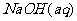 ЗДгІЕФ
ЗДгІЕФ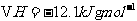 ЃЛ
ЃЛ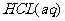 гы
гы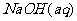 ЗДгІЕФ
ЗДгІЕФ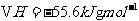 ЁЃдђ
ЁЃдђ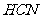 дкЫЎШмвКжаЕчРыЕФ
дкЫЎШмвКжаЕчРыЕФ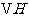 ЕШгк
ЕШгк
AЃЎ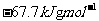 ЁЁЁЁ ЁЁЁЁBЃЎ
ЁЁЁЁ ЁЁЁЁBЃЎ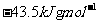
CЃЎ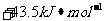 ЁЁЁЁЁЁ
DЃЎ
ЁЁЁЁЁЁ
DЃЎ 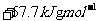
10ЃЎАб500 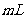 га
га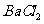 КЭ
КЭ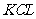 ЕФЛьКЯШмвКЗжГЩ5ЕШЗнЃЌШЁвЛЗнМгШыКЌ
ЕФЛьКЯШмвКЗжГЩ5ЕШЗнЃЌШЁвЛЗнМгШыКЌ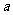
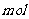 СђЫсФЦ
СђЫсФЦ
ЁЁЁЁ ЕФШмвКЃЌЧЁКУЪЙБЕРызгЭъШЋГСЕэЃЛСэШЁвЛЗнМгШыКЌ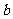
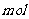 ЯѕЫсвјЕФШмвКЃЌЧЁКУЪЙТШ
ЯѕЫсвјЕФШмвКЃЌЧЁКУЪЙТШ
ЁЁЁЁ РызгЭъШЋГСЕэЁЃдђИУЛьКЯШмвКжаМиРызгХЈЖШЮЊ
AЃЎ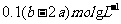 ЁЁЁЁЁЁ
BЃЎ
ЁЁЁЁЁЁ
BЃЎ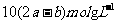
CЃЎ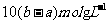 ЁЁЁЁЁЁЁЁ DЃЎ
ЁЁЁЁЁЁЁЁ DЃЎ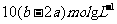
9ЃЎЯТСаИїзщжаЕФЗДгІЃЌЪєгкЭЌвЛЗДгІРраЭЕФЪЧ
ЁЁ AЃЎгЩфхБћЭщЫЎНтжЦБћДМЃЛгЩБћЯЉгыЫЎЗДгІжЦБћДМ
ЁЁ BЃЎгЩМзБНЯѕЛЏжЦЖдЯѕЛљМзБНЃЛгЩМзБНбѕЛЏжЦБНМзЫс
ЁЁ CЃЎгЩТШДњЛЗМКЭщЯћШЅжЦЛЗМКЯЉЃЛгЩБћЯЉМгфхжЦ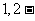 ЖўфхБћЭщ
ЖўфхБћЭщ
ЁЁ DЃЎгЩввЫсКЭввДМжЦввЫсввѕЅЃЛгЩБНМзЫсввѕЅЫЎНтжЦБНМзЫсКЭввДМ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com