
26.(17分)
F是新型降压药替米沙坦的中间体,可由下列路线合成:
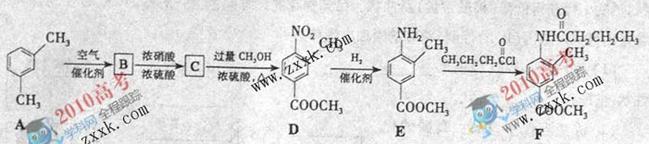
(1)A B的反应类型是
,D
B的反应类型是
,D E的反应类型是 ,E
E的反应类型是 ,E F的反应类型是
。
F的反应类型是
。
(2)写出满足下列条件的B的所有同分 异构体
(写结构式)。
异构体
(写结构式)。
①含有苯环 ②含有酯基 ③能与新制Cu(OH)2反应
(3)C中含有的它能团名称是
。已知固体C在加热条件下可深于甲醇,下列C D的有关说法正确的是 。
D的有关说法正确的是 。
a.使用过量的甲醇,是为了提高B的产 b.浓硫酸的吸水性可能会导致溶液变黑
c.甲醇即是反 物,又是溶剂 d.D的化学式为C2H2NO4
(4)E的同分异构苯丙氨酸经 合反应形成的高聚物是 (写结构简式)。
(5)已知 ;在一定条件下可水解为
;在一定条件下可水解为 , F在强酸和长时间加热条件下发生水解反应的化学方程式是
。
, F在强酸和长时间加热条件下发生水解反应的化学方程式是
。
25。答案(1)3 VIA HClO4 (2)2 H-Z H-Y (3)[Ar]3d104s1 2Cu2S+3O2=2Cu2O+2SO2
(4)2CO(g)+SO2(g)=S(s)+2CO2
(g) △H= -270kJ/mol
-270kJ/mol
解析:由表中可知,X为C Y为 S Z为 Cl W为Cu
25. (14分)
(14分)
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
|
元素 |
相关信息 |
|
X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
|
Z |
Z和Y同周期,Z的电负性大于Y |
|
W |
W的一种核素的质量数为63,中子数为34 |
(1)Y位于元素周期表第 周期表 族,Y和Z的 最高价氧化物对应的水化物的酸性较强的是 (写化学式)。
最高价氧化物对应的水化物的酸性较强的是 (写化学式)。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键。在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子核外电子排布式是 。W2Y在空气中煅烧生成W2O的化学方程式是 。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
XO(g)+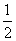 O2(g)=XO2(g)
O2(g)=XO2(g)  H=-283.0 kJ·mol-2
H=-283.0 kJ·mol-2
Y(g)+ O2(g)=YO2(g)  H=-296.0 kJ·mol-1
H=-296.0 kJ·mol-1
此反应的热化学方程式是 。
13.将0.01mol下列物质分别加入100mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度的大小顺序是(溶液体积变化忽略不计)
①Na2O1 ②Na2O ③Na2CO3 ④NaCl
A.①>②>③>④ B .①>②>④>③
.①>②>④>③
C.①=②>③>④ D.①=②>③=④
13答案:A
解析:①②溶于水,溶质都是0.02moL,但前者有氧气生成,因此氢氧根浓度大,有①>②;③中碳酸根水解使得阴离子浓 度稍大于④。因此有A正确。
度稍大于④。因此有A正确。
12.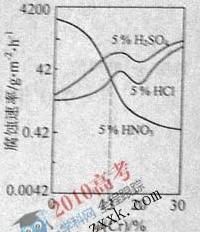 右图是一种稀硫对Fe-Gr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是
右图是一种稀硫对Fe-Gr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是
A.稀硫酸对Fe-Cr合金的腐蚀性比稀硫酸和稀盐酸的弱
B.稀硝酸和铁反应的化学方程式是:Fe+6HNO3(稀)-Fe(NO3)3+3NO2↑+3H 2O
2O
C.Cr含量大于13%时,因为三种酸中硫酸的氢离子浓度最大,所以 对Fe-Cr合金的腐蚀性最强
对Fe-Cr合金的腐蚀性最强
D.随着Cr含量增加,稀硫酸对F e-Cr合金的腐蚀性减弱
e-Cr合金的腐蚀性减弱
12答案:D
解析:A选项应该说铬的含量大于13%,稀硝酸对合金的腐蚀速率比盐酸硫酸弱。B应生成NO;C不能解释盐酸硝酸氢离子浓度相等,但硝酸腐蚀速度慢。
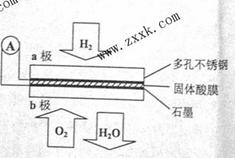
11.某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本 结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是
结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是
A.电子通过外电路从b极流向a极
B.b极上的电极反应式为:O2+2H2O+4e-=4OH-
C.每转移0.1 mol电子,消耗1.12 L的H2
D.H+由a极通过固体酸电解质传递到b极
11答案:D
解析:首先明确a为负极,这样电子应该是通过外电路由a极流向b,A错;B选项反应应为O2+4e-+4H+=2H2O ; C没有告知标准状况。
10.低脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH2(g)+NO(g)+NH2(g)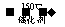 2H3(g)+3H2O(g)
2H3(g)+3H2O(g)  H<0
H<0
在恒容的密闭容器中,下列有关说法正确的是
A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B.平衡时,其他条件不变,增加NH3的浓度 ,废气中氮氧化物的转化率减小
,废气中氮氧化物的转化率减小
C.单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
10答案:C
 解析:A选项,放热反应升温平衡常数减小,错误;增大一个反应物浓度另一反应物转化率增大,B错;使用催化剂平衡不移动,D错。
解析:A选项,放热反应升温平衡常数减小,错误;增大一个反应物浓度另一反应物转化率增大,B错;使用催化剂平衡不移动,D错。
9.在pH=1的溶液中能大量共存的一组离子或分子是
A.Na+、Mg2+、ClO-、NO3- B. Al3+、 NH4+、 Br- 、Cl-
C. K+ 、Cr2O72- 、CH3CHO、 SO42- D. Na+、K+ 、SiO32-、Cl-
9答案:B
解析:酸性环境下A中生成次氯酸,C中Cr2O72-氧化CH3CHO,D中生成硅酸沉淀。
8.下列实验操作或装置符合实验要求的是
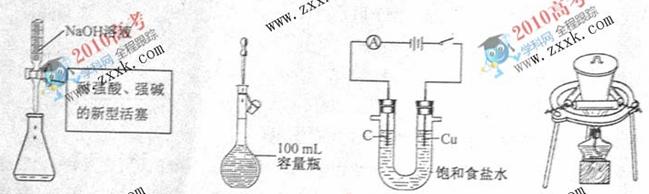
A.量取15.00 mL NaOH溶液 B.定容
C.电解制Cl2和H2 D.高温燃烧石灰石
D.高温燃烧石灰石
8答案:A
解析:B滴管口不能伸入到容量瓶内;C铜电极应该为阴极才能制备出氯气和氢气;D选项坩埚不能密 闭加热。
闭加热。
7. 亚氨基羟(Li2NH)是一种储氢容量 器,安全性好的固体储氢材料,其储氢原理可表示为Li2NH+H2=LiNH2+LiH。下列有关说法正确的是
器,安全性好的固体储氢材料,其储氢原理可表示为Li2NH+H2=LiNH2+LiH。下列有关说法正确的是
A. Li2NH中N的化合价是-1 B.该反应中H2既是氧化剂又是还原剂
C.Li+和H+的离子半径相等 D.此法储氢和钢瓶储氢的原理相同
7答案:B
解析:A选项中Li2NH中氮的化合价为-3;C选项中Li+半径 小于H-;D选项钢瓶储氢是物理过程,而该方法为化学方法。
小于H-;D选项钢瓶储氢是物理过程,而该方法为化学方法。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com