
4、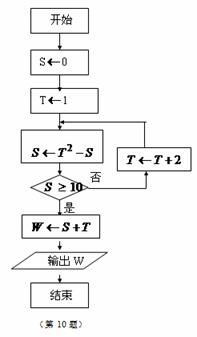 若复数
若复数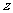 满足
满足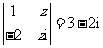 (
(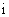 是虚数单位),则
是虚数单位),则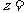 __________。
__________。
3、函数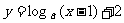
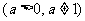 的图像恒过一定点是_________。
的图像恒过一定点是_________。
2、函数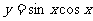 的最小正周期是___________。
的最小正周期是___________。
1、已知集合A=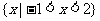 ,集合B=
,集合B=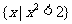 ,则
,则 =___________。
=___________。
30.(20分)
下图一表示在充满N2与CO2的密闭容器中(CO2充足),西红柿植株的呼吸速率和光合速率变化曲线;图二表示春末晴天某大棚蔬菜在不同条件下的表观光合作用强度(实际光合作用强度与呼吸作用强度之差),假设塑料大棚外环境条件相同,植株大小一致、生长正常,栽培管理条件相同。请分析回答下列问题。
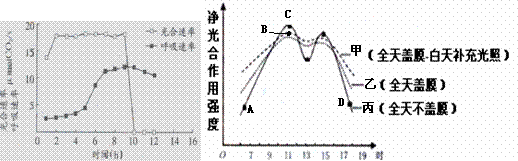
(1)图一中,5-8h间,使呼吸速率明显加快的主要原因是密闭容器内 ; 9-10h间,影响光合速率迅速下降的最可能原因是叶绿体中 减少,导致三碳糖的合成减慢。
(2)图二曲线丙中,A点植株细胞内能生成ATP的场所有 。曲线乙的峰值低于曲线甲,主要原因是光合作用过程中 阶段较慢。
(3)图二中,C点与B点相比,叶绿体内RuBP相对含量较 (高、低); A、C、D三点,植物积累有机物最多的是 。
(4)大豆种子萌发和生长过程中糖类和蛋白质的相互关系如图
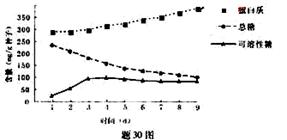
在上述定量测定之前,进行了蛋白质含量变化的预测实验,请填充实验原理,判断实验步骤上画线部分是否正确,并更正错误之处。
1)实验原理:蛋白质 ,其颜色还深浅与蛋白质含量成正比。
2)实验步骤:
①将三份等量大豆种子分别萌发1、5、9天后取出,各加入适量蒸馏水,研碎、提取、定容后离心得到蛋白质制备液;
②取3支试管,编号1、2、3,分别加入等量的萌发、5、9天的蛋白质制备液;
③在上述试管中各加入等量的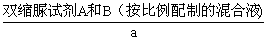 ,振荡均匀后,在
,振荡均匀后,在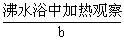 颜色变化。
颜色变化。
a
b
29.(14分)Ⅰ.根据以下资料回答问题。
一农田弃耕若干年后,演替为灌木阶段。请回答:
(1)群落演替如果是在从未有任何生物定居过的
裸岩、湖底开始,这种演替属于__________,
这种演替比从农田演替至顶极群落所需要的时
间_______________,主要原因是__________
和______________。
(2)如果不受到人类的破坏自然灾害,群落演替
是向着群落结构_______和___________的方向进行,物种的种类也将_______________;从能量流动的角度分析这种现象的原因
。
(3)弃耕的农田很快长满杂草,杂草和农作物利用同一资源而发生 ,最终会发生 。
(4)如果右图中曲线B、C表示该群落中植物物种数或个体数的变化,则曲线B表示 ,曲线A表示该群落所积累的 的变化
II(10分) .某些遗传病 具有家族性遗传的特征,非家族成员一般也非携带者。下图为80年代开始采用的“定位克隆法”示意图,通过对家系分析将与某种疾病相关的基因定位在某一染色体的特定部位。(表示氨基酸的三字母符号:Met--甲硫氨酸;Val--缬氨酸;Ser--丝氨酸;Leu--亮氨酸;Gln--谷氨酰胺;Pro--脯氨酸;Cys--赖氨酸)
具有家族性遗传的特征,非家族成员一般也非携带者。下图为80年代开始采用的“定位克隆法”示意图,通过对家系分析将与某种疾病相关的基因定位在某一染色体的特定部位。(表示氨基酸的三字母符号:Met--甲硫氨酸;Val--缬氨酸;Ser--丝氨酸;Leu--亮氨酸;Gln--谷氨酰胺;Pro--脯氨酸;Cys--赖氨酸)
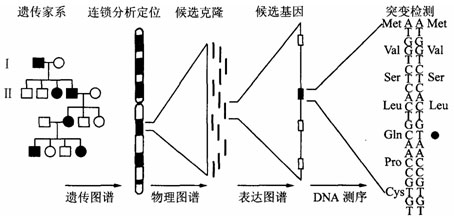
请据图回答问题:
(1)基因的本质是_______________。通过连锁分析定位,该遗传家系的遗传病致病基因最可能在_________染色体上。致病基因及等位基因用A或a表示,则患者的基因型多为_________。若此病为隐性遗传病,且在人群中的发病率为四万分之一,则人群中携带者的几率是_______________。
(2)当初步确定致病基因的位置后,需要对基因进行克隆即复制,基因克隆的原料是____种________,基因克隆必需的酶是_____________。
(3)DNA测序是对候选基因的_______进行检测。检测结果发现是基因位点发生了
,因而导致了基因突变。
28.(13分)
已知一个碳原子上连有两个羟基时,其结构极不稳定,易发生下列变化,生成较稳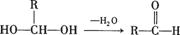 定物质:如:
定物质:如:
A-F是六种有机化合物,它们之间的关系如下图,请根据要求回答:
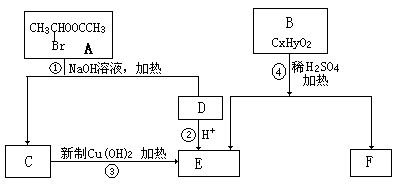
(1)在一定条件下,经反应①后,生成C和D,C的键线式为 ,反应①的类型为 。
(2)反应③的化学方程式为 。
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1,则B的分子式为 。
(4)F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
 (5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有 种结构,写出其中两种同分异构体的结构简式 、
。
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有 种结构,写出其中两种同分异构体的结构简式 、
。
27.(14分)
黄铁矿是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组对某黄铁矿石(主要成分为FeS2)进行如下实验探究。
[实验一]测定黄铁矿中硫元素的含量
Ⅰ.将m1 g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。
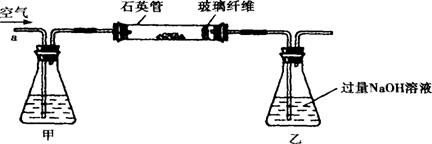
Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:
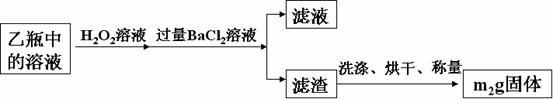
问题讨论:
(1)Ⅰ中,石英管中发生的反应方程式为 。
(2)Ⅱ中,为判断所加BaCl2是否过量,有同学设计了如下实验方案,其中合理的是
A.取少量上层清液,继续滴加BaCl2,若无沉淀产生则说明BaCl2已过量。
B.取少量上层清液,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
C.待浊液澄清后,继续滴加BaCl2,若无沉淀产生则说明BaCl2已过量。
D.待浊液澄清后,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
(3)该黄铁矿中硫元素的质量分数为 。
[实验二]测定黄铁矿中铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣;
②加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③将滤液稀释至250mL;
④取稀释液25.00mL,用浓度为0.10mol/L的酸性KMnO4溶液滴定,实验平均消耗
KMnO4溶液体积为V mL。
问题讨论:
(4)④中,需要用到的主要仪器有 ;
(5)②中,若选用铁粉作还原剂。你认为合理吗?_______,理由是 。
(6)黄铁矿中铁元素的的质量分数为 。
26.(16分)
恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。(已知:2 SO2 (g)+O2(g)  2SO3(g) △H= -196.6 KJ·mol- 1)
2SO3(g) △H= -196.6 KJ·mol- 1)
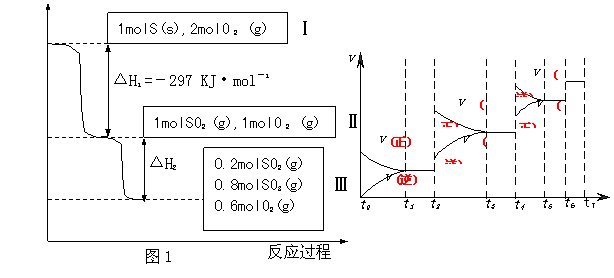

请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式: 。
(2)ΔH2 = KJ·mol-1
(3)恒温恒容时,1molSO2和2molO 2 充分反应,放出热量的数值比∣ΔH2 ∣ (填“大”“小”或“相等”)
(4)将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为 ,若溶液中发生了氧化还原反应,则该过程的离子方程式为 。
(5)恒容条件下,下列措施中能使n(SO3)/ n(SO2 )增大的有______。
a.升高温度; b.充入He气
c.再充入1molSO2 (g)和1molO 2 (g) d.使用催化剂
(6)某SO2 (g)和O 2 (g)体系,时间t1达到平衡后,改变某一外界条件,反应速率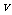 与时间t的关系如图2所示,若不改变SO2 (g)和O 2 (g)的量,则图中t4时引起平衡移动的条件可能是 _ ;图中表示平衡混合物中SO3的含量最高的一段时间是
。
与时间t的关系如图2所示,若不改变SO2 (g)和O 2 (g)的量,则图中t4时引起平衡移动的条件可能是 _ ;图中表示平衡混合物中SO3的含量最高的一段时间是
。
25.(15分)
由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样进行下列实验(部分产物略去):
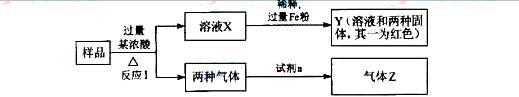
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是________________。(填化学式)
(2)如何检验Y中的金属阳离子 。
(3)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是______________________________。
②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是________________。
(4)向Y中通入过量的Cl2,并不断搅拌,充 分反应后,溶液中的阳离子是__
_。(填写离子符号)
分反应后,溶液中的阳离子是__
_。(填写离子符号)
(5)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com