
5.用于制造通讯光缆的主要原料是二氧化硅(SiO2),SiO2中硅元素的化合价是
A.+2 B.-2 C.+4 D.-4
4.保护环境,就是关爱自己。对于生产生活中的下列做法你认为正确的是
A.废旧电池随意丢弃 B.大量施用农药化肥,增加农作物产量
C.加高烟囱,减少二氧化硫的排放 D.生活污水集中处理后再排放
3.空气中含量最多的气体是
A.氧气 B.氮气 C.二氧化碳 D.稀有气体
2.(02黄冈市)下列物质中,属于纯净物的是
A.食醋 B.啤酒 C.食盐水 D.干冰
1.下列性质属于化学性质的是
A.沸点 B.硬度 C.可燃性 D.溶解性
30.回答下列何生物遗传育种有关的问题:
(1)水稻杂交育种是通过品种间杂交,创造新变异类型而选育新品种的方法。其特点是将两个纯合亲本的_____________通过杂交集中在一起,再经过选择和培育获得新品种。
(2)若这两个杂交亲本各具有期望的优点,则杂交后,F1自交能产生多种非亲本类型,其原因是F1在______________形成配子过程中,位于______________基因通过自由组合,或者位于______________基因通过非姐妹染色单体交换进行重新组合。
(3)假设杂交涉及到n对相对性状,每对相对性状各受一对等位基因控制,彼此间各自独立遗传。在完全显性的情况下,从理论上讲,F2表现型共有_____________ _种,其中纯合基因型共有______________种,杂合基因型共有______________种。
_种,其中纯合基因型共有______________种,杂合基因型共有______________种。
(4)从F2代起,一般还要进行多代自交和选择。自交的目的是______________;选择的作用是______________。
29.分析以下材料:
Ⅰ.红豆杉是我国珍贵濒危树种。南京中山植物园于上世纪50年代从江西引进一些幼苗种植于园内。经过几十年的生长繁殖,现在已形成了一个种群。请回答下列问题。
(1)在植物园引种栽培红豆杉的措施(增加/减少)_________植物园的生物多样性。
(2)如果对红豆杉种群密度进行调查,常用的方法是__________。将统计到的植株按高度(h)分为5级,每一级的植株数量见下表。
|
等级 |
a级 |
b级 |
C级 |
d级 |
e级 |
|
高度(cm) |
h≤10 |
10<h≤30 |
30<h≤lOO |
100<h≤300 |
h>300 |
|
数量(株) |
120 |
62 |
32 |
16 |
6 |
根据表中数据,在答题卡上的坐标图中画出该种群各级别的植株数量柱状图。______
(3)由表可以看出,此红豆杉种群的年龄结构属于________________。
(4)研究表明,红豆杉的种子成熟后被某种鸟类吞食,果肉状的假种皮被消化而种子随粪便散播到山坡上再萌发生长。从种间关系看,鸟类与红豆杉之间存在_________关系。
Ⅱ. 某人在持续几天咳嗽后发热,经诊断是细菌感染引发了肺炎。用药后得以康复。请回答问题:
(1)侵入人体的细菌是一种发热激活物,通过一系列反应引起人体发热。体温过高时,人体新陈代谢加快,细胞内葡萄糖氧化分解____________,耗氧量______________;由于供氧不足,肌肉组织中____________含量增高,病人会感觉肌肉酸痛。
(2)人的体温是由位于_______________的______________中枢调控的。
(3)发热到体温恢复正常的过程中,人体的_____________和______________系统参与了调节,最终实现稳态。
28.(16分)已知一个碳原子上连有两个羟基时,其结构极不稳定,易发生下列变化,生成较稳定物质: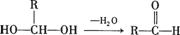 如:
如:
A-F是六种有机化合物,它们之间的关系如下图,请根据要求回答:
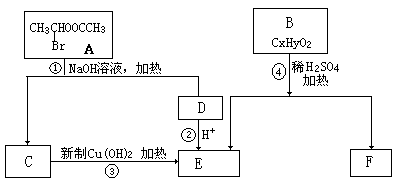
(1)在一定条件下,经反应①后,生成C和D,C的键线式为 ,反应①的类型为 。
(2)反应③的类型为 。
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2∶1,则B的分子式为 。
(4)F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的产物为 。
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有 种结构,写出其中两种同分异构体的结构简式 、 。
27.(14分)[实验一]黄铁矿是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组测定黄铁矿中硫元素的含量。
Ⅰ.将m1 g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。
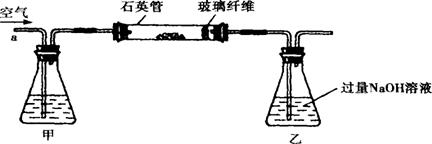
Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:
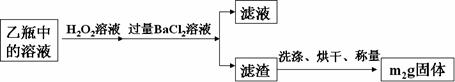
问题讨论:
(1)Ⅰ中,石英管中发生的反应方程式为 。
(2)Ⅱ中,为判断所加BaCl2是否过量,有同学设计了如下实验方案,其中合理的是
A.取少量上层清液,继续滴加BaCl2,若无沉淀产生则说明BaCl2已过量。
B.取少量上层清液,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
C.待浊液澄清后,继续滴加BaCl2,若无沉淀产生则说明BaCl2已过量。
D.待浊液澄清后,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
(3)该黄铁矿中硫元素的质量分数为 。
[实验二]某课外小组在实验室制备氨气,并进行有关氨气的性质探究。
(1)该小组同学加热生石灰与氯化铵的混合物制取干燥的氨气。
①应该选用的仪器及装置有(填字母) 。
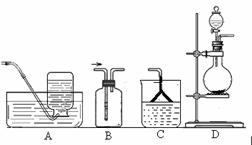

②生石灰与氯化铵反应生成氨气的化学方程式为 。
(2)该小组同学设计如图所示装置探究氨气的还原性。
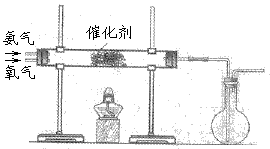
在上述过程会同时发生多个反应,其中属于置换反应的化学方程式中氧化产物和还原产物的物质的量之比_________。若实验时通入氨气的速率过快,在烧瓶中会出现白烟,该物质的化学式为 。
26.(14分)I.常温下在20mL0.1mol∙L-1Na2CO3溶液中逐滴加入0.1mol∙L-1 HCl溶液40 mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示。回答下列问题:
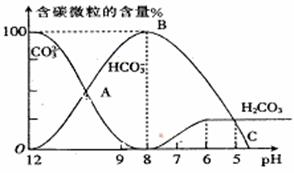
(1)H2CO3、HCO3-、CO32-中不能大量共存于同一溶液中的是___________________。
(2)实验室可用“ 双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:①取固体样品配成溶液;②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点指示剂B的变色范围在pH=_____左右最理想。
双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:①取固体样品配成溶液;②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点指示剂B的变色范围在pH=_____左右最理想。
(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是____________________。
(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh==2×10-4,当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH= 。
II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:
H2A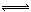 H++HA- HA-
H++HA- HA-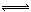 H++A2-
H++A2-
已知相同浓度时的电离度α(H2A)> α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号) :
(5)c(H+)最大的是_________,c(H2A)最大的是___________,c(A2-)最大的是_________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com