
15. 已知A、B、C是单质且C是绿色植物光合作用的产物之一,
已知A、B、C是单质且C是绿色植物光合作用的产物之一,
X、Y是化合物,它们之间的转化关系如右图(反应条件略),
下列A、B间的对应关系,不正确的是( )
A. A 是铝,B是铁 B. A 是碳,B是硅 C. A 是氢气,B是铜 D. A 是钠,B是氢气
14、下列实验操作或对实验事实的叙述正确的有几个
①用氨水清洗做过银镜反应的试管;
②配制一定物质的量浓度的溶液时,未振荡摇匀则溶液浓度偏高。
③用湿润的pH试纸测定稀盐酸的pH;
④用碱式滴定管量取20.00mL0.1mol/LKMnO4溶液
⑤将Na2CO3固体在瓷坩埚中加热熔融;
⑥不慎将苯酚溶液沾到皮肤上,立即用NaOH稀溶液清洗
⑦向沸腾的NaOH溶液中滴加FeCl3溶液,制备Fe(OH)3胶体
⑧配制FeSO4溶液时,需加入少量铁粉和稀硫酸
A.2 B.3 C.5 D.6
13、中学化学教材中有大量数据,下列为某同学对数据的利用 情况,其中不正确的是( )
A. 用NaOH和HCl 反应测得的中和热,推算一定量稀H2SO4和NaOH 溶液反应的反应热
B. 用沸点数据推测两种液体混合物用蒸馏方法分离开来的可能性
C. 用沸点数据来分析分子的稳定性
D. 用原子(或离子)半径数据比较某些原子(或离子)氧化性或还原性强弱
二选择题(每小题只有一个正确选项,每小题3分,共21分)
12、短周期元素W、X、Y、Z的原子序数依次增大,W与Y、X与Z位于同一主族。W与X可形成共价化合物WX2,Y原子的内层电子总数是其最外层电子数的2.5倍。下列叙述中不正确的是
A. WX2分子中所有原子最外层都为8电子结构
B. WX2、ZX2的化学键类型和晶体类型都相同
C. WX2是以极性键结合成的非极性分子
D. 原子半径大小顺序为X<W<Y<Z
11、设NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.7.8gNa2O2与足量水反应中电子转移了0.2NA
B.在0.1mol熔融KHSO4中,含有0.1NA个SO42-
C.常温常压下,4.4gCO2和N2O的混合物中所含有的原子数为0.3NA
D.80mL 10mol/L浓盐酸与足量MnO2反应,转移电子数为0.4NA
10. 把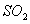 通入
通入 溶液中,溶液由黄色变为浅绿色,但立即又变为黄色,此时若滴
溶液中,溶液由黄色变为浅绿色,但立即又变为黄色,此时若滴
人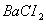 容液,则会产生白色沉淀。在上述一系列变化过程中,最终被还原了的是( )
容液,则会产生白色沉淀。在上述一系列变化过程中,最终被还原了的是( )
A.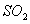 B、
B、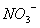 C
C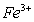 D、
D、
9.已知 均具有相同的电子层结
构,对A、B、C、D四种短周期元素的叙述正确的是( )
A.原子半径:A > B > C > D B.原子序数:b> a >c >d
C.离子半径: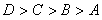 D.金属性:
D.金属性: ;非金属性::
;非金属性::
8、下列离子方程式正确的是 ( )
A.用醋酸除去水垢:CaCO3 + 2H+ =Ca2+ + H2O + CO2↑
B.Ca(HCO3)2与过量Ca(OH)2溶液:Ca2++2HCO3-+2OH- = CaCO3↓+CO32-+2H2O
C.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O ==2HCO3-+SO32-
 D.用稀HNO3溶解FeS固体:FeS+2H+=Fe2++H2S↑
D.用稀HNO3溶解FeS固体:FeS+2H+=Fe2++H2S↑
7、一定温度下,向饱和碳酸钠溶液中通入足量的CO2气体,忽略溶液体积的变化,下列有关说法中正确的是
A.c(Na+)不变 B.溶液的pH变大
C.溶液质量增大 D.溶液中溶质的质量分数变小
6.叠氮酸钠(NaN3)是抗禽流感药物“达菲”合成过程中的中间活性物质,3mol
NaN3受撞击会生成4mol 氮气和离子化合物(Na3N)。下列有关叙述错误的是( )
A.NaN3受撞击时,既是氧化剂又是还原剂 B.NaN3跟水反应时,有NH3生成
C.Na3N中N3-半径比Na+半径大 D.NaN3中,既存在离子键又存在非极性共价键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com