
3.用NA表示阿伏加德罗常数,下列叙述中正确的是( )。
A. 0.1 mol/L稀H2SO4中含SO42-个数为0.1NA
B. 2.4 g Mg与足量盐酸反应,转移电子数为0.1NA
C. 1 mol NH3中含有的电子数为10NA
D. 标准状况下22.4 L SO3中含有氧原子数为3NA
2.已知充分燃烧a g 乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是( )
A.2C2H2(g) + 5O2(g) == 4CO2(g) + 2H2O(l);△H = -4b KJ/mol
B.C2H2(g) + 5/2O2(g) == 2CO2(g) + H2O(l);△H = 2b KJ/mol
C.2C2H2(g) + 5O2(g) == 4CO2(g) + 2H2O(l);△H = -2b KJ/mol
D.2C2H2(g) + 5O2(g) == 4CO2(g) + 2H2O(l);△H = b KJ/mol
1.化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C.MgO的熔点很高,可用于制作耐高温材料
D.电解MgCl2饱和溶液,可制得金属镁
(一)、命题作文
1.请以“脚比路远”为题写一篇文章。(60分)
写作提示: 可以写人的意志与决心。
2.请以“门槛”为题写一篇文章。(60分)
写作提示: 可以写显示生活中的种种现象。
3.请以“做梦与圆梦”为题写一篇文章。(60分)
写作提示: 可以写理想与奋斗。
4.请以“清水与混水”为题写一篇文章。(60分)
写作提示: 可以写事物的相互转化。
5.请以“宜与不宜”为题写一篇文章。(60分)
写作提示: 可以写做事的取舍。
6.请以“给心灵一次沐浴”为题写一篇文章。(60分)
写作提示: 可以写人生思考,情感体验,生命感悟。
7.请以“降温”为题写一篇文章。(60分)
写作提示: 可以写清醒、反思。
8.请以“底线”为题写一篇文章。(60分)
写作提示: 可以写道德、节操。
9.请以“学会倾听”为题写一篇文章。(60分)
写作提示: 可以写坦荡的胸怀。
10.请以“手”为题写一篇文章。(60分)
写作提示: 可以写人的智慧与创造性。
11.请以“山寨一路红?”为题写一篇文章。(60分)
写作提示: 可以写思辨思想。
⑴命题形式会稳中求变,审题难度不会太大;
⑵新材料作文、命题作文平分秋色,话题作文将会很少出现;
⑶2008年以命题作文形式进行考查的地区,2009年应注重对材料作文的训练;2008年以材料作文形式进行考查的地区,2009年则须注重对命题作文的训练;
⑷2009年作文命题将会更加关注生活,贴近考生生活实际,让考生有话可说,有理可论;让考生以自己所知之事打动人,以自己所明之理说服人,以自己所倾之情感染人;
⑸注重考查考生的想象能力,注重考查考生的领悟、思辨能力以及语言表达能力等;
⑹鼓励个性写作,大胆张扬个性, 努力使自己的作文有个性特征;
⑺强调内容丰富。 “丰富”是作文考查的重点之一, 2009年高考作文可能会在这方面有更高的要求;
30.(16分)资料显示不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为10lkPa,温度为0℃)。
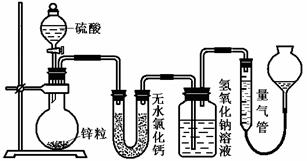
(1)若在烧瓶中放入1.30g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,量气管的适宜规格是_____________ (选填:200,400,500) mL 。
(2)若1.30g锌粒完全溶解,氢氧化钠洗气瓶增重l.28g ,则圆底烧瓶中发生反应的化学方程式为:________________________________________
(3)若烧瓶中投入ag锌且完全反应,氢氧化钠洗气瓶增重b g.量气瓶中收集到VmL气体,则有:ag/65g·mol-1=bg/64g·mol-1+V mL / 22400 mL·mol-1,依据的原理是____________________________。
(4)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中,n(H2)/n(SO2)=_______________(用含字母的代数式表示)。
(5) 反应结束后,为了准确地测量气体体积,量气管在读数时应注意:
、 、
。
29.(14分) 甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:
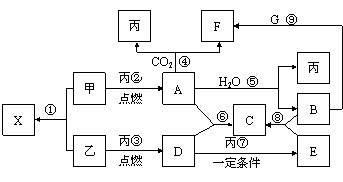
(1)写化学式:丙 E________
(2)X的电子式为_____________。
(3)写出反应⑥的化学反应方程式: 。
(4)写出B与G溶液反应生成F的离子方程式: 。
(5)在上图的反应中,不属于氧化还原反应的是(填序号)____________________。
(6)将8 g 乙在足量丙中燃烧,所得气体D通入100mL 3.5mol·L-1的B溶液中,完全吸收后,溶液中的溶质及其物质的量分别为 ;若同体积的气体D通入100mL 2.5mol·L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为 。
28.(10分)某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-,取该溶液进行如下实验:
① 用蓝色石蕊试纸检测该溶液,试纸显红色; 。
② 取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色;
③ 取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④ 取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤ 取实验 ④ 后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。
请回答下列问题:
⑴用简要语言描述在实验 ① 中的操作
⑵根据上述实验判断原溶液中肯定存在的离子是______________,
肯定不存在的离子是
⑶写出与②③两个实验有关的离子方程式:
②___________________________ ③_________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com