
5.下列式子能确定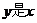 的函数是
的函数是
①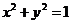 ②
②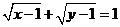 ③
③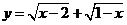
A.①② B.②③ C.② D.③
4.设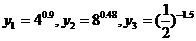 ,则
,则
A. 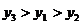 B.
B.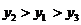 C.
C.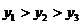 D.
D.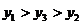
3.下列函数中,值域为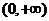 的函数为
的函数为
A.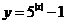 B.
B.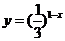 C.
C.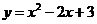 D.
D.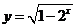
2.设全集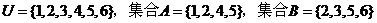 ,则
,则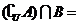
A.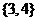 B.
B. C.
C.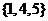 D.
D.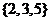
1.设集合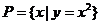 ,集合
,集合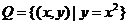 ,则P、Q的关系是
,则P、Q的关系是
A.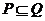 B.
B.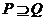 C.
C.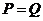 D.以上都不对
D.以上都不对
21.(9分)标准状况下的甲烷和一氧化碳的混合气体8.96L,其质量为7.60g,则混合气体平均相对分子质量为____________;混合气体中一氧化碳的体积为_________,甲烷的质量为___________。
|
(1)葡萄糖的摩尔质量为_________________。
(2)该溶液中含水________g。
该溶液的密度约为_______g·mL-1。
(3)该溶液的物质的量浓度为___________ mol·L-1
(精确到小数点后面两位)。
(4)血液中甘油三酯(假设其化学式为C55H104O6,M=860)的含量是人体健康重要参数。正常人的甘油三酯的含量为0. 8~2.2mmol/L。在某次体检中,测得某被检者血液的密度为0.99g·mL-1,血液中甘油三酯的质量分数为1.72‰,则该被检者甘油三酯的含量________(填“偏低”、“正常”、“偏高”或“无法确定”)。
20.(9分)解答下列各题。
(1)在标准状况下,0.5 mol H2的体积是_______,质量是______,分子数是__________。
(2)标准状况下,某气体的密度是1.25g/L,该气体的相对分子质量是_______。
(3)电解36g H2O可得到标准状况下的H2______L,O2_____L。
(4)在相同的温度和压强下,相同质量的CH4、O2两种气体的体积比为________;相同体积的两种气体的质量比为_________,物质的量比为__________。
19.(11分)实验室欲配制0.05 mol/L的NaOH溶液500 mL。有以下仪器:①烧杯、②100 mL量筒、③100 mL容量瓶、④500 mL容量瓶、⑤玻璃棒、⑥托盘天平(带砝码)
(1)配制时,必须使用的仪器有_______(填代号),还缺少的仪器是______________。该实验中两次用到玻璃棒,其作用分别是_____________________________,____________
________________。
(2)使用容量瓶前必须进行的一步操作是_______________________。
(3)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其正确的操作顺序为___________(用序号填写)。在①操作中需称量NaOH_______g。
(4)若某学生用托盘天平称量药品时,在托盘天平左盘放有20g砝码,天平达平衡时游码的位置如图,则该同学所称量药品的质量为__________________。
(5)在用98%的浓H2SO4配制2 mol/L的H2SO4溶液的实验中,以下
操作中会引起所配稀H2SO4溶液浓度偏高的是_______。
A.洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
B.稀释后的H2SO4溶液未冷却趁热转移到容量瓶中
C.容量瓶中原有少量蒸馏水
D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管滴加蒸馏水至刻度线
E.定容时俯视
18.(8分)为了除去粗盐中含有的可溶性杂质CaCl2、MgCl2和Na2SO4,需进行下列实验操作,请在( )中填写所使用除杂试剂的化学式,在[ ]中填写实验操作名称。
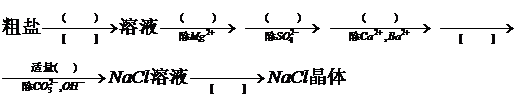
17.(5分)用下列仪器的编号回答问题。
①容量瓶 ②蒸馏烧瓶 ③蒸发皿 ④量筒 ⑤烧杯 ⑥托盘天平
(1)标有温度的是_________。
(2)标有零刻度的是_________。
(3)常用于溶解固体物质的是_________。
(4)加热时必须垫石棉网的是__________。
(5)使用时必须检查是否漏水的是____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com