
3.下列氯化物中,不能用金属与氯气直接化合而生成的是( )
A. 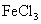 B.
B. 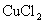 C.
C. 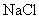 D.
D. 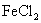
1.下列关于氯水的叙述不正确的是( )
A.新制氯水长期放置后颜色会逐渐褪色为无色
B.长期放置的氯水也能使有色布条褪色
C.长期放置的氯水中含有的 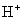 多于新制氯水
多于新制氯水
D.新制氯水中含有的阳离子只有
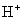
2下列关于氯气的说法不正确的是( )
A. 尽管氯气的化学性质很活泼,但是干燥的液氯能用钢瓶贮存。
B. 氯气和液氯是两种不同的物质
C. 可以用浓硫酸除去氯气中的水蒸气。
D. 氯气有毒,它曾在战争中被用于制造毒气弹
11.现有制取气体的装置如图所示
(1) 下列气体①HCl ②CO2③Cl2④H2能用上述装置制取的是______________
(2) 固体D可能是下列物质:①MnO2②CaCO3③NaCl④Zn中的(填序号)。
(3) 长颈漏斗内的液体C可能是①稀硫酸②浓硫酸③稀盐酸④浓盐酸⑤稀硝酸⑥浓硝酸中的__________________
(4) 发生器内小试管A的作用是___________________
(5) 洗气瓶B内浓磷酸的作用是___________________
(6) 如何检验集气瓶内是否充满气体?_________________________________48
12写出下列反应的化学方程式(如果是离子反应,请写出离子反应方程式)
⑴将氯气通入氢氧化钠溶液中
⑵盐酸和二氧化锰混合加热
⑶亚硫酸钠溶液和稀硫酸的反应
⑷氧化铁和盐酸的反应
⑸氧化铜和硫酸的反应
⑹过量二氧化碳通入澄清石灰水
⑺二氧化硫和足量氢氧化钠溶液的反应
⑻铁片加入到硫酸铜溶液中
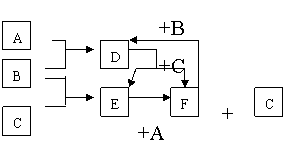 13A、B、C是中学化学中常见的三种元素的单质。A、B、C及其他物质反应的关系如下图示,其中B、D、E溶液呈酸性,又知常温下B为气体:
13A、B、C是中学化学中常见的三种元素的单质。A、B、C及其他物质反应的关系如下图示,其中B、D、E溶液呈酸性,又知常温下B为气体:
请回答:
⑴三种单质分别是:
A._________B.___________C._______________.
 ⑵B与C反应生成E时的反应现象是:_____________.
⑶写出下列反应的离子方程式:
⑵B与C反应生成E时的反应现象是:_____________.
⑶写出下列反应的离子方程式:
 F+B D_______________________________________.
F+B D_______________________________________.
 D+C E+F____________________________________.
D+C E+F____________________________________.
⑷E溶液显酸性的离子方程式:____________________.
14用水吸收氯化氢气体来制备溶质的质量分数为36.5%、溶液密度1.18
g.cm-3的盐酸,计算1L水吸收氯化氢气体的确体积(标准状况)是多少?
15计算工业用消石灰和氯气反应制取漂白粉的有效率是多少?(假设消石灰完全反应)(提示:漂白粉的主要成分是Ca(ClO)2和CaCl2,有效率是求Ca(ClO)2的质量分数)
选择题
9.
 (2000年全国,12)氯气通入石灰乳得漂白粉,其主要成分是Ca(OH)2。3CaCl(ClO)·
(2000年全国,12)氯气通入石灰乳得漂白粉,其主要成分是Ca(OH)2。3CaCl(ClO)·
nH2O。一定质量的漂白粉和一定浓度的盐酸完全反应,生成Cl2的质量与参加反应的漂
白粉质量之比可标志“有效氯”的多少。如果某漂白粉测其“有效氯”的质量分数为
35%,该漂白粉的组成和上述化学式相符时,求式中的n值。
A.. 6.5 B. 8 C. 8.5 D. 10
10下图A处通入Cl2,当关闭B阀时,C处湿润
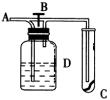 的红布条没有明显变化;当打开B阀时,C处的
的红布条没有明显变化;当打开B阀时,C处的
湿润红布条逐渐退色。则D瓶中装的溶液是
( )35
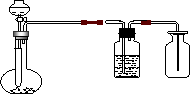 A.H2SO4 B.NaOH溶液 C.水 D.饱和溶液
A.H2SO4 B.NaOH溶液 C.水 D.饱和溶液
2.市场上销售的“84”消毒液,其商品标识上有如下叙述:①本品为无色液体,呈碱性;
②使用时需加水稀释;③可对餐具、衣物进行消毒,可漂白浅色衣物。据此,可推测其有效成分可能是
A.氯气 B.二氧化硫 C.次氯酸钠 D.高锰酸钾
3氯化碘(ICl )的化学性质跟氯气相似,预计它跟水反应的最初生成物是( )
A.HI 和HClO B. HCl 和HIO C. HClO 3 和HIO D. HClO 和 HIO
4下列物质中不会因见光而分解的是( )
A.NaHCO3 B.HNO3 C.AgI D.HClO
5下列关于氯水的叙述正确的是( )
A.新制氯水只含Cl2和 H2O 分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水放置数天后溶液的PH将变小
6下列物质不与氯水反应的是( )
①NaOH溶液 ②H2S溶液 ③AgNO3溶液 ④品红溶液⑤镁粉⑥ SO2 ⑦FeSO4溶液 ⑧Fe(NO3)3 ⑨NaHCO3 溶液
A.只有 ④ B.只有⑧ C. ④⑥⑧ D. ④⑥⑧⑨
7 向混合溶液中,通入一定量的氯气后,将溶液蒸干并灼烧,得到的剩余固体的组成可能是( )
A.NaCl Na2SO4 B.NaCl NaBr Na2SO4
C.NaCl Na2SO4 I2 D.NaCl NaI Na2SO4
8有标准状况下的H2 Cl2混合气,经光照反应后,所得气体恰好能使bmol NaOH 溶液完全变成盐,那么a和b的关系不可能是( )
A.b=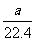 B.b<
B.b<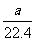 C b.>
C b.>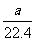 D. b
D. b
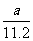
1.自来水用适量氯气杀菌消毒。不法商贩运用自来水冒充纯净水谋取暴利,可用化学试剂辨别真伪,该试剂可以是
A.酚酞试液 B.氯化钡溶液 C.氢氧化钠溶液 D.硝酸银溶液
[例1](2001年全国春季,3)放在敞口容器中的下列溶液,久置后溶液中该溶质的浓度会变大的是
A.浓硫酸 B.氢氧化钠 C.氯水 D.氯化钠
[例2]1996 年上海,14)检验氯化氢气体中是否混有氯气,可采用的方法是
A.用干燥的蓝色石蕊试纸 B.用干燥的有色布条
C.硝酸银溶液 D.湿润的碘化钾淀粉试纸
[例3](2002年全国理综,25)已知:①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z。元素Y、X、Z的核电荷数依次递增。②X在A、B、C、D中都不呈现它的最高化合价。③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是_______,Z是_______。(2)写出③中反应的化学方程式:
_____________________。(3)写出④中反应的化学方程式_______________________
1氯气为双原子分子,分子式为 ____________,电子式为________,结构式为________,键的极性是__________,分子极性为____________。
2通常情况下,氯气是_________色、有_______气味的、有毒气体,密度比空气______,易液化(沸点-34.6℃),能溶于水,在饱和食盐水中的溶解度较____,在有机溶剂中溶解度较________。
3化学性质
a.氯气与金属的反应:金属+Cl2→高价金属氯化物
|
金属 |
化学反应式 |
现象 |
说明 |
 ①钠 ①钠 |
|
|
|
|
②铜 |
|
|
|
|
③铁 |
|
|
|
b.氯气与非金属的反应
|
非金属 |
化学方程式 |
现象 |
说明 |
 ①氢气(点燃) ①氢气(点燃) |
|
|
|
|
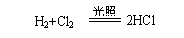
②氢气(光照) |
|
|
|
|
③磷(点燃) |
|
|
|
C氯水与液氯的比较
|
|
氯 水 |
液 氯 |
|
物质类别 |
|
|
|
微粒种类 |
|
|
|
主要性质 |
|
|
|
保存方法 |
|
|
讨论:⑴向新制氯水中滴入紫色石蕊溶液,现象是_________.
⑵新制氯水与久置氯水有何区别?
⑶次氯酸有哪些主要化学性质?
d.氯气与碱溶液反应
Cl2+2NaOH==____________________
Cl2+NaOH ___________________
___________________
Cl2+Ca(OH)2===__________________
讨论:漂白粉的主要成分和有效成分各是什么?漂白粉如何产生漂白作用?
e.与某些还原性化合物反应
还原性物质_________________等都能被氯气氧化。
讨论 ⑴用湿润的KI淀粉试纸检验Cl2的方程
⑵用浓氨水检验氯气管道是否漏气的方程
⑶等物质的量的SO2 Cl2通入品红溶液中
f氯气与有机物的反应(取代反应和加成反应各举一例)
4氯气的实验室制法
|
|
具体内容 |
说明 |
|
①反应原理 |
|
(1)若没有浓盐酸时,可用浓硫酸与固体食盐和MnO2的混合物共热。 (2)若没有MnO2时可用KMnO4代替,此时可不加热,则选用发生装置不同。 |
|
②制气类型 |
|
|
|
③发生装置 |
|
|
|
④收集方法 |
|
|
|
⑤净化方法 |
|
|
|
⑥验满方法 |
|
|
|
⑦尾气处理 |
|
5氯气的工业制法
14.(1)碳(或C)
(2)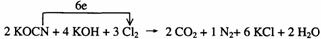
(3)35.5
13.(1)2NO+O2=2NO2 3O2=2O3 (2)CH3CH=CHCH3 + 2O3→ 2CH3CHO+ 2O2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com